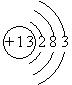
短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
(1)X的离子结构示意图为
;J的电子式是
.
(2)若A是与X、Y同周期的一种常见金属单质,则A与B溶液反应的化学方程式是
2Al+2NaOH+2H2O=2NaAlO2+3H2↑(或2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑)
2Al+2NaOH+2H2O=2NaAlO2+3H2↑(或2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑)
.
(3)若A是一种常见酸性氧化物,且可用于制造玻璃,则E与F反应的离子方程式是
SiO32-+2H+=H2SiO3↓
SiO32-+2H+=H2SiO3↓
.
(4)将一定量F和H的水溶液混合使其溶液显碱性,则此溶液中离子浓度由大到小的顺序是
c(NH4+)>c(Cl-)>c(OH-)>c(H+)
c(NH4+)>c(Cl-)>c(OH-)>c(H+)
.
(5)汽油是一种可燃性液体,汽油-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,该电池放电时的正极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.



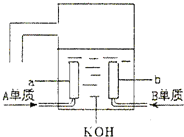 A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素;已知B、D二元素原子核中质子数之和是A、C二元素原子核中质子数之和的2倍;四种元素形成的单质中有两种是气体,两种是固体.请回答以下问题:
A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素;已知B、D二元素原子核中质子数之和是A、C二元素原子核中质子数之和的2倍;四种元素形成的单质中有两种是气体,两种是固体.请回答以下问题:
 短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则: