
题目列表(包括答案和解析)
(12分)(1)环境专家认为可以用铝将水中的NO3- 转化为N2 ,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(不用配平)。
NO3-+ + → + +
该反应过程中,被氧化与被还原的元素的物质的量之比为 。
(2)若4Al(s)+3O2(g)=2 Al2O3(s) △H= a KJ/mol
C(s)+O2(g)=CO2(g) △H= c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式: 。
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mLPH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如上图:则反应过程中产生氢气的总体积为 L(标准状况)。
(12分)(1)环境专家认为可以用铝将水中的NO3-转化为N2 ,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(不用配平)。
NO3- + + → + +
该反应过程中,被氧化与被还原的元素的物质的量之比为 。
(2)若4Al(s)+3O2(g) ="2" Al2O3(s) △H=" a" KJ/mol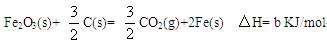
C(s)+O2(g)=CO2(g) △H=" c" KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式: 。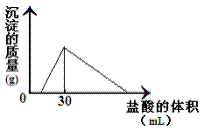
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如上图:则反应过程中产生氢气的总体积为 L(标准状况)。
(12分)(1)环境专家认为可以用铝将水中的NO3- 转化为N2 ,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3- 、N2,请将各粒子分别填入以下空格(不用配平)。
NO3- + + → + +
该反应过程中,被氧化与被还原的元素的物质的量之比为 。
(2)若4Al(s)+3O2(g) =2 Al2O3(s) △H= a KJ/mol
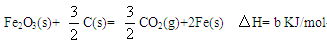
C(s)+O2(g)=CO2(g) △H= c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式: 。
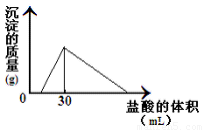
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如上图:则反应过程中产生氢气的总体积为 L(标准状况)。
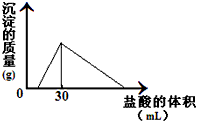
(1)环境专家认为可以用铝将水中的NO3- 转化为N2 ,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3- 、N2,请将各粒子分别填入以下空格(不用配平)。
NO3- + + → + +
该反应过程中,被氧化与被还原的元素的物质的量之比为 。
(2)若4Al(s)+3O2(g) =2 Al2O3(s) △H= a KJ/mol
![]()
C(s)+O2(g)=CO2(g) △H= c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式: 。
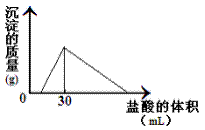
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如上图:则反应过程中产生氢气的总体积为 L(标准状况)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com