
题目列表(包括答案和解析)
下列说法正确的是
A.已知反应CH4(g)+2O2(g)→CO2(g)+2H2O(1) 其△S>0
B.对有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.在滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液,溶液褪色
D.在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si
下列说法正确的是
A.已知反应CH4(g)+2O2(g)=CO2(g)+2H2O(l) ,其ΔS>0
B.已知反应X+Y= M+N为放热反应, X和Y的总能量一定高于M和N的总能量
C.活化分子之间发生的碰撞一定为有效碰撞
D.对有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
下列说法正确的是( )
A.在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的 ΔH =" —40.69" kJ·mol-1 H2O(l) 的 ΔH =" —40.69" kJ·mol-1 |
| B.在25℃、101kPa,2mol S的燃烧热是1mol S的燃烧热2倍 |
| C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH代表燃烧热 |
| D.已知: |
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
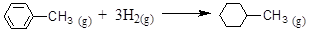 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1A.在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的 ΔH =" —40.69" kJ·mol-1 H2O(l) 的 ΔH =" —40.69" kJ·mol-1 |
| B.在25℃、101kPa,2mol S的燃烧热是1mol S的燃烧热2倍 |
| C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH代表燃烧热 |
| D.已知: |
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
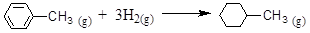 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com