
جâؤ؟ءذ±ي(°üہ¨´ً°¸؛ح½âخِ)

تµرéت±سذبçدآ²ظ×÷£؛
A.½«´إ¹ـضذرùئ·¼سببµ½800،ھ850 ،و،£
B.³ئب،رذد¸µؤ»ئجْ؟َرùئ·،£
C.ء¬½س؛أب«²؟زائ÷£¬²¢¼ى²éئنئّأـذش،£
D.½«رùئ·ذ،ذؤ·إبëس²ضت´إ¹ـضذ²؟،£
E.زش¾ù؛مµؤثظ¶ب²»¶د¹ؤبë؟صئّ،£
F.سأ±ê×¼µâبـز؛µخ¶¨؛¬µي·غµؤSO2ث®بـز؛،£
£¨1£©صب·µؤتµرé²½ضèµؤ´خذٍتا£¨زشA،¢B،،µؤذٍ؛إ±يت¾£©_______________،£
£¨2£©×°ضأ¢ظµؤ×÷سأتا_______________£»×°ضأ¢عµؤ×÷سأتا_______________،£
£¨3£©µâ¸ْSO2ث®بـز؛·´س¦µؤہë×س·½³جت½تا_____________________________________،£
£¨4£©¸ù¾ف______________________________دضدَإذ¶دµخ¶¨زر´ïµ½ضصµم،£
£¨5£©سذح¬ر§بدخھسأةدتِ×°ضأ²â³ِµؤ»ئجْ؟َضذءٍشھثطµؤضتء؟·ضتح¨³£½«ئ«µح£¬ؤمتا·ٌح¬زâ¸أ¹غµم_______________£¨جî،°تا،±»ٍ،°·ٌ،±£©£¬اëثµ³ِؤمµؤض÷زھہيسة_______________________،£
£¨6£©¼ظ¶¨؟َرùضذµؤءٍب«²؟×ھ»¯خھSO2£¬²¢ب«²؟±»ث®خüتص،£بô³ئµأ؟َرùµؤضتء؟خھ0.090 0 g£¬µخ¶¨¹ـضذµâبـز؛µؤ³ُ¶ءتخھ1.10 mL£¬ؤ©¶ءتخھ25.60 mL£¬±ê×¼µâبـز؛µؤإ¨¶بخھ0.050 0 mol،¤L-1£¬شٍ¸أ»ئجْ؟َرùئ·ضذءٍشھثطµؤضتء؟·ضتخھ_______________،£
(1)بôإنضئ´َش¼1 mol،¤L-1µؤبـز؛100 mL£¬ثù¸ّزائ÷ض»سذحذإججىئ½،¢ء؟ح²،¢´ّ؟ج¶بµؤةص±،¢²£ء§°ô£¬دآءذ؟ةر،سأµؤتش¼ءتا__________(ر،جî×ضؤ¸ذٍ؛إ)،£
A.اâرُ»¯ؤئ¹ججه B.إ¨ءٍثل(98£¥) C.إ¨رخثل(37£¥) D.إ¨دُثل(63£¥)
(2)دآح¼تاؤ³ر§ةْشعإنضئ0.100 mol،¤L-1µؤج¼ثلؤئبـز؛100 mLت±£¬½«µعز»´خد´µسز؛×ھزئµ½بفء؟ئ؟ؤعµؤ²ظ×÷،£
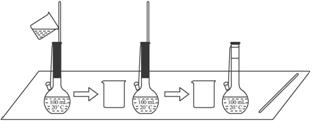
¸أ²½²ظ×÷¶شثùµأبـز؛إ¨¶بµؤس°دىتا__________(جî،°ئ«¸ك،±،°ئ«µح،±»ٍ،°خقس°دى،±)£¬شزٍتا_______
_____________________________________________________________________،£
(3)بôإنضئ(2)ضذبـز؛ت±£¬¸أةْت¹سأحذإججىئ½³ئب،ج¼ثلؤئ£¬شٍسë¼ئثمء؟ز»ضآآً?خھت²أ´?_______
____________________________________________________________________،£
(4)دضسأزئز؛¹ـ×¼ب·ء؟ب،20.0 mL 0.100 mol،¤L-1µؤج¼ثلؤئبـز؛£¬×¢بë׶ذخئ؟ضذµخ¼س¼×»ù³بتش¼ء2،ھ3µخ£¬´ثت±بـز؛³ت__________ة«،£ب»؛َ½«´²âد،رخثل×¢بë½à¾»،¢¸ةشïµؤµخ¶¨¹ـؤع£¬¼ادآµخ¶¨¹ـؤعد،رخثلµؤ³ُت¼؟ج¶ب¶ءت£¬½س×إ؟ھت¼دٍ׶ذخئ؟ؤعµخ¼سرخثل،£µ±×¶ذخئ؟ؤعبـز؛رصة«ح»±ن³ة__________ة«ت±¼´´ïµ½µخ¶¨ضصµم£¬´ثت±دû؛ؤرخثلجه»خھ21.36 mL£¬شٍ´²âرخثلµؤإ¨¶بخھ__________ mol،¤L-1،£
إنضئز»¶¨خïضتµؤء؟إ¨¶بµؤبـز؛تاتµرéتز½ّذذ؟ئر§رذ¾؟µؤضطزھ»·½ع،£
(1)بôإنضئ´َش¼1 mol،¤L-1½ذµؤبـز؛100 mL£¬ثù¸ّزائ÷ض»سذحذإججىئ½،¢ء؟ح²،¢´ّ؟ج¶بµؤةص±،¢²£ء§°ô£¬دآءذ؟ةر،سأµؤتش¼ءتا (جî×ضؤ¸ذٍ؛إ)،£
A£®اâرُ»¯ؤئ¹ججهB£®إ¨ءٍثل(98£¥) C£®إ¨رخثل(37£¥) D£®إ¨دُثل(63£¥)
(2)دآح¼تاؤ³ر§ةْشعإنضئ0.100 mol،¤L-1µؤج¼ثلؤئبـز؛100 mLت±£¬½«µعز»´خد´µسز؛×ھزئµ½بفء؟ئ؟ؤعµؤ²ظ×÷،£
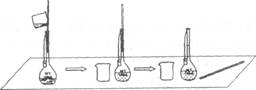
¸أ²½²ظ×÷¶شثùµأبـز؛إ¨¶بµؤس°دىتا (جî،°ئ«¸ك،±،¢،°ئ«µح،±»ٍ،°خقس°دى،±)£¬شزٍتا
.
(3)بôإنضئ(2)ضذبـز؛ت±£¬¸أةْت¹سأحذإججىئ½³ئب،ج¼ثلؤئ£¬شٍسë¼ئثمء؟ز»ضآآً?خھت²أ´?
.
(4)دضسأزئز؛¹ـ×¼ب·ء؟ب،20.0 mI،£0.100 mol،¤L-1إخج¼ثلؤئبـز؛£¬×¢بë׶ذخئ؟ضذµخ¼س¼×»ù³بتش¼ء2،«3µخ£¬´ثت±بـز؛³ت ة«،£ب»؛َ½«´²âد،رخثل×¢بë½à¾»،¢¸ةشïµؤµخ¶¨¹ـؤع£¬¼ادآµخ¶¨¹ـؤعد،رخثلµؤ³ُت¼؟ج¶ب¶ءت£¬½س×إ؟ھت¼دٍ׶ذخئ؟ؤعµخ¼سرخثل،£µ±×¶ذخئ؟ؤعبـز؛رصة«ح»±ن³ة ة«ت±¼´´ïµ½µخ¶¨ضصµم£¬´ثت±دû؛ؤرخثلجه»خھ21.36 mI،££¬شٍ´²âرخثلµؤإ¨¶بخھ mol،¤L-1،£
£¨17·ض£©تµرéتز؟ةہûسأ¼×´¼،¢؟صئّ،¢حضئ±¸¼×ب©£¬¹طسع¼×´¼؛ح¼×ب©µؤ·ذµم؛حث®بـز؛ذش¼ûدآ±ي£؛
| ·ذµم/،و | ث®بـذش | |
| ¼×´¼ | 65 | سëث®دàبـ |
| ¼×ب© | ¨D21 | سëث®دàبـ |
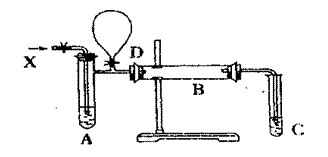
دآح¼تاؤ³خ»ح¬ر§ةè¼ئµؤتµرé×°ضأ£¬ئنضذD´¦µؤئّاٍشع·´س¦½لتّت±ت¹سأ،£
![]()
 |
![]()
![]()
![]()
![]()
![]()
![]()
![]() اë»ط´ً£؛
اë»ط´ً£؛
![]() £¨1£©ح¨حùAتش¹ـµؤXتا £¬B¹ـضذ·¢ةْ·´س¦µؤ»¯ر§·½³جت½خھ ،£
£¨1£©ح¨حùAتش¹ـµؤXتا £¬B¹ـضذ·¢ةْ·´س¦µؤ»¯ر§·½³جت½خھ ،£
![]() £¨2£©Cتش¹ـضذ×°بëµؤتش¼ءتا £¬¹ـؤعتص¼¯µ½µؤخïضتسذ ،£
£¨2£©Cتش¹ـضذ×°بëµؤتش¼ءتا £¬¹ـؤعتص¼¯µ½µؤخïضتسذ ،£
![]() £¨3£©¶ش×°ضأضذµؤA،¢B،¢C»¹ذèزھ²ةب،ت²أ´´ëت©£¨تµرéتزجل¹©سأئ·£©£¬²إؤـت¹تشرéث³ہû½ّذذ£؛¶شAتا £»¶شBتا £»¶شCتا ،£
£¨3£©¶ش×°ضأضذµؤA،¢B،¢C»¹ذèزھ²ةب،ت²أ´´ëت©£¨تµرéتزجل¹©سأئ·£©£¬²إؤـت¹تشرéث³ہû½ّذذ£؛¶شAتا £»¶شBتا £»¶شCتا ،£
![]() £¨4£©·´س¦½لتّت±£¬¶شD´¦ئّاٍµؤ²ظ×÷تا ،£
£¨4£©·´س¦½لتّت±£¬¶شD´¦ئّاٍµؤ²ظ×÷تا ،£
![]()
 ¢ٌ£®تزخآت±1L 0.01mol?L-1µؤءٍثلاâؤئبـز؛µؤpHخھ
¢ٌ£®تزخآت±1L 0.01mol?L-1µؤءٍثلاâؤئبـز؛µؤpHخھ| µخ¶¨´خت | ´²âجه»£¨mL£© | ±ê×¼ةص¼îجه»£¨mL£© | |
| µخ¶¨ا°¶ءت | µخ¶¨؛َ¶ءت | ||
| µعز»´خ | 20.00 | 0.40 | 20.40 |
| µع¶´خ | 20.00 | 2.00 | 24.10 |
| µعب´خ | 20.00 | 4.00 | 24.00 |
¹ْ¼تر§ذ£سإر، - ء·د°²لءذ±ي - تشجâءذ±ي
؛±±ت،»¥ءھحّخ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨ئ½ج¨ | حّةدسذ؛¦ذإد¢¾ظ±¨×¨اّ | µçذإص©ئ¾ظ±¨×¨اّ | ةوہْت·ذéخقض÷زهسذ؛¦ذإد¢¾ظ±¨×¨اّ | ةوئَاضب¨¾ظ±¨×¨اّ
خ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨µç»°£؛027-86699610 ¾ظ±¨ستدن£؛58377363@163.com