
题目列表(包括答案和解析)

 N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.
N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.| 时间/h | 1 | 2 | 3 | 4 | 5 | |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |

(1)在如图甲所示的装置中,烧瓶中充满干燥气体A,将滴管中的液体B挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,尖嘴管有液体呈喷泉状喷出,最终几乎充满烧瓶,下列情况满足题意的是________.
①NH3-H2O
②HCl-H2O
③CO2-4 mol/L NaOH溶液
④Cl2-饱和NaCl水溶液
⑤HCl-AgNO3溶液
⑥Cl2-淀粉碘化钾溶液
⑦Cl2-溴化钠溶液
⑧NH3-汽油
⑨NO2-H2O
⑩NH3-酚酞溶液
(2)500 mL烧瓶中充满某种气体(273 K、101325 Pa)X,烧杯中盛满水,L=30 cm,h=6 cm,气体溶解度在此状况下为1∶40.通过计算回答:如果能看到喷泉,开始时胶头滴管应先向烧瓶内注入水的体积是________mL.
(3)某学生利用氨和水做喷泉实验,(氨为该学生制备和收集),结果未能形成喷泉,请你替他分析实验不成功的可能原因?
(4)①在图乙的锥形瓶中,分别加入足量的下列物质,反应可能产生喷泉的是________
A.CaCO3和稀H2SO4
B.NH4HCO3和稀盐酸
C.Al和浓硝酸
D.NaHCO3与NaOH溶液
②锥形瓶中加入酒精,水槽中加入冷水,再加入足量下列物质,结果也产生喷泉的是
A.浓硫酸
B.食盐
C.硝酸铵
D.硫酸铜
③城市中常见的人造喷泉及火山爆发的原理与上述(填图甲或图乙)装置的原理是相同的.
(5)如果只提供如图丙的装置,请说明引发喷泉的方法:________.
甲同学设计以下实验制取氧气和氧化铜。
(1)制取氧气
①用20%的![]() 溶液,通过反应
溶液,通过反应![]() 来制取氧气,则在下列A、B、C三装置中最佳装置是_____
来制取氧气,则在下列A、B、C三装置中最佳装置是_____

②与气体发生装置相连接的D装置的导管口是_____
③为了能使产生的氧气被充分干燥,可采取的操作是
(2)制取氧化铜
将m g铜粉在氧气流中加热到高温,使铜粉全部氧化,得n g粉末X。乙同学查阅资料知: 铜与氧气的反应有:①![]() ,②
,②![]() ;在酸性条件下:
;在酸性条件下:![]() 。由此得出结论:铜虽然全部氧化,但由于加热温度偏高,产物不一定是纯CuO,可能含有一定量的氧化亚铜(
。由此得出结论:铜虽然全部氧化,但由于加热温度偏高,产物不一定是纯CuO,可能含有一定量的氧化亚铜(![]() )。
)。
(3)探究铜的氧化物的成分
为测定粉末X中是否含有![]() ,甲、乙、丙三同学分别设计如下实验方案。
,甲、乙、丙三同学分别设计如下实验方案。
甲同学的实验方案是:向粉末X中加入稀硫酸,若有___ ,则说明固体中含有![]() 。
。
乙同学的实验方案是:再将粉末X放人氧气中加热,如果其质量增加,则说明其中含有![]() 。
。
丙同学的实验方案是:通过分析实验数据就可以确定粉末X的成分。若n的取值范围是![]() ,则粉末X中含有
,则粉末X中含有![]() ,其物质的量是_____。
,其物质的量是_____。
请你再设计一个与上述三个实验方案中现象均不相同的实验方案,通过对化学反应和对实验现象的分析来确定粉末X中是否含有![]() 。写出该实验中反应的离子方程式。
。写出该实验中反应的离子方程式。
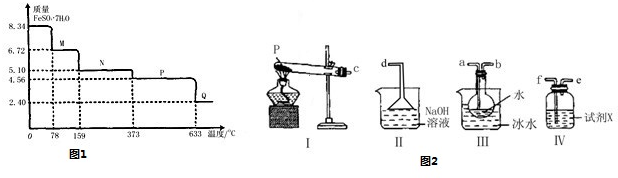
硫酸铜是一种用途广泛的化工原料.将适量稀硝酸分多次加人到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶,得到硫酸铜晶体(装置如图所示).

(1)图中烧瓶内发生的离子反应方程式为:________.
(2)反应时B瓶内的现象是________________.
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
把Fe2(SO4)3作催化剂加人到铜粉与稀硫酸的混合物中,并通人空气或氧气,即发生反应.反应完全后向其中加人物质甲调节pH,产生Fe(OH)3沉淀,过滤、蒸发、结晶,得到硫酸铜晶体,滤渣作催化剂循环使用.
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
请回答下列问题:
①物质甲是________(填字母序号).
a.NH3·H2O
b.CuCO3 c.NaOH d.CuO②该方案中调节
PH的范围是________.第二组:过氧化氢氧化法
将铜丝放到稀硫酸中,加入10%的H2O2,微热.充分反应后,经过滤、蒸发结晶、抽滤等操作,用少量95%的酒精淋洗后晾干,得到硫酸铜晶体.

请回答下列问题:
③加热时温度不宜过高的原因是________________,晶体采用酒精淋洗的优点是________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com