天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH
4(g)+2O
2(g)=CO
2(g)+2H
2O(l)△H=-889.6kJ/mol.
(1)反应物能量总和
(填“大于”、“小于”或“等于”)生成物能量总和.
(2)若1mol甲烷完全燃烧生成二氧化碳和水蒸气,则放出的热量
889.6kJ.(填“>”、“<”或“=”)
(3)已知氢气燃烧生成液态水的热化学方程式是:2H
2(g)+O
2(g)=2H
2O(l)△H=-572kJ/mol,则相同质量的甲烷和氢气,完全燃烧生成液态水,放热较多的是
.
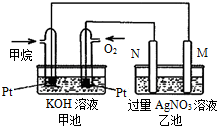
(4)如图所示的甲池装置是由CH
4、O
2和KOH溶液组成的新型燃料电池,利用该装置可以将
能转化为
能.
(5)乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
(6)M电极的材料是
,N的电极电极反应式为:
;乙池的总反应式是
,通入甲烷的铂电极上发生的电极反应式为
.
(7)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为
L(标准状况下);若此时乙池溶液的体积为400mL,则乙池中溶液的H
+的浓度为
.

 天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.
天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.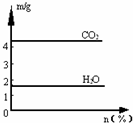 将气体甲通入液体乙中得一混合液,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
将气体甲通入液体乙中得一混合液,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( ) 分别回答下列问题.
分别回答下列问题. 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: