
题目列表(包括答案和解析)
15.下列说法中,正确的是 ( )
A.从伦琴射线管对阴极发出X射线时,对阴极中的原子和原子核的结构并没有改变,
只是原子从较高能级跃迁到了较低的能级
B.用升温、加压的方法和化学的方法都不能改变原子核衰变的半衰期
C.由两种元素的原子核结合成一种新元素的原子核时,可能放出能量,也可能吸收能量
D.在核反应过程的前后原子核的质量数守恒,质量也守恒
14.下列有关热现象的叙述中正确的是 ( )
A.物体内所有分子的热运动动能的总和就是物体的内能
B.对于同一种气体,温度越高,分子平均动能越大
C.物体的内能增加,一定要从外界吸收热量
D.一定质量的气体,温度升高时,体积可能不变
13、生活里的化学反应可用离子方程式来表示,以下书写正确的是
 A. 用氯气作为水的消毒剂:Cl2+H2O 2H++Cl-+ClO-
A. 用氯气作为水的消毒剂:Cl2+H2O 2H++Cl-+ClO-
B. 倒一些食醋清除热水瓶胆里的水垢:2H++CaCO3=Ca2++H2O+CO2↑
C. 胃药里含氢氧化铝能降低胃酸的酸度:Al(OH)3+3H+=Al3++3H2O
 D.纯碱用于清洁厨具是由于它溶于水呈碱性的缘故:HCO3-+H2O OH-+H2CO3
D.纯碱用于清洁厨具是由于它溶于水呈碱性的缘故:HCO3-+H2O OH-+H2CO3
12、相同温度下,取2aL醋酸和aL盐酸分别与bL物质的量浓度为cmol/L的NaOH溶液混合,都恰好完全中和,则下列说法中正确的是
A. 完全中和后两溶液的pH相等
B. 盐酸和醋酸所含的阴离子的物质的量相等
C. 盐酸物质的量浓度是醋酸物质的量浓度的2倍
D. 盐酸中由水电离出来的c(H+)比醋酸溶液中水电离出来的c(H+)大
11、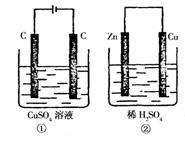 如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol·L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是
如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol·L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是
A.产生气体的体积:①>②
B.电极上析出物质的质量:①>②
C.溶液的pH变化:①增大,②减小
D.电极反应式:①中阳极 4OH--4e-=2H2O+O2↑;
②中负极:2H++2e-=H2↑
10、对于平衡体系mA(g)+nB(g)
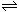 pC(g)+qD(g);△H<0。下列结论中正确的是
pC(g)+qD(g);△H<0。下列结论中正确的是
A.若平衡时A、B的转化率之比为m:n(m、n不相等),说明反应开始时,A、B的物质的量之比为m:n
B.若其它条件不变,将容器的体积增大1倍,此时A的浓度变为原来的0.48倍,则m+n>p+q
C.若m+n=p+q,则往含有a mol气体的平衡体系中再加入b mol B,达到新平衡时,气体的总物质的量等于(a+b)mol
D.若升高温度时,平衡混合气体的平均相对分子质量增大,则m+n>p+q
9、下列各组物质间反应,水既不做氧化剂又不做还原剂的氧化还原反应是:①F2和H2O ②Na和H2O ③Na2O2和H2O ④CaO和H2O ⑤Na2O和H2O ⑥Cl2和H2O ⑦NO2和H2O
A.③④⑤⑥⑦ B.①⑤⑦ C.②③⑤ D.③⑥⑦
8、下列叙述正确的是(NA为阿佛加德罗常数)
A.、15.6g Na2O2中含有的阴离子的数目为0.4NA
B.、7、1g氯气与氢氧化钠反应时,转移电子数为0.2NA个
C.、11.2升的HCl气体溶于水,制成1升盐酸溶液,其浓度为0.5mol/L
D、0℃、2.02×l05帕时,1molCO2的质量为44g
7、X、Y是元素周期表中ⅦA族中的两种元素。下列叙述中能说明X的非金属性比Y强的是
A. X原子的电子层数比Y原子的电子层数多
B. X的氢化物的沸点比Y的氢化物的沸点低
C. Y的单质能将X从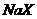 的溶液中置换出来
的溶液中置换出来
D. X的气态氢化物比Y的氢化物稳定
6.2002年由德、法、美及波兰等多国科学家组成的科研小组合成了非常罕见的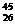 Fe原子,有关
Fe原子,有关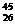 Fe的说法正确的是
Fe的说法正确的是
A.它是一种新元素 B.它是一种新核素
C.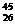 Fe 与
Fe 与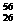 Fe互为同素异形体 D.这种铁原子发生衰变放出两个质子后变成
Fe互为同素异形体 D.这种铁原子发生衰变放出两个质子后变成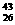 Fe
Fe
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com