
题目列表(包括答案和解析)
3.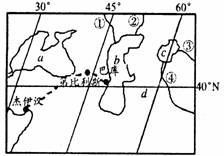 关于图中相关地理事物的叙述正确的是
关于图中相关地理事物的叙述正确的是
A.①②③④四条河都为内流河,最长的是②河
B.a,b,c三个水域都为国际水域,都属于咸水湖
C.杰伊汉所在地区的自然带为常绿阔叶林带
D.d地区气候干旱,为世界著名的大沙漠之一
2.此时我们教室里的钟表指示的时间是
A.11时 B.12时 C.13时 D.14时
在美国的推动下,把里海地区的石油直接运往地中海的里海石油管道,即巴库(阿塞拜疆)--第比利斯(格鲁吉亚)--杰伊汉(土耳其)石油管道,于7月13日正式开通启用。回答3-4题。
1.如果非阴影部分的日期是11月30日。
则阴影部分的日期是
A.11月29日 B.11月29日或12月1日
C.12月1日 D.无法确定
31.(20分)
小家鼠的毛色的黄与灰为一对相对性状,由等位基因B、b控制;尾形的弯曲与正常为另一对相对性状,由等位基因T、t控制。在毛色遗传中,具有某种纯合基因型的合子 不能完成胚胎发育。让毛色、尾形相同的多对小家鼠交配,其中雌鼠的基因型相同,雄 鼠的基因型相同,所得子一代类型及其在子一代总数中的比例如下表。请回答:

(1)控制毛色的基因在_________染色体上,不能完成胚胎发育的合子基因型是________。
(2)小家鼠尾形性状中,显性性状是_________,控制该性状的基因在_________染色体上。
(3)亲代雌鼠、雄鼠的基因型分别是______、________。子一代中灰毛尾正常小家鼠的基因型是_________。
(4)若不考虑毛色性状的遗传,让子一代中全部的尾弯曲雌鼠与尾弯曲雄鼠交配,雌 鼠产生卵子的基因型是_______,其理论上的比例是_______,后代的表现型是_____,其理论上的比例是____________。
(5)选取子一代中灰毛尾弯曲的纯合雌鼠与黄毛尾正常的雄鼠,进行一代杂交实验,请预期实验结果,并用遗传图解表示。
2008年福建省普通高中毕业班质量检查
30. (22分)
(22分)
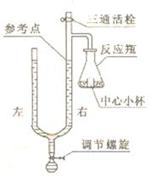
右图所示的是检测气压变化的密闭装置。反应瓶和中心小杯中放置有关实验材料和试剂,关闭活栓后,U形管右管液面高度变化反映瓶中气体体积变化。实验开始时将右管 液面高度调至参考点,实验中定时记录右管液面高度相对于参考点的变化(忽略其他原因引起的容积变化)。
Ⅰ.课题小组同学利用该装置探究某种异养型微生物的细胞呼吸方式。
(1)取甲、乙两套该密闭装置设计实验,请补充下表有关内容:
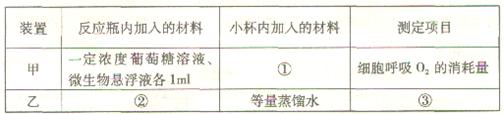
(2)将甲、乙装置均置于28℃恒温条件下进行实验(实验过程中微生物保持活性),60min后读数。请补充下表有关内容:
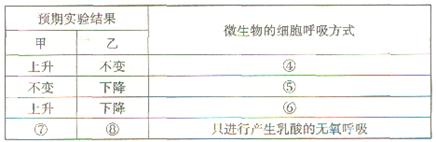
Ⅱ.除了可以测定细胞呼吸方式外,你认为用上述密闭装置和选用下列材料用具还可以 开展哪些生物学问题的探究,请写出一个课题题目。
材料用具:小麦种子、玉米幼苗、小麦幼苗、一定浓度KOH溶液、NaHCO3稀溶液、蒸馏水、一定浓度葡萄糖溶液、恒温装置、暗箱。
课题题目:____________________________。
29.(16分)
苯乙烯(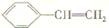 )与A、B、C、D、E、F、G、H、I等有机化合物之间存在如下图所示转化关系。
)与A、B、C、D、E、F、G、H、I等有机化合物之间存在如下图所示转化关系。
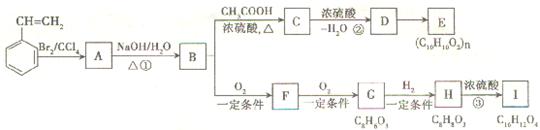
请回答下列问题:
(1)反应①、②的反应类型分别是__________、________________。
(2)C可能的结构简式有_____________________________________。
(3)H有多种同分异构体。符合下列条件的同分异构体共有___________种。
①与FeCl3溶液发生显色反应;
②1 mol H最多能与3 mol NaOH反应;
③苯环上只有两个取代基。
其中,任意一种同分异构体的结构简式为___________________。
(4)反应③的化学方程式是_________________________________________。
(5)聚苯乙烯可用于制备高频绝缘材料。由苯乙烯合成这种高聚物的化学方程式为
_______________________________________________________。
28.(18分)
某研究性学习小组欲测定某绿色粉末Cu2(OH)2CO3·xH2O中的x值,并进行相关实验探究。
已知:Cu2(OH)2CO3·xH2O固体在加热条件下发生反应:
Cu2(OH)2CO3·xH2O 2CuO +CO2↑+(x+1)H2O
2CuO +CO2↑+(x+1)H2O
(Mr[Cu2(OH)2CO3]=222;Mr(CuO)=80;Mr(CO2)=44;Mr(H2O)=18)
[实验一]测定Cu2(OH)2CO3·xH2O中的x值。
(1)准确称取m1 g该粉末样品,置于坩埚中,用酒精灯缓慢加热至完全分解,冷却,称得剩余固体的质量为m2 g 。加热粉末时,除了坩埚、坩埚钳、三角架、玻璃棒、酒精灯外,还要用到的仪器是____________,操作中需用玻璃棒轻轻搅拌固体,目的是________
____________________________________________________________________________。
所测得的x值为______________(用含m1、m2的代数式表示)。
(2)下列是甲、乙两位同学对实验过程中绿色粉末是否已完全分解的判断依据。
甲:观察到粉末变成黑色,不再有水蒸气逸出。
乙:重复加热、冷却、称量,至恒重(两次称量的质量差不超过0.1g)。
你认为其中合理的是 (填“甲”或“乙”)。
(3)测定x值还有其它方法。下列是几位同学在实验设计中拟测定的数据,其中无法计算得出x值的是_____________(填序号)。
①只测定生成物CO2、CuO的质量
②只测定生成物CO2、H2O的质量
③只测定反应物Cu2(OH)2CO3·xH2O和生成物CO2的质量
④只测定反应物Cu2(OH)2CO3·xH2O和生成物H2O的质量
[实验二]利用上述反应的分解产物氧化铜氧化乙醇制备乙醛(沸点为20.8℃)。
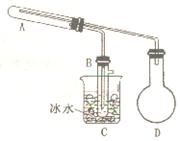 (1)用如右图所示装置(图中夹持装置已略去)进行实验时,需要加热的仪器是_______(填标号)。B装置中收集到的物质有__________________。
(1)用如右图所示装置(图中夹持装置已略去)进行实验时,需要加热的仪器是_______(填标号)。B装置中收集到的物质有__________________。
(2)能证明氧化铜氧化乙醇的实验现象是_____________,
试管A内发生反应的化学方程式为
________________________________________。
27.(14分)
中学常见物质A、B、D、E、G、M、Q之间有如下图所示变化关系(反应条件已省略):
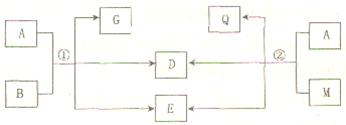
(1)若A是黑色非金属固体单质,G、Q、D是气体,E是水,D的化学式为__________。
(2)若A是红色金属,B、M是同种溶质不同浓度的溶液,G、Q是气体,且G可通过
化合反应生成Q。反应①的离子方程式是________________________________。
(3)若A是Ca(OH)2,D是极易溶于水的气体。
①工业上合成D使用铁触媒作催化剂,采用500~C左右、20MPa-50MPa为生产 条件的原因有___________(填标号)。
a.化学反应速率最大 b.催化剂的活性最大
c.反应物转化率最大 d.综合经济效益较好
上述反应中,每生成1mol D时放出热量46.2kJ,该反应的热化学方程式是:
___________________________________________________
②当1mol Ca(OH)2分别与B、M完全反应时,反应①、②生成的D的物质的量之比为2∶1,B、M的化学式分别为___________、______________。
26.(12分)
短周期元素A、B、C、D、E的原子序数依次增大,A与C、B与D分别同主族。A与E能形成化学式为AE型的共价化合物,C与D能形成化学式为C2D型的离子化合物。
(1)AE的电子式为___________________。
(2)C的单质在B的单质中燃烧,生成物中含有的化学键为______________。
(3)用惰性电极电解C2DB4的水溶液时,阳极反应式为________________________。
(4)与C同周期的某金属元素单质,溶于由A、B、C三种元素组成的化合物的水溶液
时,反应的离子方程式为__________________________。
(5)由B、C、D三种元素组成的某化合物,与稀硫酸反应并生成沉淀的化学方程式 为_____________________________________。
25.(20分)
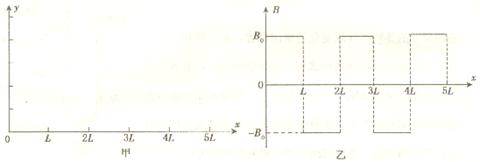
自由电子激光器是利用高速电子束射人方向交替变化的磁场,使电子在磁场中摆动着前进,进而产生激光的一种装置。在磁场中建立与磁场方向垂直的平面坐标系xoy,如图 甲所示。方向交替变化的磁场随x坐标变化的图线如图乙所示,每个磁场区域的宽度L=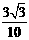 m,磁场的磁感应强度大小B0=3.75×10-4 T,规定磁场方向垂直纸面向外为正方向。现将初速度为零的电子经电压U=4.5×103V的电场加速后,从坐标原点沿x轴正方向射入磁场。电子电荷量e为1.6×10一19C,电子质量m取9×10一31kg,不计电子的重力,不考虑电子因高速运动而产生的影响。
m,磁场的磁感应强度大小B0=3.75×10-4 T,规定磁场方向垂直纸面向外为正方向。现将初速度为零的电子经电压U=4.5×103V的电场加速后,从坐标原点沿x轴正方向射入磁场。电子电荷量e为1.6×10一19C,电子质量m取9×10一31kg,不计电子的重力,不考虑电子因高速运动而产生的影响。
(1)电子从坐标原点进入磁场时的速度大小为多少?
(2)请在图甲中画出x= 0至x= 4L区域内电子在磁场中运动的轨迹,计算电子通过图 中各磁场区域边界时位置的纵坐标并在图中标出;
(3)从x= 0至x= NL (N为整数)区域内电子运动的平均速度大小为多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com