
题目列表(包括答案和解析)
33.(6分)今年春节前夕,我国北方遭遇冰雪灾害。为了清除道路上的冰雪,有关部门投入了大量工业盐融雪剂用于除冰雪。同学们从新闻中得知:①使用工业盐融雪剂后,道路两旁树木、农作物大量死亡;②桥梁路面除冰不得使用工业盐融雪剂。
[提出问题]工业盐融雪剂对树木、农作物和桥梁为什么会造成危害?
[查找资料](1)工业盐的主要成分是NaCl和NaNO2。
(2)土壤盐碱化会造成树木、农作物死亡。
[提出猜想]猜想一:工业盐溶液可能显碱性;
猜想二:工业盐溶液对钢铁可能有更强的腐蚀性。
[实验探究]同学们对猜想一和猜想二进行了探究,请你帮他们完成下列实验报告:
|
|
实验操作 |
实验现象 |
实验结论 |
|||||||||
|
猜 想 一 |
________________________________ ________________________________。 |
_______________。 |
工业盐溶液显碱性,会造成道路两旁的土壤盐碱化。 |
|||||||||
|
猜想 二 |
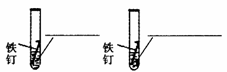
实验① 实验② (请将液体名称填在上面的横线上) |
实验①:6-7天后明显生锈。 实验②: 2-3天后明显生锈。 |
__________________ __________________ ________________。 |
[反思与应用]
对于道路除冰,请你提出更好的建议 。
32.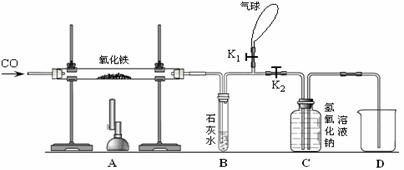 (6分)某同学为了研究炼铁的原理并测定生成铁的质量,用一氧化碳与氧化铁反应,按下图进行实验。
(6分)某同学为了研究炼铁的原理并测定生成铁的质量,用一氧化碳与氧化铁反应,按下图进行实验。
(1)首先,该同学称量氧化铁的质量,然后进行实验,他先打开K1,关闭K2,通入一氧化碳,其目的是排尽玻璃管内的空气,防止加热时因一氧化碳不纯而引起爆炸,然后关闭K1,打开K2,加热,反应一段时间后,冷却,再次称量固体的质量,发现固体质量减少了12克,则生成铁的质量为_____,玻璃管中发生反应的化学方程式为_____________________________________________。
(2)装置B中反应的化学方程式是________________________________。
(3)装置C的两个作用是________________________________________________,
(4)实验结束后,烧杯内的溶液中含有的溶质是_________________(写化学式)。
31.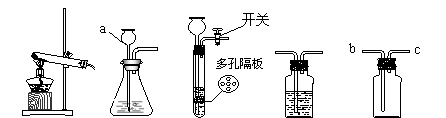 (7分) 请结合下列实验常用装置,回答有关问题。
(7分) 请结合下列实验常用装置,回答有关问题。
A B C D E
(1)写出图中标有字母的仪器名称:a_________________。
(2)若用高锰酸钾制取氧气,应选用的发生装置是__________(填装置的序号),反应的化学方程式为 。
(3)若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入___________。若要获得干燥的二氧化碳,还应选用D装置,并在该装置中盛放 (填写试剂名称)。如果用E装置收集该气体,则气体从_________端进入(填“b”或“c”)。
(4)实验室若用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其改进后的优点是 。
30.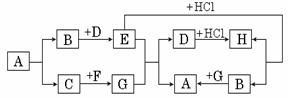 (5分)下图是初中化学所学的常见化合物之间的相互转化关系(图中“→”表示物质间存在转化关系,反应条件和生成产物中的部分物质已略去)。其中A是一种常见的建筑材料,B是一种常见的气体,H是一种含钠的化合物。请回答下列问题:
(5分)下图是初中化学所学的常见化合物之间的相互转化关系(图中“→”表示物质间存在转化关系,反应条件和生成产物中的部分物质已略去)。其中A是一种常见的建筑材料,B是一种常见的气体,H是一种含钠的化合物。请回答下列问题:
(1)写出A、F、H的化学式:A:__________;F:_________;H:___________。
(2) 写出反应的化学方程式:
① E + G :_____________________________________________;
② B + D:______________________________________________。
29.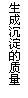
 (6分)现有HCl、NaCl、NaOH、Na2CO3等溶液。若进行下列实验,请判断可能的溶液组合。
(6分)现有HCl、NaCl、NaOH、Na2CO3等溶液。若进行下列实验,请判断可能的溶液组合。
(1)两两组合进行实验:
① 组合后无明显现象,但发生反应的组合是____________;
写出该反应的化学方程式为______________________。
② 组合后有明显现象,该现象是__________________。
反应的化学方程式为___________________________________。
(2)任意组合进行实验:
若将氢氧化钙溶液逐滴滴入组合溶液中,产生的沉淀与加入的氢氧化钙有如图所示的关系,则溶液的组合可能是 。
28.(8分)下面是初中常见化学概念之间的相互关系。
 (1)下面是部分元素的粒子结构示意图。请回答下列问题:
(1)下面是部分元素的粒子结构示意图。请回答下列问题:
镁原子中所含的质子数为 ,上述元素组成的金属单质中,活动性最强的是 。
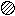
 (2)下图是表示气体分子的示意图,图中“ ”和“ ”分别表示两种不同的原子,其中表示化合物的是 ,表示混合物是 ,表示单质的是 ,
(2)下图是表示气体分子的示意图,图中“ ”和“ ”分别表示两种不同的原子,其中表示化合物的是 ,表示混合物是 ,表示单质的是 ,
(3)印刷铜制电路板的“腐蚀液”为FeCl3溶液。已知铜、铁均能与FeCl3溶液反应,反应方程式分别为:Cu+2FeCl3=2FeCl2+CuCl2,Fe+2FeCl3=3FeCl2。现将一包铜、铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,则烧杯溶液中一定含有的溶质是__________,烧杯中一定含有的固体是 。
27.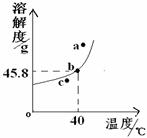 (6分)请运用溶液的知识回答下列问题。
(6分)请运用溶液的知识回答下列问题。
(1)右图是40℃时氯化铵的溶解度曲线。40℃时,
氯化铵的溶解度是___________。从该曲线可
以看出,氯化铵的溶解度随温度升高而_______。
(2)氯化铵属于化学肥料中的 (填序号)。
A.钾肥 B.氮肥 C.磷肥
(3)该图中a、b、c三点能表示氯化铵溶液处于不饱和状态的是 。在不饱和氯化铵溶液变为饱和溶液的过程中,下列描述正确的是 。
A.溶质的质量一定变小 B.溶剂的质量一定变小
C.溶液的质量一定变大 D.溶质质量分数可能不变
(4)室温下,将一瓶氯化铵溶液敞口放置一段时间,溶质质量分数由10%变成25%,放置前后溶剂的质量比 。
26.(5分)芝麻酱是常见的调味品之一。其主要成分如下图所示:

(1)图中未标出的营养素是 ,其中的“钙、铁”是指 (填“元素”、“单质”或“化合物”)。芝麻酱所含的营养素中,能提供能量的是 (写出一种即可)。
(2)芝麻酱中钙、铁、蛋白质含量较高。人们食用芝麻酱可以防治 (填序号)。
A.佝偻病 B.缺铁性贫血 C.骨质疏松 D.坏血病
(3)正常情况下,每人每日摄入的油脂不超过50 g。由此计算,食用此芝麻酱每日最多不应超过 g。
25.下列除杂质的方法不正确的是
|
选项 |
物质(括号内为杂质) |
除杂方法 |
|
A |
N2(O2) |
通过灼热的铜网 |
|
B |
NaOH溶液(Na2CO3) |
加入适量的Ca(OH)2溶液,再过滤 |
|
C |
CO(水蒸气) |
通过浓硫酸 |
|
D |
Fe(Fe2O3) |
加入过量稀盐酸,再过滤 |
24. 物质X可发生下列所示的两个反应, ①X+酸→盐+水 ;②X+水→碱;则X可能是
A.CaO B.Na2CO3 C.CO2 D.NaOH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com