
题目列表(包括答案和解析)
2.实验室里制取气体的装置包括___________和_________两部分。确定气体的发生装置应考虑的因素是_________和_________,确定气体的收集装置应考虑的因素是气体的_________和_________等。
思路解析:本题考查实验室制备气体时装置的选择原则和气体收集时需要考虑的主要因素。
答案:发生装置 收集装置 反应物的状态 反应条件 密度 水溶性
1.实验室里制取CO2的药品是_________,化学反应方程式为___________________________;收集CO2的方法是___________________________;检验CO2的方法是_________________;验满CO2的方法是______________________________________________________
思路解析:本题考查实验室制取二氧化碳的反应原理和收集、检验、验满二氧化碳的方法和过程,考查对该实验基本知识的掌握。
答案:大理石或石灰石与稀盐酸CaCO3+2HCl====CaCl2+ CO2↑+H2O向上排空气法将产生的气体通入澄清的石灰水中,澄清的石灰水变浑浊,则证明产生的气体是二氧化碳将燃着的木条放到集气瓶,若木条熄灭,则证明已满
6.2 二氧化碳制取的研究
中考资源网 一、选择题
中考资源网 1.实验室制二氧化碳常用的方法是 中考资源网 ( )
中考资源网 A.煅烧石灰石 B.石灰石和稀盐酸反应 C.燃烧木炭 D.大理石和稀硫酸反应
中考资源网 2.检验二氧化碳是否充满集气瓶的正确方法是 ( )
中考资源网 A.将澄清石灰水倒入集气瓶内振荡 B.将点燃的木条伸入集气瓶内
中考资源网 C.将点燃的木条放在集气瓶口 D.将带火星的木条接近集气瓶口
中考资源网 3.下列装置能用来收集二氧化碳气体的是 ( )
中考资源网 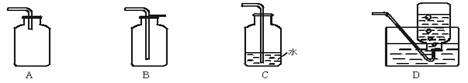
中考资源网
中考资源网
中考资源网 4.实验室用石灰石和稀盐酸反应制取二氧化碳而不能用硫酸的原因是 ( )
中考资源网 A.这两种物质间不能反应
中考资源网 B.反应太剧烈来不及收集
中考资源网 C.因为硫酸易挥发,因而产生的气体中混有杂质
中考资源网 D.生成了微溶性物质覆盖在石灰石表面,阻止了反应的进一步进行
中考资源网 5.实验室制二氧化碳时无需用到的仪器是 ( )
中考资源网 A.集气瓶 B.水槽 C.导气管 D.长颈漏斗
中考资源网 6.下列粒子中,能保持二氧化碳化学性质的是 ( )
中考资源网 A.碳原子 B.二氧化碳分子 C.氧原子 D.碳原子和氧原子
中考资源网 7.下列气体只能用向上排空气法收集的是 ( )
中考资源网 A.H2 B.O2 C.CO2 D.O2和CO2
中考资源网 8.鉴别H2、O2、CO2三种气体的方法是 ( )
中考资源网 A.三种气体分别通过灼热的氧化铜
中考资源网 B.将三种气体分别通过灼热的铜网
中考资源网 C.将少量澄清的石灰水倒入集气瓶中、振荡
中考资源网 D.将燃着的木条分别伸入三种气体中
中考资源网 9.实验室里制取二氧化碳气体的主要操作步骤是 ①收集气体 ②检查装置的气密性③按要求装配好仪器 ④向漏斗里注入酸液⑤将固体药品加入到锥形瓶中。下列操作顺序正确的是 ( )
中考资源网 A.③②⑤④① B.③②④⑤① C.②③⑤④① D.③⑤④②①
中考资源网 10.两份质量相等的碳酸钙,一份充分煅烧,另一份与足量稀盐酸充分反应,两种方法得到二氧化碳的质量 ( )
中考资源网 A.一样多 B.跟稀盐酸反应得到的多 C.煅烧后得到的多 D.无法判断
中考资源网 二、填空题
中考资源网 1.实验室常用_______和________反应制CO2,化学方程式为_______________________,集满二氧化碳气体的集气瓶要用 盖好,瓶口向 放在桌上备用。
中考资源网 2.现在有下列实验仪器:(1)大试管(2)烧杯(3)酒精灯(4)集气瓶(5)长颈漏斗(6)
中考资源网 带导管的双孔塞(7)导气管(8)玻璃片(9)铁架台(10)水槽等仪器,在实验制取CO2
中考资源网 时,应选用的仪器有(填序号) 。
中考资源网 3.回顾制取O2、CO2等气体的实验,我们整理出实验室制取气体的一般思路:若要制取某种气体,
中考资源网 (1)首先研究生成气体的 。
中考资源网 (2)然后根据 和 选择并安装实验仪器设备,而且一定要检查 。
中考资源网 (3)根据 确定气体的收集方法。
中考资源网 4.将洗净的鸡蛋壳(主要成分是CaCO3)放在一个玻璃杯中,往杯中加入少量稀盐酸,用蘸有澄清石灰水的玻璃片盖住杯口,可观察到的现象是
中考资源网 (1) ;(2) 。
中考资源网 5.文文同学收集了一些家庭装修时废弃的大理石碎片,并设计了如下图的装置来制取二氧化碳(该装置能随时控制反应的发生)。请回答问题:
中考资源网 
中考资源网 (1)大理石应放在_______中,装置A中反应的化学方程式为________ ____。
中考资源网 (2)用装置B收集CO2,验满时应把燃着的木条放在_________(选填字母)处。
中考资源网 6.如图所示,锥形瓶内有一支试管,试管内盛有足量的稀盐酸,锥形瓶
中考资源网 底部盛有足量碳酸钙,气球紧紧绑在玻璃导管上(本装置气密性很好)。
中考资源网 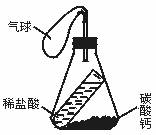 将此装置放在托盘天平左盘上,调节天平平衡后,取下此装置并将其倾
将此装置放在托盘天平左盘上,调节天平平衡后,取下此装置并将其倾
中考资源网 斜,使试管内的稀盐酸流入锥形瓶底部。过一会儿,观察到的现象是__
中考资源网 ___________________。再将此装置放回天平左盘上,天平指针_______
中考资源网 ___ __(填“偏左”或“偏右”或“不偏”),其原因是_______________
中考资源网 ____ _____。
中考资源网 7.根据下图所示实验装置回答下列问题:
中考资源网 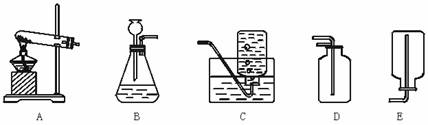
中考资源网 ①用加热固体的方法产生气体,应选发生装置 (填序号,下同),收集难溶性气体应选 。
中考资源网 ②B装置中长颈漏斗末端应伸至液面以下,可以防止 。伸进D,E中的导管均应接近集气瓶底部是为了 。
中考资源网 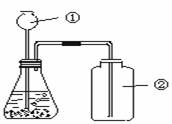 三、实验题
三、实验题
中考资源网 1.下图是实验室制取二氧化碳的装置图,回答下列问题:
中考资源网 (1)写出有标号的仪器的名称:
中考资源网 ①___________________②___________________。
中考资源网 (2)气体发生装置内的药品是_______和_______
中考资源网 (3)制备二氧化碳的化学方程式为:_________________
中考资源网 (4)用向上排空气法收集二氧化碳的原因是______________________________
中考资源网 (5)收集二氧化碳_____(填“能”或“不能”)用排水法,其原因是_____________________。
中考资源网 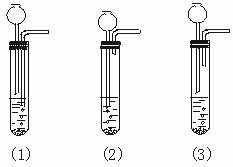 2.有人设计了实验室制取二氧化碳的简易装置(如下图)哪种是正确的?哪种是错误的?为什么?
2.有人设计了实验室制取二氧化碳的简易装置(如下图)哪种是正确的?哪种是错误的?为什么?
中考资源网
中考资源网
中考资源网
中考资源网
中考资源网
中考资源网 四、计算题
中考资源网 1.将200 g石灰石与足量的盐酸反应,共收集二氧化碳66 g。
中考资源网 求:(1)该石灰石中CaCO3的质量分数多少?
中考资源网 (2)这些二氧化碳用多少木炭充分燃烧可制得?
中考资源网
中考资源网
中考资源网
中考资源网 2.某石灰石样品中含有80%的碳酸钙。假若取100 g这样的石灰石与足量的盐酸完全反应,可生成多少g CO2?
中考资源网
中考资源网
中考资源网
中考资源网 4.高炉炼铁的原理是用CO还原铁矿石(主要成分是Fe2O3)。
中考资源网 (1)写出CO还原Fe2O3的化学方程式。
中考资源网 (2)计算冶炼1 t铁(其中含杂质5%),需要多少t铁矿石(假定铁矿石中含Fe2O3 80%)。
中考资源网
中考资源网
中考资源网
中考资源网
中考资源网
中考资源网
中考资源网
8.早在17世纪,质量守恒定律发现之前,英国化学家波义耳曾经做过一个实验:在密闭的容器中燃烧金属时,得到了金属灰,然后打开容器盖,称量金属灰的质量,发现比原来金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律。
解答:(1)金属燃烧是金属和氧气发生化合反应,生成金属氧化物。根据质量守恒定律可知,参加反应的金属与氧气的质量之和等于生成的金属氧化物的质量。生成的金属灰是金属氧化物,所以金属灰的质量比原来金属的质量增加了。
(2)分别称量反应前后密闭容器的质量。
13.6克÷85%=16克
答案:(1)12.5 (2)16
0.8x 6.4克 y
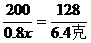 ,x=12.5克
,x=12.5克
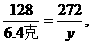 y=13.6克
y=13.6克
7.火力发电厂用石灰石泥浆吸收废气中的二氧化硫以防止污染环境,其反应方程式为:2CaCO3(粉末) + 2SO2+ O2====2CaSO4+ 2CO2。
(1)若100克废气中含6.4克二氧化硫,则处理100克这种废气需含碳酸钙(CaCO3)的石灰石__________克。
(2)处理上述100克废气,可得到含CaSO4 85%的粗产品_________克。
思路解析:题中给出的化学方程式,即为计算的依据。
设需含CaCO3 80%的石灰石的质量为x,生成纯CaSO4的质量为y。
2CaCO3+2SO2+O2====2CaSO4+2CO2
200 128 272
36.5×10% x
x=4 g
污水中所含NaOH的质量分数为: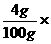 100%=4%。
100%=4%。
答案:(1)4 g(2)4%
36.5 40
6.(2010福建福州中考,30)某综合实践活动小组同学,对我市某化工厂排放的污水进行检测,发现主要的污染物为氢氧化钠。为测定污水中氢氧化钠的含量,取100 g污水于烧杯中,加入36.5 g质量分数为10%的稀盐酸恰好完全反应。(假设污水中其他成分不与稀盐酸反应,反应的化学方程式为:HCl+NaOH====NaCl+H2O)
求:(1)100 g污水中含氢氧化钠多少克?
(2)污水中所含氢氧化钠的质量分数。
思路解析:设100 g污水中含NaOH质量为x。
HCl+NaOH====NaCl+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com