
题目列表(包括答案和解析)
28、取一定量的碳酸钠、碳酸氢钠和硫酸钠的固体混合物与250mL、1.00mol/L的盐酸(过量)反应,得到标准状况下的CO2气体2.016L,然后加入500mL、0.1mol/L的氢氧化钡溶液,得到沉淀2.33克,溶液中过量的碱用10.0mL、1.00mol/L的盐酸恰好中和。通过计算求混合物中各物质的质量。
答案:1.B 2.B 3.D 4.A 5.C 6.C 7.B 8.C 9.C 10.C 11.C 12.B 13.D 14.C 15.A 16.A 17.B 18.D 19.B 20.D 21.C 22.D
27、某课外兴趣小组利用右图所示的装置进行HNO3、NO2、NO联合性质实验,其过程如下:
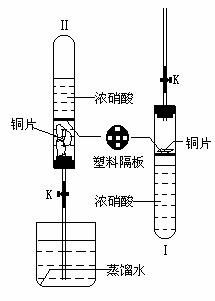 先在如图Ⅰ所示的装置中加入一定量的浓硝酸,在试管上部放上一片塑料隔板,在隔板上放上几片铜片(此时铜片与浓硝酸不接触),然后塞上带导气管的塞子,最后按图Ⅱ所示将它倒过来使铜和浓硝酸接触,并使导气管下端深入到蒸馏水中,然后打开夹子K。
先在如图Ⅰ所示的装置中加入一定量的浓硝酸,在试管上部放上一片塑料隔板,在隔板上放上几片铜片(此时铜片与浓硝酸不接触),然后塞上带导气管的塞子,最后按图Ⅱ所示将它倒过来使铜和浓硝酸接触,并使导气管下端深入到蒸馏水中,然后打开夹子K。
在实验过程中装置图Ⅱ中出现了如下的实验现象:
(1)铜片在塞子和塑料隔板之间翻滚并剧烈反应,产生了在量的红棕色气体集中在试管的上部空间,试管中的浓硝酸被逐渐压入下面烧杯中,到最后试管中只剩下几片未反应完的铜片和大量的红棕色的气体,且试管外壁非常烫。
(2)关闭K,让试管在空气中自然冷却,待冷却到室温时打开K,此时烧杯中的液体立刻涌入到试管中,试管中的红棕色气体颜色逐渐变为无色,仔细观察还可以看到前面剩余的铜片又开始与涌入试管中的液体发生缓慢的反应,产生一种无色的气体,经过相当长的时间后,试管中的液体又被压回烧杯中,而试管中充满了无色的气体。
根据你所学的知识对实验过程中产生的现象做出相应的解释:
(1)写出铜和浓硝酸反应的化学反应方程式,并根据现象(1)判断该反应是一个吸热反应还是放热反应。
(2)解释现象(2)中出现的打开K时烧杯中的液体立刻涌入到试管中中原因:
(3)用化学反应方程式解释现象(2)中剩余的铜片又开始与涌入试管中的液体发生缓慢的反应,产生一种无色的气体:
(4)若将实验后的试管在空气中打开,你认为将出现的实验现象是: 原因是:
(5)取反应后的烧杯中的液体3mL,并加入2mL、6mol/L的盐酸,最后加入足量的铜粉,写出对应的离子反应方程式:
25、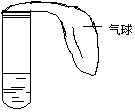 某学生课外活动小组利用右图所示装置分别做如下实验:
某学生课外活动小组利用右图所示装置分别做如下实验:
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________________溶液;加热时溶液由红色逐渐变浅的原因是: ___________________________________________________。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是_______溶液;加热时溶液由无色变为红色的原因是: ___________________________ 。
24、已知:①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z。元素Y、X、Z的原子序数依次递增。②X在A、B、C、D中都不呈现它的最高化合价。③室温下气态单质A与某种常见一元强碱溶液反应,可得到B和C。④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是 ,Z是 ,Y的电子式为:
(2)写出③中反应的化学方程式: 。
(3)写出④中反应的化学方程式: 。
23、已知短周期的四种元素A、B、C、D形成的四种离子:A+、B2+、C-、D2-电子层结构相同,则四种元素的原子半径按小到大的顺序排列为_____________四种元素的原子序数按由大到小的顺序排列为___________________。
22、已知Cu(NO3)2受热分解的化学反应方程式为: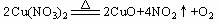
某人将少量的Cu(NO3)2固体放入试管中加热,然后用带火星的木条放入试管中,木条复燃,则下列说法正确的是:
A、NO2能支持燃烧 B、NO2不能支持燃烧
C、木条复燃是因为硝酸铜分解产生了氧气的缘故
D、木条复燃是因为硝酸铜分解产生了氧气和二氧化氮共同作用的结果
21、强热绿矾晶体发生如下反应:2FeSO4·7H2O==Fe2O3+SO3+SO2+14H2O。若将反应生成的气体物质全部通入到BaCl2溶液中去,则会:①有BaSO4白色沉淀生成②有BaSO3白色沉淀生成③有SO2气体逸出④有SO3气体逸出,其中正确的有:
A、①④ B、②④ C、①③ D、②③
20、有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式为:( ) A、I2O4 B、I2O5 C、I4O7 D、I4O9
19、在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温、同压下相同体积的氧气时,三个反应中转移的电子数之比为: A 1︰1︰1 B 2︰2︰1 C 2︰3︰1 D 4︰3︰2
18、某金属单质与一定量的稀硝酸反应,得到对应硝酸盐和NO和水,已知反应中消耗的金属单质与硝酸的物质的量之比为1:3,则该金属元素可能为: A、Cu B、Ag C、Al D、Fe
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com