
题目列表(包括答案和解析)
27、(3分)
26、(7分)(1) (2) (3)
25、(8分)(1)A B C D (2) (3)
24、(5分)(1) (2) (3) (4) (5)
23、(3分)
30、(8分)有Na2SO4和Na2CO3 混合液10.0mL,加入足量的BaCl2溶液,充分反应后,经过滤、洗涤、烘干,得到白色沉淀1.45g。将沉淀与过量的盐酸反应,得到112mL(标准状况)CO2 气体,(1)写出有关化学方程式
(2)求原混合溶液中Na2SO4 和Na2CO3 的物质的量浓度。
第二学期期末考试
高 一 化 学 答 卷 纸
29、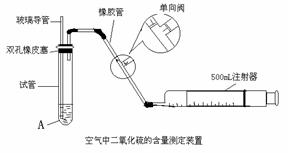 (9分)SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如下实验装置:
(9分)SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如下实验装置:
(1)检查该装置的气密性时,先在试管中装入适量的水(保证玻璃导管的下端没在水中),然后 (填写操作方法)时,如看到 (填写实验现象),则证明该装置的气密性良好。
(2)向试管中加入0.00005mol/L的碘水10mL,用适量的蒸馏水稀释后再加入2~3滴淀粉溶液配制成溶液A。测定指定地点的空气中的SO2的含量时,推拉注射器的活塞反复抽气,A溶液由色 变为 色时反应恰好完全进行,此时停止抽气,该反应的化学方程式为 。
(3)我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3)为一级标准0.15,二级标准0.50,三级标准0.70。该学生课外活动小组在某一地点测量空气中SO2的含量,当反应恰好完全时,记录抽气次数为120次(假设每次抽气500mL)。则试通过计算确定该地点的空气中SO2的含量为 ,属于 级标准。
28、(9分)下图是实验室制SO2并验证SO2某些性质的装置图,试回答:
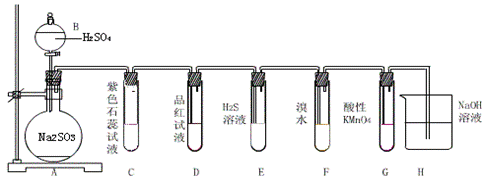

(1)⑥中发生的化学反应方程式为____________________________________________。
(2)①中实验现象为______________证明______________________________________。
(3)②中品红溶液_________,证明SO2有___________。
(4)③中现象是_____________,证明SO2有___________性。
(5)④中现象是_____________,证明SO2有___________性。
27、(3分)抽取某地酸雨水样进行检验,测得各离子的浓度分别是:[Na+]=2.3×10-5 mol/L [Cl-]=3.5×10-5mol/L [NH4+]=7.0×10-6mol/L [SO42-]=2.5×10-6mol/L 则该酸雨中[H+]=________。
26、(7分)有一包白色固体,可能含有NaCl、Na2SO4、CaCl2、CuSO4、Na2CO3 和CaCO3 ,将固体放入水中,经搅拌后变为无色溶液,在溶液里加入BaCl2 溶液,产生白色沉淀,再加入盐酸,沉淀全部消失并有气体放出,由此推断: (1)原固体肯定有_____________________________, (2)原固体肯定不存在______________________________________。 (3)______________不能确定存在与否,要确定其存在,应进行的实验是___________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com