
题目列表(包括答案和解析)
21。
(04年北京理综)在一定温度下,一定体积的密闭容器中有如下平衡:H2(气)+I2(气) 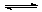 2HI(气)。 已知H2和I2的起始浓度均为0.10mol·L-1时,达平衡时HI的浓度为0.16 mol·L-1,若H2和I2的起始浓度均为0.20 mol·L-1时,则平衡时H2的浓度(mol·L-1)是
A.0.16 B.0.08 C.0.04 D.0.02
2HI(气)。 已知H2和I2的起始浓度均为0.10mol·L-1时,达平衡时HI的浓度为0.16 mol·L-1,若H2和I2的起始浓度均为0.20 mol·L-1时,则平衡时H2的浓度(mol·L-1)是
A.0.16 B.0.08 C.0.04 D.0.02
18.某元素原子的最外层只有2个电子,则该元素
(A)一定是ⅡA族元素 (B)-定是金属元素
(C)一定是正二价元素 (D)可能是金属元素,也可能不是金属元素
( )19 有a、b、c、d四种元素。a、b的阳离子与c、d的阴离子具有相同的电子层结构;a的阳离子的正电荷数小于b的阳离子的正电荷数,c的阴离子的负电荷数大于d的阴离子的负电荷数。则它们的离子半径的关系是
(A)a>b>c>d (B)b>a>d>c
(C)c>a>d>b (D)c>d>a>b
( )20,(04全国理综)某温度下在密闭容器中发生如下反应:

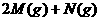 2E(g) 若开始时只充入2mol E(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2mol M和1mol N 的混合气体达平衡时M的转化率为
2E(g) 若开始时只充入2mol E(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2mol M和1mol N 的混合气体达平衡时M的转化率为
A.20% B.40% C.60% D.80%
17.为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A-D四个实验,你认为结论不正确的是
A.在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快
B.将相同大小、形状的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大
C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解
D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同
16.下列说法中不正确的是
A. 化学反应都伴随能量变化 B. 化学反应中的能量变化都表现为热量变化
C. 反应物的总能量高于生成物的总能量时,反应释放能量
D. 若化学键形成时释放的总能量大于破坏化学键所吸收的总能量,反应释放能量
15.( )下列说法正确的是
A. 在共价化合物中不可能含有离子键
B. 阴阳离子之间通过静电引力形成的化学键,叫离子键
C. 含有共价键的化合物一定是共价化合物 D. 含有离子键的化合物不一定是离子化合物
14.( )一定条件下,可逆反应2A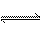 B+3C,在下列四种状态中处于平衡的是
B+3C,在下列四种状态中处于平衡的是
正反应速率 逆反应速率
A. νA=2mol/L·min νB=2mol/L·min
B. νA=2mol/L·min νC=2mol/L·min
C. νA=1mol/L·min νB=2mol/L·min
D. νA=1mol/L·min νC=1.5mol/L·min
10.( )既有离子键又有共价键的化合物是
A.Na2O B.MgCl2 C.NaOH D.NH3
( )11 当两个原子形成共价键时,原子的能量将
A、升高 B、降低 C、保持不变 D、一个升高,一个降低,但总能量不变
( ) 12 下列反应属于放热反应的是
A、铁与盐酸反应 B、C与CO2共热到高温
C、碳酸钙分解 D、八水氢氧化钡晶体与氯化铵固体反应
( )13一个原电池的总反应的离子方程式是Fe+Cu2+=Fe2++Cu,该反应的原电池的正确组成是
|
|
正极 |
负极 |
电解质溶液 |
|
A |
Fe |
Cu |
CuCl2 |
|
B |
Cu |
Zn |
H2SO4 |
|
C |
Cu |
Fe |
CuSO4 |
|
D |
Zn |
Fe |
CuCl2 |
9.( )对于A2 + 3B2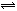 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
A、v(B2) =0.8mol/(L•s); B、v(A2) =0.4mol/(L•s);
C、v(C) =0.6mol/(L•s); D、v(B2) =4.2mol/(L•min)。
8.( )元素X的最高正价和最低负价的绝对值之差为6,Y元素的离子与X元素的离子具有相同的电子层结构,则X、Y形成的化合物可能是
A.MgF2 B.K2S C.NaCl D.KCl
7.( )短周期元素A、B、C原子序数依次递增,它们的原子的最外层电子数之和为10。A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数。下列正确的是
A.原子半径A<B<C B.A的氢化物的稳定性小于C的氢化物
C.B的氧化物的熔点比A氧化物高 D.A与C可形成离子化合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com