
题目列表(包括答案和解析)
24.(11分) 某化学兴趣小组为检验碳和浓硫酸反应生成的产物,设计如下图装置(已知SO2能使溴水褪色),请回答:

(1)指出仪器名称:甲 乙
(2)乙仪器中发生反应的化学方程式为 ;
(3)证明有二氧化碳产生的实验现象是 ;
(4)F试管中的离子反应方程式为 ;
(5)若把B玻璃管移到F试管后连接,是否可行 (填“可行”或“不可行”),理由 。
高一化学 第 (5) 页,共 8页
23.(12分)“速力菲”是一种人工合成的补铁剂,某研究性学习小组为探究其主要成分,进行了如下实验:
(1)打开这种药片的密封膜,发现其外观为淡黄色;
(2)将“速力菲”投入小试管中,加入少量蒸馏水,充分振荡后发现溶液变浑浊;慢慢加入稀硫酸后溶液变得澄清透明并显黄色;滴加KSCN溶液,立即变为血红色。学生甲由此断定“速力菲”的主要成分是三价铁盐;
(3)学生乙的操作与甲大致相同,所不同的是他动作敏捷,且在振荡前用橡皮塞塞紧试管口。结果发现:溶液仅显示淡红色。乙同学认为“速力菲”的主要成分不是三价铁盐而是亚铁盐。
(4)为了确认甲、乙的结论是否正确,学生丙将乙所得的淡红色溶液分成两份继续进行实验:
高一化学 第 (4) 页,共 8页
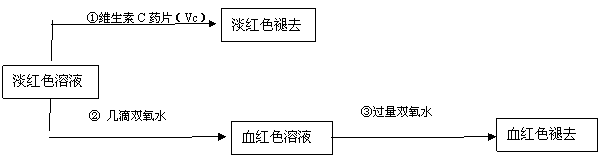
试回答下列问题:
(1)甲、乙两位同学的结论中比较合理的是 ,另一同学判断出错的原因是 。 (2)丙的实验①说明维生素C具有较强的 性(填“氧化”或“还原”)。
(3)写出与②中现象对应的离子反应方程式 。
(4)关于③中的实验现象,丙同学提出了两种假设:一种是过量的双氧水与Fe3+结合生成了某种稳定的新物质;另一种则是过量的双氧水将SCN-氧化了。请你设计一个实验方案以确认哪种假设更合理
。
(5)针对实验目的,本次实验尚未完成的任务是 。
22.(14 分)游泳池水的含氯气量应该控制
在0.5mg/L至1.0 mg /L之间,
(1)写出氯气溶于水后的化学方程式 。
溶于水中的哪种物质可杀菌消毒 。
(2)右图显示一星期中每天19时泳池中水的
氯气含量,哪几天使用泳池不安全 。
(3)你认为哪几天的天气炎热、阳光强
烈 ,说出一种理由是
。
(4)若把一片紫色的花瓣放入氯水中,可观察到
现象 。
(5)小型泳池通常使用次氯酸钠溶液而非氯气来消毒池水,试举出使用次氯酸钠溶液而非氯气的一项理由 。用化学方程式说明工业上如何生产次氯酸钠溶液 。
21.(3分)下列各化学反应中,盐酸均是反应物。利用盐酸氧化性的是(填下列选项的序号,下同) ,利用盐酸的还原性的是 :只利用盐酸的酸性的是___________。
①CaCO3+2HCl=CaCl2+H2O+CO2↑ ②Fe+2HCl=FeCl2+H2↑
③2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O

15.下列现象与胶体知识无关的是
A.日常生活中看到的云、烟、雾
B.向豆浆中加入石膏制得可口的豆腐
C.蒸发饱和食盐水析出氯化钠晶体
D.向沸水中逐滴加入饱和的FeCl3溶液,得到红褐色透明的分散系
16.下列关于物质性质的叙述中,正确的是:
A.浓硫酸具有吸水性,能使胆矾晶体由蓝变白
B.同温同物质的量浓度的Na2CO3溶液和NaHCO3溶液,前者的碱性弱
C.过量铁粉加入CuCl2溶液中,充分反应后溶液中的阳离子主要是Fe3+
D.硅是应用广泛的半导体材料,常温下易与氧气、氯气、硫酸等物质反应
17.铝合金在日常生活、建筑装潢、航空航天和汽车制造等方面均有着广泛的用途。下列关于铝合金具有广泛用途的分析不正确的是
A.铝元素在地壳中的含量高,储量丰富
B.铝容易形成致密的氧化膜,抗腐蚀性能好
C.铝化学性质稳定,常温下不与任何酸碱反应
D.铝的冶炼技术基本成熟,可以大量生产
18.正确的存放化学药品,是化学实验基本要求之一。下列物质存放错误的是
A.漂白粉长期敞口放置于广口瓶中
B.金属钠存放于煤油中
C.水玻璃盛放在带橡皮塞的试剂瓶中
D.浓硝酸存放在棕色试剂瓶中
19、下列物质既能与盐酸反应,又能与烧碱溶液反应的是
① Al2O3 ② Al(OH)3 ③ Al ④ NaHCO3 ⑤ NaHS
⑥ CaCO3 ⑦ NaHSO4 ⑧NaHSO3
A.除⑥外
B.除⑥、⑦、⑧外
C.除⑥、⑦外
D.除①、②、③、④、⑤外
20.38.4g铜跟适量的浓硝酸反应,铜全部作用后,共收集到气体22.4L(标况),则反应消耗的硝酸的物质的量是
A、1.0 mol B、1.6 mol
C、2.2 mol D、2.4 mol
高一化学 第 (3) 页,共 8页
第Ⅱ卷(非选择题,共50分)
11.NO在人体内起着多方面的重要生理作用。下列关于NO的说法错误的是
A.NO是具有刺激性气味的红棕色气体
B.NO是汽车尾气的有害成分之一
C.NO常温下遇到O2就化合成NO2
D.NO2与水反应,有NO生成
12.室温下,在强酸性溶液中能大量共存的离子组是
A.Na+、Ca2+、ClO-、Br- B.K+、Na+、CO32-、HCO3-
C.NH4+、Fe3+、Cl-、NO3- D.Ba2+、Cu2+、Cl-、SO42-
13.下列离子方程式书写正确的是
A.烧碱溶液与小苏打溶液反应:OH-+HCO3- H2O+CO2↑
B.铝粉与烧碱溶液反应:2Al+2OH-+H2O 2AlO2-+2H2↑
C.氯化亚铁溶液中滴加氯水:2Fe2++Cl2
2Fe3++2Cl-
D.氯气通入冷的氢氧化钠溶液中:2Cl2+2OH- 3Cl-+ClO-+H2O
14.NA代表阿伏加德罗常数的值,下列说法正确的是
A.5.6 g 铁在足量氯气中燃烧,电子转移0.2 NA个
B.标准状况下,2.24 L水中含有0.1 NA个水分子
C.1.12 L氯气中含有0.1 NA个氯原子
D.12 g 石墨和C60的混合固体中,含碳原子 NA个
高一化学 第 (2) 页,共 8页
10.配制100mL0.2mol·L-1NaCl溶液,不会用到下列仪器中的哪一种
A.分液漏斗 B.烧杯 C.玻璃棒 D.容量瓶
9.下列有关离子的检验方法一定正确的是
A.向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则说明原溶液中一定含Ag+
B.向某溶液中滴加KSCN溶液,若溶液出现血红色则说明原溶液中含Fe3+
C.向某溶液中滴加足量稀HCl,产生气体使澄清石灰水变浑浊,则说明原溶液中一定含CO32-
D.用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色未见紫色,说明原溶液中不含K+
8.下列有关物质用途的说法,不正确的是
A.过氧化钠可用于潜水艇的氧气来源 B.氯气可用于制农药
C.纯碱可用于治疗胃酸过多 D.钠可用于冶炼金属钛
7.将CO2气体通人CaCl2溶液,若要有白色沉淀产生,可加入的试剂是
A.氯化钾溶液 B.碳酸氢钙溶液 C.氯水 D.氢氧化钠溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com