
题目列表(包括答案和解析)
20、(9分)海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:

(1)提出提取碘的过程中有关的实验操作名称:① ③ ;
写出过程②中的有关反应的化学方程式 。
在过程②反应中的氧化剂是_______, 还原剂是_______若生成1mol的单质生成物共转移了 mol的电子。
(2)提取碘的过程中,可供选择的有机试剂有
A.四氯化碳 B.汽油 C.酒精 D.醋酸
17、卤化氢皆为 色,卤素为 价的气体,气体溶于水呈 性,其中酸性最弱的是(写化学式) ,酸性最强的是 ,卤化氢的稳定性______>______>_______>_______。(5分)
18 (16分) (1)(4分) 氯水中含有多种成分.将紫色石蕊试液滴入石蕊中,溶液显红色,起作用的成分主要是 ;过一会儿,溶液的颜色逐渐褪去,起作用的成分是 。往氯水中滴入硝酸银溶液,产生白色沉淀,起作用的成分是 。氯水能使淀粉碘化钾试纸变蓝,起作用的成分是 。(以上空白均填化学式)
(2)法医做指纹实验时,常用AgNO3溶液喷洒指纹,经过处理后会出现黑色的纹路,请用化学方程式表示其原理是:
① 。② 。(4分)
(3)(4分)已知反应 ①过氧化钠与水反应 ②氧化钠与水反应 ③钠与水反应 ④2F2 + 2H2O = 4HF + O2
根据上述反应,试填序号回答:
(1)上述反应中不属于氧化还原反应的有_________(2)水被氧化的有_______.
(3)水被还原的有_______.(4)是氧化还原反应,但水既不被氧化、又不被还原的是________.
(4) (4分) KClO3和浓盐酸在一定条件反应会生成绿黄色的易爆物二氧化氯,化学反应方程式如下:
2KClO3 + 4HCl = 2KCl + 2ClO2↑+ Cl2↑+ 2H2O⑴浓盐酸在反应中显示出来的性质是 ;
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
⑵产生0.1 mol Cl2 ,则转移的电子总数约为______________________
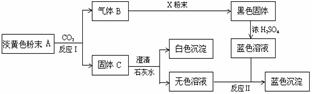 19(11分)物质有以下转化关系:
19(11分)物质有以下转化关系:
根据上图和实验现象,回答下列问题:(用化学式表示)
(1) A是 ,B是 ,C是 ,X粉末是 。
(2)确认A中阳离子的实验方法是 。
(3)写出反应Ⅰ的化学方程式 。
(4)写出反应Ⅱ的离子方程式 。
(5)若参加反应的A的质量为39g,则消耗CO2的体积(标况下)为 L,反应过程中转移电子的物质的量为 mol。
16、将标准状况下的a升氯化氢气体溶于1000克水中,得到的盐酸的密度为b克/毫升,则该盐酸的物质的量的浓度是( )
A
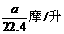 B
B 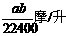 C
C 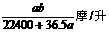 D
D 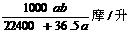
第Ⅱ卷(非选择题 共60分)
1515、使相同摩尔浓度的NaCl、MgCl2、AlCl3溶液中的Cl-离子完全沉淀时,若所用相同浓度的AgNO3溶液的体积比为3:2:1,则上述三种溶液的体积比是
(A)9:4:1 (B) 9:3:1 (C)6:3:2 (D) 3:2:1
14.某温度下,将Cl2通入氢氧化钾溶液中,反应后得到KCl、KclO、KClO3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
A. 2:3 B. 4:3 C. 10:3 D. 11:3
13.卤素从F到I性质递变规律正确的是 ( )
①单质的氧化性增加 ②单质颜色加深 ③单质沸点升高 ④气态氢化物稳定性增强
⑤气态氢化物水溶液酸性增强 ⑥离子半径逐渐增大,还原性逐渐增强
A.①③⑤ B.②④⑥ C.②③⑤⑥ D.①④⑤⑥
12.在盛有KI溶液的试管中,滴入氯水充分反应后,再加四氯化碳振荡,静置后观察到的现象是 ( )
A. 上层紫红色,下层接近无色 B. 均匀、透明、紫红色 C. 均匀、透明、无色 D. 上层接近无色,下层紫红色
11. 潮湿的氯气、新制的氯水、次氯酸钠及漂白粉的水溶液均能使有色布条褪色,是因为它们均含有( )
A. 氯气 B. 次氯酸 C. 次氯酸根 D. 氯化氢
10.氟是最活泼的非金属,能体现这个结论的是 ( )
A. 氢氟酸是弱酸 B. 氢氟酸是剧毒 C. NaF是农药 D. 氟有XeF2、KrF2等化合物
9.下列性质比较正确的是: ( )
A.热稳定性:Na2CO3 >H2CO3>NaHCO3 B.氧化性:Li+> Na+> K+>Rb+>Cs+
C.氢卤酸的酸性:HF> HCl>HBr>HI D.熔点: Cs>Rb>K>Na>Li
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com