
题目列表(包括答案和解析)
25.有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图所示:
|
|

|
白色沉淀
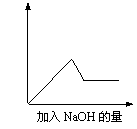 第③个实验中,生成白色沉淀的量与加入NaOH的量有右图
第③个实验中,生成白色沉淀的量与加入NaOH的量有右图
所示的相互关系。据此可知:
⑴在原溶液中一定不存在的离子有_____________________,
⑵为满足该溶液中一定存在的离子的要求,一般可溶解两
种常见物质为(写化学式)___________和_________。
⑶写出第③个实验中发生反应的离子方程式
____________________
。
24.某学生做实验:
实验一:在一个白色的点滴板的孔穴中分别故入小纸片、少量CuSO4·5H2O。然后如图所示,分别滴入几滴浓硫酸或稀硫酸,观察现象。回答下列问题:
⑴、浓硫酸滴入小纸片上,小纸片变 __________________(填实验现象),说明浓硫酸具有_____________性。
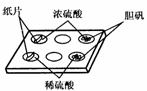 ⑵、稀硫酸滴入CuSO4·5H2O中,胆矾_______________(填实验现象);
⑵、稀硫酸滴入CuSO4·5H2O中,胆矾_______________(填实验现象);
浓硫酸滴入CuSO4·5H2O中,胆矾_____________________(填实验现象),说明浓硫酸具有_______________性。
实验二:为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
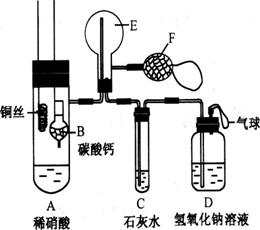
⑴、实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先赶出去其中的空气。将装CaCO3的干燥管下移与稀HNO3反应产生CO2,当看到C处有_____________现象可以确定E中空气已被赶尽:
⑵、将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为:__________________________________。
⑶、如何证明E中收集到的是NO而不是H2?
______________________________________________________
当证明出是NO后,C中白色沉淀溶解,其原因是
________________________________________________________
⑷、装置D的作用是___________________________________________________
23.已知A.B.C.D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①A+B→白色沉淀,加入稀硝酸,沉淀不溶解。
②B+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色。
③C+D→白色沉淀,继续加D溶液,白色沉淀逐渐消失。
⑴、则各是什么物质的化学式为:A 、B 、C 、D 。
⑵、现象③中所发生反应的离子方程式为:
、 。
22.今有HCl、Cl2、H2S、NH3、NO2、CO2、H2、SO2等气体,问:
⑴、形成酸雨的是____________________________;
⑵、比空气轻的气体是____________________________;
⑶、用水做溶剂,可作喷泉实验的氢化物是____________________________;
⑷、能用碱石灰干燥的是____________________________;
⑸、能使品红试液褪色的是____________________________;
⑹、可导致光化学烟雾的是____________________________。
21.用化学方程式解释下列有关实验现象:
⑴、向氨水中滴几滴酚酞试液,溶液变红色:
⑵、两只棉球分别滴有几滴浓氨水和浓盐酸放入同一只烧杯中,用表面皿盖住烧杯口,烧杯内有白烟:
⑶、一瓶无色气体打开瓶盖后,瓶口呈现出红棕色:
⑷、长期暴露在空气中的亚硫酸钠变质:
⑸、当电闪雷鸣之时,空气会发生很多化学反应,试写出与氮元素有关的化学方程式:
; ; 。
20.有10.2g镁和铝的混和粉末溶于500mL 4mol·L-1的盐酸中。若加入2mol·L-1的氢氧化钠溶液,要使产生的沉淀的质量最大,则需加入的氢氧化钠溶液的体积为
A.100ml B.500mL C.1000mL D.1500mL
19.下列离子方程式正确的是
A.铜与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
B.氯气跟水反应:C12+H2O=2H++C1-+C1O-
C.钠跟水反应:Na+2H2O=Na++2OH-+H2↑
D.氯化铁溶液中加入铜片Fe3++Cu=Fe2++Cu2+
18.等质量的CH4和NH3相比较,下列结论错误的是
A.它们的分子个数之比为17:16 B.它们的原子个数之比为17:16
C.它们的氢原子个数之比为17:12 D.同温同压下两种气体的体积之比是17:16
17.设NA代表阿伏加德罗常数,下列说法正确的是
A.23g金属钠变为钠离子时失去的电子数为NA
B.18g水所含的电子数目为NA
C.在常温常压下11.2L氯气所含的原子数目为NA
D.常温常压下32g氧气所含的原子数目为NA
16.下列操作正确的是
A.制备Fe(OH)2时,将盛NaOH(aq)的滴管伸入到试管内FeSO4(aq)的液面下
B.焰色反应是将铂丝用盐酸洗净后,直接蘸取待检物置于酒精灯或煤气灯的外焰上灼烧,观察火焰的颜色
C.为了使过滤速率加快,可用玻棒在过滤器中轻轻搅拌,加速液体流动
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com