
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ИљОнЛьКЯЮяжаИїЮяжЪШмНтадЁЂЗаЕуЁЂБЛЮќИНадФмМАдкВЛЭЌШмМСжаШмНтадЕФВЛЭЌЃЌПЩвдбЁгУЙ§ТЫКЭНсОЇЁЂеєСѓ(ЛђЗжСѓ)ЁЂжНЩЯВуЮіЁЂнЭШЁКЭЗжвКЕШЗНЗЈНјааЗжРыКЭЬсДПЁЃ
|
ЗжРыЬсДПЗНЗЈ |
ЪЪгУЗЖЮЇ |
ЪЕР§ |
|
Й§ТЫ |
ЙЬЬхгывКЬхВЛЛЅШмЕФЛьКЯЮя |
ДжбЮЕФЬсДП |
|
НсОЇгыжиНсОЇ |
 ЛьКЯЮяжаИїГЩЗждкШмМСжаШмНтЖШВЛЭЌЃЌАќРЈеєЗЂШмМСНсОЇКЭНЕЮТНсОЇ ЛьКЯЮяжаИїГЩЗждкШмМСжаШмНтЖШВЛЭЌЃЌАќРЈеєЗЂШмМСНсОЇКЭНЕЮТНсОЇ |
ЗжРыNaClКЭKNO3ЕФЛьКЯЮя |
|
еєСѓ(ЗжСѓ) |
ЂйФбЛгЗЂЕФЙЬЬхдгжЪдквКЬхжааЮГЩЕФЛьКЯЮя ЂкЛЅШмвКЬхЗаЕугаУїЯдВювь |
еєСѓЫЎЁЂЮоЫЎввДМЕФжЦБИЁЂЪЏгЭЕФЗжСѓ CCl4(ЗаЕу76.75Ёц)КЭМзБН(ЗаЕу110.6Ёц)ЛьКЯЮяЕФЗжРы |
|
ВуЮі |
БЛЮќИНФмСІВЛЭЌЕФЮяжЪЕФЗжРы |
КьЁЂРЖФЋЫЎЛьКЯЮяжаЕФВЛЭЌЩЋЕФЗжРы |
|
ЗжвК |
СНжжЛЅВЛЛьШмЕФвКЬхЛьКЯЮя |
CCl4КЭЫЎЕФЗжРы |
|
нЭШЁ |
ШмжЪдкЛЅВЛЯрШмЕФШмМСРяШмНтЖШВЛЭЌ |
РћгУCCl4ДгфхЫЎжанЭШЁфх |
зЂвтЃКВЛЭЌЕФЗжРыЗНЗЈЖМгавЛЖЈЕФЪЪгУЗЖЮЇЃЌвЊИљОнВЛЭЌЛьКЯЮяЕФаджЪбЁдёКЯЪЪЕФЗНЗЈНјааЗжРыЃЌЧвгаЪБашвЊЖржжЗНЗЈХфКЯЪЙгУЁЃ
2ЃЎНтОіЛЗОГЮЪЬташвЊЛЏбЇПЦбЇ
ЂХЁЁЖўбѕЛЏСђЁЁЕФХХЗХЪЧдьГЩСђЫсаЭЫсгъЕФжївЊдвђЃЌЮЊМѕЩйСђЫсаЭЫсгъЖдЛЗОГдьГЩЕФЮЃКІЃЌВЩгУЁЁЪЏЛвЪЏЃЪЏИрЗЈЁЁЁЂЁЁАБЫЎЗЈЁЁШМУКбЬЦјЭбСђЃЌМШПЩвдЯћГ§ШМУКбЬЦјжаЕФЖўбѕЛЏСђЃЌЭЌЪЧЪБЛЙПЩвдЕУЕНИБВњЦЗЁЁЪЏИрЁЁКЭЁЁСђЫсяЇЁЁЁЃ
ЂЦЦћГЕЗЂЖЏЛњШМгЭХХЗХЕФЮВЦјжаЁЁCOЁЂNOЁЂNO2ЁЂЬМЧтЛЏКЯЮяЁЂПХСЃЮяЁЁдьГЩЕФПеЦјЮлШОЃЌЦЦЛЕСЫЩњЬЌбЛЗЁЃЮЊЯћГ§ЦћГЕЮВЦјЫљдьГЩЕФЮлШОЃЌЫљВЩШЁЕФДыЪЉгаЃКдкЪЏгЭСЖжЦЙ§ГЬжаНјааЁЁЭбСђДІРэЁЁЃЛЗЂУїСЫЦћГЕЮВЦјЁЁДпЛЏОЛЛЏзЊЛЏзАжУЁЁЃЌЪЙЮВЦјжаЕФЁЁCOЁЂNOЁЁдкДпЛЏМСЕФзїгУЯТзЊЛЏЮЊЮоКІЕФЁЁN2ЁЂCO2КЭH2OЁЁХХГіЃЛгУаТЕФЮоКІЕФЦћгЭЬэМгМСДњЬцЁЁЫФввЛљЧІЁЁПЙе№МСЃЛЪЙгУЁЁОЦОЋЁЂЬьШЛЦјЁЁДњЬцВПЗжЛђШЋВПШМгЭЃЛЪЙгУЁЁЧтЁЁзїЦћГЕШМСЯЃЌЪЕЯжЁЁЁАСуХХЗХЁБЁЁЁЃ
ЂЧДѓЦјжаЖўбѕЛЏЬМЕФХЈЖШВЛЖЯдіМгЃЌЁЁЮТЪваЇгІЁЁШевцбЯжиЃЌЮЊДЫЃЌПЦбЇМвбаОПВЂЗЂЯжЃКЖўбѕЛЏЬМКЭЁЁЛЗбѕБћЭщЁЁдкДпЛЏМСзїгУЯТПЩЩњГЩвЛжжЁЁПЩНЕНтЫмСЯЁЁЁЃ
ЂШДгИљБОЩЯНтОіЛЗОГКЭЩњЬЌЮЪЬтЃЌвЊвРППЁЁЁАТЬЩЋЛЏбЇЁБЁЁЃЌТЬЩЋЛЏбЇвЊЧѓРћгУЛЏбЇдРэДгдДЭЗЩЯЯћГ§ЮоЮлШОЃЌЦкЭћдкЛЏбЇЗДгІКЭЛЏбЇЙЄвЕЙ§ГЬжаГфЗжРћгУВЮгыЗДгІЕФдСЯЃЌЫљгаЮяжЪдСЯЁЂжаМфВњЮяЖМдкФкВПбЛЗЁЂРћгУЃЌЪЕЯжЁАСуХХЗХЁБЁЃ
1ЃЎЯжДњПЦбЇММЪѕЕФЗЂеЙРыВЛПЊЛЏбЇ
ЂХвЛаЉПЦбЇМвШЯЮЊЃКЁЁЛЏбЇКЯГЩКЭЗжРыММЪѕЁЁЪЧШЫРрЩњДцЫљБиашЕФЃЌЪЧЁЁаХЯЂММЪѕЁЁЁЂЁЁЩњЮяММЪѕЁЁЁЂЁЁКЫПЦбЇКЭКЫЮфЦїММЪѕЁЁЁЂЁЁКНПеКНЬьКЭЕМЕЏММЪѕЁЁЁЂЁЁМЄЙтММЪѕЁЁЁЂЁЁФЩУзММЪѕВЛПЩЛђШБЕФЮяжЪЛљДЁЁЃ
ЂЦдкСЫНтЁЁЙтКЯзїгУЁЁЁЂЁЁЙЬЕЊзїгУЛњРэЁЁКЭЁЁДпЛЏМСРэТлЁЁЕФЛљДЁЩЯЃЌПЩвдЦкЭћЪЕЯжХЉвЕЕФЙЄвЕЛЏЃЌдкЙЄГЇжаЩњВњСИЪГКЭЕААзжЪЃЌЪЙШЫРрЕФЩњЛюжЪСПДѓДѓЬсИпЁЃ
2ЃЎЛЏбЇЪЧШЫРрДДдьаТЮяжЪЕФЙЄОп
ЂХдкЛЏбЇПЦбЇЕФЗЂеЙЙ§ГЬжаЃЌПЦбЇМвЛ§РлСЫЮяжЪжЦБИЕФвЛЯЕСаЗНЗЈЃЌЬиБ№ЪЧЫцзХЯжДњЁЁКЯГЩММЪѕЁЁЁЂЁЁЗжРыКЭМьбщММЪѕЁЁЕФЗЂеЙЃЌШЫУЧМКОФмЙЛЩшМЦВЂДДдьГіЗћКЯашвЊЕФаТЮяжЪЁЃ
ЂЦЕчНтдРэЕФЗЂЯжЃЌЕчНтММЪѕЕФНјВНЬсИпСЫЪГбЮЕФРћгУМлжЕЃКЁЁЕчНтШлШкЪГбЮЁЁПЩвдЕУЕНЛюЦУЕФН№ЪєФЦЃЌЖјЁЁЕчНтБЅКЭЪГбЮЫЎЁЁЕУЕНЕФЪЧЩеМюЁЂТШЦјЁЂЧтЦјЃЌРћгУЁЁЧтЦјдкТШЦјжаШМЩеЁЁдђПЩжЦЕУбЮЫсЁЃ
ЂЧ20ЪРМЭвдРДЃЌЁЁКЯГЩАБЁЁЁЂЁЁКЯГЩФђЫиЁЁЁЂЁЁКЯГЩПЙЩњЫиЁЁЕШММЪѕЕФЯрМЬЗЂУїЃЌИпЗжзгЕФЛЏбЇКЯГЩЁЂаТВФСЯЕФЧќГіВЛЧюЁЂЗжРыММЪѕВЛЖЯИФНјЃЌЪЙШЫРрЕФЩњЛюЫЎВЛВЛЖЯЬсИпЁЃ
1ЃЎЛЏбЇЪЧДђПЊЮяжЪЪРНчЕФдПГз
ЂХ19ЪРМЭЃЌЛЏбЇПЦбЇРэТлНЈСЂСЫвдЁЁдзгТлЁЁЁЂЁЁЗжзгНсТлЁЁКЭЁЁдзгМлМќРэТлЁЁЮЊжааФФкШнЕФОЕфдзгЗжзгТлЃЛЗЂЯжСЫЁЁдЊЫижмЦкТЩЁЁЃЛЬсГіСЫЁЁжЪСПЪиКуЖЈТЩЁЁЃЌЕьЖЈСЫЛЏбЇЗДгІЖЏСІбЇЛљДЁЃЛШЫЙЄКЯГЩЁЁФђЫиЁЁЃЌГЙЕзЖЏвЁСЫЁАЩњУќСІТлЁБЃЌЪЙгаЛњЛЏбЇЕУЕНбИУЭЗЂеЙЁЃ
ЂЦЛЏбЇМвБЋСжЃЌЬсГіСЫЁЁЧтМќРэТлЁЁКЭЁЁЕААзжЪЗжзгЕФТна§НсЙЙФЃаЭЁЁЃЌЮЊDNAЗжзгЫЋТна§НсЙЙФЃаЭЕФЬсГіЕьЖЈСЫЛљДЁЁЃ
ЂЧШЫРрЖдЫсМюЕФШЯЪЖЃК
ЂйЫсМюЕчРыРэТлЃК1883ФъЃЌШ№ЕфМвАЂТзФсЮкЫЙДДСЂСЫЕчРыбЇЫЕЃЌЬсГіЁЁЕчНтжЪЕчРыЪБВњЩњЕФбєРызгШЋЪЧЧтРызгЕФЁЁЪЧЫсЃЌЁЁЕчНтжЪЕчРыВњЩњЕФвѕРызгШЋЪЧЧтбѕИљРызгЕФЁЁЪЧМюЃЌЁЁЕчНтжЪЕчРыЪБМШВњЩњЧтРызггжВњЩњЧтбѕИљРызгЁЁЪЧСНадЮяжЪЃЛ
ЂкЫсМюжЪзг(H+)РэТлЃК1923ФъЃЌгжгаЛЏбЇМвЬсГіСЫдкЗЧЫЎШмвКжаКЭЮоЫЎЬѕМўЯТЪЪгУЕФЫсМюРэТлЃЌЗВФмЁЁИјГіжЪзгЕФЮяжЪЁЁЖМЪЧЫсЃЌЗВФмЁЁНгЪмжЪзгЕФЮяжЪЁЁЖМЪЧМюЃЌЁЁМШФмИјГіжЪзггжФмНгЪмжЪзгЕФЮяжЪЁЁЪЧСНадЮяжЪЁЃ
5ЃЎЕААзжЪКЭАБЛљЫс
ЂХЕААзжЪдкФГаЉЁЁХЈЮоЛњбЮШмвКЁЁжаЃЌЛсВњЩњЁЁбЮЮіЯжЯѓЁЁЃЌРћгУетвЛаджЪПЩвдЖдЕААзжЪНјааЁЁЗжРыЛђЬсДПЁЁЃЛ
ЂЦЕААзжЪдкЁЁШШЁЂЧПЫсЁЂЧПМюЁЂжиН№ЪєбЮЁЂзЯЭтЯпЁЂXЙтЁЂИЃЖћТэСжЁЂОЦОЋЕШЁЁзїгУЯТЃЌЛсЗЂЩњЁЁБфадЁЁЃЌЪЇШЅЩњРэЙІФмЃЌРћгУетвЛаджЪПЩвдНјааЁЁЩБОњЯћЖОЁЁЁЃ
ЂЧАБЛљЫсЕФНсЙЙЃКАБЛљЫсЗжзгжажСЩйКЌгавЛИіЁЁ вЛCOOHЁЁ КЭвЛИіЁЁвЛNH2ЁЁЁЃІСЃАБЛљЫсжажСЩйгавЛИіЁЁ АБЛљ ЁЁвЛИіЁЁ єШЛљ ЁЁСЌдкЁЁ ЭЌвЛИіЬМдзг ЁЁЩЯЁЃ
зЈЬтЫФЃКЛЏбЇПЦбЇгыШЫРрЮФУї
4ЃЎЬЧРр
ГЃМћЕФЬЧРргаЃКЦЯЬбЬЧЁЂесЬЧЁЂТѓбПЬЧЁЂЕэЗлКЭЯЫЮЌЫиЁЃЦфЪЧЁЁЁЁЁЁКЭЁЁЁЁЁЁЪЧЭЌЗжвьЙЙЬхЃЌЁЁЁЁЁЁКЭЁЁЁЁЁЁВЛЭЌЭЌЗжвьЙЙЬхЁЃ
ЂХЦЯЬбЬЧОпгаЛЙдадЃКФмгыЁЁвјАБШмвКЁЁЗЂЩњвјОЕЗДгІЃЛКЭЁЁаТжЦЕФЧтбѕЛЏЭаќзЧвКЁЁЗДгІВњЩњЁЁКьЩЋЕФбѕЛЏбЧЭГСЕэЁЁЁЃ
ЂЦЕэЗлШмвКгіЁЁЕтЫЎЁЁЛсБфРЖЃЌЖјЯЫЮЌЫидђВЛФмЃЌЕЋЫќУЧЖМЫЎНтЕУЕНЁЁЦЯЬбЬЧЁЁЁЃ
ЂЧЮЊМьбщЕэЗлЕФЫЎНтГЬЖШЃЌдкМгШывјАБШмвКЛђаТжЦЕФЧтбѕЛЏЭаќзЧвКжЎЧАЖМгІМгШыЁЁЧтбѕЛЏФЦШмвКЁЁЃЌФПЕФЪЧЮЊСЫЁЁжаКЭСђЫсЁЁЁЃ
3ЃЎѕЅКЭгЭѕЅ
гЭѕЅЕФЫЎНтЗДгІЃКдкЫсадЬѕМўЯТЃЌЫЎНтЩњГЩЁЁИпМЖжЌЗОЫсЁЁКЭЁЁИЪгЭЁЁЃЛдкМюадЬѕМўЯТЃЌЫЎНтЩњГЩЁЁИпМЖжЌЗОЫсФЦбЮ(гВжЌЫсФЦ)ЁЁКЭИЪгЭЁЃ
2ЃЎввЫсЕФЗжзгЮЊЁЁЁЁЁЁЃЌНсЙЙМђЪНЮЊЁЁЁЁЁЁЃЌєШЫсЕФЙйФмЭХЪЧЁЁЁЁЁЁЁЃ
ЂХввЫсЪЧвЛдЊгаЛњЁЁШѕЫсЁЁЃЌЕЋЦфЫсадБШЬМЫсвЊЁЁЧПЁЁЃЌФмЪЙЁЁзЯЩЋЪЏШяЪдвКЁЁБфКьЁЃ
ЂЦввЫсКЭввДМдкХЈСђЫсзіДпЛЏМСЃЌВЂМгШШЬѕМўЯТЃЌЗЂЩњѕЅЛЏЗДгІ(вВЪЧЁАШЁДњЗДгІЁБ)ЃКЦфжаввЫсШЅЁЁЁЁЁЁЁЁЃЌввДМШЅЁЁЁЁЁЁЃЌЦфЗДгІЗНГЬЪНПЩБэЪОЮЊЃК
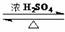 CH3CO18OH+CH3CH2OHЁЁЁЁЁЁЁЁCH3COOCH2CH3+H218O
CH3CO18OH+CH3CH2OHЁЁЁЁЁЁЁЁCH3COOCH2CH3+H218O
ЂйХЈСђЫсЕФзїгУЪЧЃКЁЁДпЛЏМСЁЁКЭЁЁЮќЫЎМСзїгУЁЁЃЛ
ЂкБЅКЭЬМЫсФЦЕФзїгУЪЧЃКОЛЛЏввЫсввѕЅЃЌБугкЗжРыЬсДПввЫсввѕЅЃЌЦфЗжРыЗНЗЈЪЧЁЁЗжвКЁЁЃЛ
ЂлЮЊЗРжЙдкМгШШЪБЗЂЩњБЉЗаЃЌдкЗДгІЛьКЯЮяжагІМгШыЁЁЗаЪЏЛђМИПщЫщДХЦЌЁЁЃЛ
ЂмМцОпФ§зїгУЕФГЄЕМЙмВЛФмВхШывКУцЯТЕФдвђЪЧЃКЗРжЙМгШШВЛОљВњЩњЁЁЕЙЮќЁЁЯжЯѓЁЃ
1ЃЎввДМЕФЗжзгЪНЮЊЁЁЁЁЁЁЁЂНсЙЙМђЪНЮЊЁЁЁЁЁЁЁЂДМЕФЙйФмЭХЪЧЁЁЁЁЁЁЁЃ
ЂХввДМгыЪЧЁЁCH3ЃOЃCH3ЁЁЭЌЗжвьЙЙЬх
ЂЦввДМдкгаДпЛЏМСДцдкЪБЃЌВЂдкМгЬѕМўЯТЃЌФмБЛбѕЦјбѕЛЏГЩЁЁЁЁCH3CHOЁЁЃЌВЂНјвЛВНбѕЛЏГЩЁЁCH3COOHЁЁЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com