
题目列表(包括答案和解析)
8. NA为阿伏加德罗常数,下列物质所含分子数最少的是
A.0.8 mol SO3
B.标准状况下4.48 L氨气
C.0.36 g水
D.含0.1NA个氢原子的甲烷
7. 下列物质在空气里变质的过程中,不涉及氧化还原反应的是
A.Na 
B.Na2SO3溶液
C.Na2O2
D.Na2SiO3溶液
6. 进行化学实验必须注意安全。下列说法正确的是
A.不能用手直接接触药品
B.剩余的药品倒入水池
C.用鼻孔凑到容器口去闻气体的气味
D.尝一下实验室酒精的味道
5. 合金是一类用途广泛的金属材料。下列物质中,不属于合金的是
A.碳素钢
B.黄铜 C.硬铝
D.水银
4.下列物质中,能使干燥的红色布条褪色的是
A.干燥的氯气
B.新制的氯水
C.潮湿的氯化氢
D.氯化钙溶液
3. 光导纤维被认为是20世纪最伟大的发明之一,它使信息科学迅猛发展。光导纤维的主要成分是
A.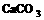
B.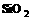

C.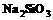
D.
2. 溶液、胶体与浊液的本质区别是
A.分散系是否有颜色
B.是否有丁达尔效应
C.能否透过滤纸
D.分散质粒子的大小
1. 对危险化学品要在包装标签上印有警示性标志,硝酸应选用的标志是




A B C D
21.将5克的钠铝合金投入到200mL的水中,固体完全溶解,产生4.48L标准状况下的气体,溶液中只有一种溶质。回答下列问题。
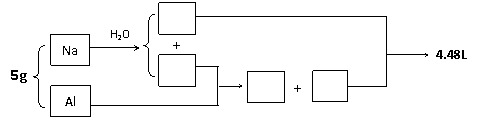 (1)处理计算问题,通常可以用图示分析的方法。以下是某同学的部分图示分析,请帮助填写完整。
(1)处理计算问题,通常可以用图示分析的方法。以下是某同学的部分图示分析,请帮助填写完整。
经过分析得出钠铝合金中两金属的物质的量之比为_______▲_______;
你得出该结论的依据是_____________▲________________。
(2)计算所得溶液的物质的量浓度。(假设溶液体积变化忽略不计)
20.(10分)含氮化合物在生产生活中有着广泛的用途
Ⅰ.Murad等三位教授最早提出NO分子在人体内有独特功能,近来此领域研究有很大进展而荣获了1998年诺贝尔医学及生理学奖。
(1)NO对环境的危害在于(填编号,有一个或多个答案) ▲ 。
A.破坏臭氧层 B.形成光化学烟雾
C.在空气中最终能形成酸雨 D.与人体内的血红蛋白结合
(2)在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO。写出Cu+和亚硝酸根(NO2-)离子在酸性水溶液中反应的离子方程式 ▲ 。
Ⅱ.2010年1月11日,我国航天专家孙家栋院士获得我国最高科技奖,发射航天飞行器离不开高能燃料。
(3)肼(N2H4)是发射航天飞船常用的一种高能燃料。将NH3和NaClO按一定物质的量比混合,在一定条件下发生反应,生成肼(N2H4)、NaCl和水,该反应中发生氧化反应的是 ▲ 。
(4)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时, 即产生在大量气体,并放出大量热。产物为水和一种无毒无害的气体,写出化学方程式 ▲ 。当有1mol过氧化氢参加反应时,转移的电子数为__ __▲_____mol.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com