
题目列表(包括答案和解析)
2.将一定质量的钠投入24.6g t℃的水中,得到t℃NaOH溶液饱和溶液31.2g。t℃时,NaOH的溶解度是
A. 48g B. 62.5g C. 23g D. 31g
1.在一定温度下,向足量的饱和Na2CO3溶液中加入1.06克无水Na2CO3,搅拌后静置,最终所得晶体的质量
A.等于1.06克 B.大于1.06克而小于2.86克
C.等于2.86克 D.大于2.86克
6、 有一种工业废水, 已知其中含有大量硫酸亚铁, 少量Ag+和Na+。今设计一种既经济又合理的方法, 回收银和硫酸亚铁。设计方案如下图所示
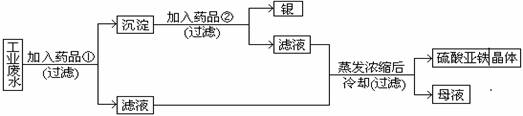
1)药品①是 (2)沉淀是
(3)药品②是 (4)母液中存在的阳离子:
4.向10 mL 0.1 mol·L-1的CuSO4溶液中加入10 mL 0.15 mol·L-1NaOH溶液时,产生一种蓝色沉淀,溶液中的Cu2+几乎被沉淀完全,该蓝色沉淀的主要成分为( )
A.Cu(OH)2 B.Cu2(OH)2CO3
C.3Cu(OH)2·CuSO4 D.Cu(OH)2·CuOH
5 某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
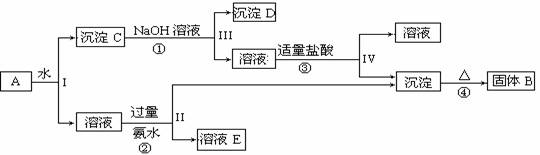 1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
。
1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
。
2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀B ;固体C ;沉淀D ;溶液E 。
3)写出①、②、③、④四个反应方程式
① ②
③ ④ 。
3.一定量的CuO和0.5L稀硫酸充分反应后,再将一根50g铁棒插入上述反应后的溶液中,当铁棒质量不再增加时,铁棒增重0.24g,并收集到224mL(标准状况下)氢气。由此可推知CuO的质量 ( )
A.2.40g B.8.00g
C.6.40g D.1.92g
2.某溶液中含有NH4+、Mg2+、Fe2+、Al3+4种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是 ( )
A.NH4+ B. Mg2+
C.Fe2+ D. Al3+
1.某铁的氧化物用1.4 mol·L-1盐酸50mL恰好溶解,所得溶液还能和56mL(标准状况下)Cl2反应,那么该氧化物的化学式为 ( )
A.Fe2O3 B.Fe3O4
C.Fe4O5 D.Fe5O7
3]Fe3O4可以写出Fe2O3·FeO,若把Fe3O4看成是一种盐,又可写成Fe(FeO2)2 根据化合价规律和化学式书写方法,把Pb3O4用上述氧化物形成表示,其化学式为________;若看成是一种盐,化学式为____________。又知,高价Fe不能把HCl氧化,而高价Pb能把HCl氧化成Cl2。试分别写出Fe3O4、Pb3O4与盐酸反应的化学方程式。
[答案] PbO2·2PbO;Pb2(PbO4);
Fe3O4+8HCl=2FeCl3+FeCl2+4H2O Pb3O4+8HCl=3PbCl2+Cl2↑+4H2O
精选题
2]已知Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu。简述如何用最简便的实验方法来检验CuO经H2还原所得到的红色产物中是否含有碱性氧化物Cu2O。要求只从下列试剂中选择:浓H2SO4、浓HNO3、稀H2SO4、稀HNO3、FeCl3。溶液及pH试纸。
1]右图试样X由氧化亚铁和氧化铜组成,取质量相等的两份试样如右图所示进行实验:试回答在题右的两个问题。
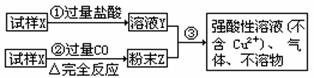
(1)请写出步骤③中所发生的全部反应的离子方程式______。
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量为m,则每份试样X中氧化铜的质量为______(用m表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com