
题目列表(包括答案和解析)
25、(9分)某有机化合物A的相对分子质量(分子量)大于110,小于150。经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧。请计算:
(1)该化合物分子中含有几个氧原子?
(2)该化合物的相对分子质量及分子式?
24、(6分)某中学化学小组查阅资料发现金属氧化物A也能催化氯酸钾的分解,且A和二氧化锰的最佳催化温度均在500℃左右。于是对A和二氧化锰的催化性能进行了定量对照实验。实验时均以收满500mL氧气为准(其他可能影响实验的因素均已忽略)。
表一 用MnO2作催化剂
|
实验序号 |
KClO3质量(g) |
MnO2质量(g) |
反应温度(℃) |
待测数据 |
|
1 |
8.00 |
2.00 |
500 |
|
|
2 |
8.00 |
2.00 |
500 |
|
表二 用A作催化剂
|
实验序号 |
KClO3质量(g) |
A质量(g) |
反应温度(℃) |
待测数据 |
|
1 |
8.00 |
2.00 |
500 |
|
|
2 |
8.00 |
2.00 |
500 |
|
请回答:
(1)上述实验中的待测数据应是:__________ ____。
(2)完成此研究后,他们准备发表一篇研究报告,请你替他们拟一个报告的题目:____________________ __________________________。
23.(6分)现有下列三个氧化还原反应:
①2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2
②2FeCl2 + Cl2 = 2FeCl3
③2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 8H2O + 5Cl2↑
(1)上述三个反应中氧化剂的氧化性由强到弱的顺序为(用具体物质的化学式或离子符号回答) 。
(2)若某溶液中有Fe2+、Cl-、I-共存,要除去I-,而不影响其它离子的存在,可加上述反应物中的(写化学式) 。
(3)在强酸性溶液中,将含有MnO4-、Fe2+、Fe3+和I-四种离子的溶液混合,充分反应后:
①若溶液中Fe3+有剩余,则溶液中可能还有 离子,一定无 离子;
②若溶液中Fe2+有剩余,则溶液中可能还有 离子,一定无 离子
22、(10分)已知,葡萄糖在乳酸菌的催化作用下可转化乳酸(C3H6O3)
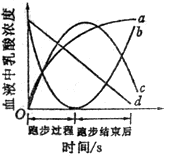
(1)上图中能够说明运动员在短跑从开始到结束后血液中乳酸浓度变化的曲线_______。
A、曲线a B、曲线b C、曲线c D、曲线d
(2)取9.0g乳酸与足量金属钠反应,可产生2.24L气体(标准状况)。另取9.0g乳酸与等物质的量的乙醇反应,生成0.1mol乳酸乙酯和1.8g H2O.乳酸在铜做催化剂时,可氧化生成物质X,向X中加入碱和银氨溶液微热,无银镜产生。
由以上实验可确定X的结构简式是_______ __,
乳酸的结构简式是___ _____。
(3)写出乳酸在一定条件下发生缩聚反应的化学方程式:
___________ __。
(4)与乳酸具有相同官能团的乳酸的同分异构体A在酸性条件下,加热失水生成B,由A生成B的化学反应方程式为:
_____________ _______。
(5)B的甲酯可以聚合,聚合物的结构简式为_________ ________。
21、(8分)X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。已知:
①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;
②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
请回答:
(1)Z2Y的化学式是 。
(2)Z2Y2与X2Y反应的化学方程式是 。
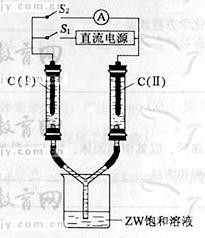
(3)如图所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气
体生成。试写出电解ZW饱和溶液的化学方程式:
;
一段时间后(两玻璃管中液面未脱离电极),
断开S1,接通S2,电流表的指针发生偏转。此时:
C(Ⅰ)的电极名称是 ;
C(Ⅱ)的电极反应式是
。
20、(8分)测定硫酸铜晶体(CuSO4·5H2O)里结晶水的含量,实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量。
请回答下列问题:
(1)现有坩埚、坩埚钳、三脚架、泥三角、玻璃棒、干燥器、药匙、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是 。
(2)该实验中哪一步骤需要使用干燥器?使用干燥器的目的是什么?
答: 。
(3)实验步骤⑥的目的是 。
(4)若操作正确而实验测得的硫酸铜晶体中结晶水的含量偏低,其原因可能有(填入选项的编号): 。
A.被测样品中含有加热不挥发的杂质 B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水 D.加热前所用的坩埚未完全干燥
19、(4分)发射卫星时可用肼(N2H4)为燃料,用NO2作氧化剂,这两种物质反应生成N2和水蒸气。已知N2(g)+2O2(g)=2NO2(g); △H1=+67.7KJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g); △H2=-534.7KJ·mol-1
(1)计算1mol肼和NO2完全反应放出的热量为_______ ___KJ
(2)写出肼和NO2反应的热化学方程式
_________________ __________。
18、在某温度下,测得甲醛、乙醛和丙酮组成的液态混合物中氢元素的质量分数为9.8%,则该混合物的平均相对分子质量为( )
A.44 B.49 C.50 D.51
第Ⅰ卷 (选择题共49分)
第Ⅱ卷(非选择题,共51分)
17、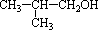 是某有机物加氢的还原产物,该有机物可能是( )
是某有机物加氢的还原产物,该有机物可能是( )
A.乙醇的同系物 B.丁醛的同分异构体
C.2-甲基丙酸 D.丁酸的同分异构体
16、在25℃,将pH=11的NaOH溶液a mL与pH=1的H2SO4溶液b mL混合,当恰好完全中和时,a与b的比值为 ( )
A.1000:1 B.100:1 C.50: 1 D.10: 1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com