
题目列表(包括答案和解析)
1.下列关于2311Na的叙述,错误的是 ( C )
A.质子数是11 B.电子数为11 C.中子数是11 D.质量数是23
27.(10分)有机化合物A广泛存在于水果肉中,尤以苹果、葡萄、西瓜、山楂内为多。已知:
① A中碳和氢的质量分数之和为40.3%,其余为氧;其相对分子质量大于110,小于150。
② A与乙酸或丙醇在浓硫酸、加热的条件下生成有香味的产物;
③ 1molA与足量的钠最多能产生1.5 mol气体;
④ A在一定温度下脱水得到产物B(不是环状化合物),B可以和溴水发生加成反应。
试回答:
(1)A的分子式为 。
(2)对A的结构可作出的判断是 (多选扣分)。
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有一COOR官能团
(3)有机物A的结构简式(不含一CH3)为 、 。
(4)A在一定温度下的脱水产物B具有顺反异构现象,B和溴水反应的化学方程式:
。
26.(10分)柠檬酸结构简式如下:
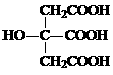
若将柠檬酸加热到150℃,则分子内失去一分子水而形成不饱和酸--顺乌头酸,后者在一定条件下会和水反应又生成柠檬酸和异柠檬酸两种异构体。
(1)写出顺乌头酸和异柠檬酸的结构简式:
顺乌头酸: 异柠檬酸: 。
(2)由柠檬酸转化为顺乌头酸的反应过程,属于 反应(填反应类型),
顺乌头酸转化为柠檬酸和异柠檬酸的反应过程,属于 反应(填反应类型)。
(3)传统塑料增塑剂为邻苯二甲酸双酯(DEHP)。因其结构中含苯环,可能致癌。柠檬酸酯无毒无味,可替代传统增塑剂。请写出用柠檬酸合成柠檬酸三乙酯(TEC)的化学方程式:
。
25.(11分)如图所示,当关闭K时,向A中充入2molX、7molY,向B中充入4molX、14molY,起始时VA=VB=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g) Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
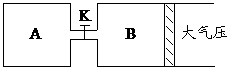 (1)B中X 的转化率α(X)B为__________。
(1)B中X 的转化率α(X)B为__________。
(2)A中W和B中Z的物质的量的比较:
n(W)A ______ n(Z)B (填<、>、或=)
(3)打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为_______升(用含a的代数式表示,连通管中气体体积不计)
(4)要使B容器恢复原来反应前的体积,可采取的措施是_________________。
24.(10分)在一个盛有催化剂的容积可变的密闭容器中,保持一定温度和压强,进行以下反应,N2(气)+3H2(气) 2NH3(气),已知加入1mol N2和4molH2时,达到平衡后生成amolNH3,在相同条件下,且保持平衡时各组分的百分含量不变,填写表中空白:
2NH3(气),已知加入1mol N2和4molH2时,达到平衡后生成amolNH3,在相同条件下,且保持平衡时各组分的百分含量不变,填写表中空白:
|
编号 |
起始物质的量(mol) |
平衡时NH3的物质的量(mol) |
||
|
N2 |
H2 |
NH3 |
||
|
已知 |
1 |
4 |
0 |
a |
|
(1) |
1.5 |
6 |
0 |
|
|
(2) |
|
|
1 |
0.5a |
|
(3) |
m |
n(n≥4m) |
|
|
23.(9分)某温度下SO2的转化反应的平衡常数K =532.4
2SO2+O2  2SO3
2SO3
下面三个混合体系中各物质的浓度如下表:
|
体系 |
c(SO2) mol/L |
c(O2) mol/L |
c(SO3) mol/L |
反应方向 |
|
(1) |
0.0600 |
0.400 |
2.000 |
|
|
(2) |
0.0960 |
0.300 |
0.500 |
|
|
(3) |
0.0862 |
0.263 |
1.020 |
|
试判断各体系中反应进行的方向:
体系(1) ;
体系(2) ;
体系(3) 。
22.(10分)在一次学生实验中,学生用铝片分别和稀盐酸、稀硫酸反应,发现:铝片与稀盐酸反应现象非常明显,而和稀硫酸几乎不反应。这和教材中“铝能跟稀盐酸或稀硫酸反应生成氢气“的说法不一致。已排除因试剂变质等因素造成的影响,该学生在教师的指导下重新进行下列实验,验证是否存在上述现象。
实验用品:仪器(略,凡是实验需要的都有)
药品:3.0mol/L盐酸、1.5mol/L硫酸、3.0mol/L硫酸,相同大小的铝片(纯度>99.5%)
实验过程:往三支相同的试管中分别加入相同的铝片各一片,再往试管中分别加入等体积的3.0mol/L盐酸、1.5mol/L硫酸、3.0mol/L硫酸,观察反应进行到1、2、5、15、20分钟时的铝与酸反应的情况。结果如下:
|
反应进程(分钟) |
1 |
2 |
5 |
15 |
20 |
|
3.0mol/L盐酸 |
少量气泡 |
较多气泡 |
大量气泡 |
反应剧烈 |
铝片耗尽 |
|
1.5mol/L硫酸 |
均无明显现象(无气泡产生) |
||||
|
3.0mol/L硫酸 |
均无明显现象(无气泡产生) |
通过上述实验可知,无论是用1.5mol/L硫酸还是3.0mol/L硫酸,均无明显的现象,而3.0mol/L盐酸与铝片反应的现象却十分明显。
(1)写出铝与酸反应的离子方程式______________________________________________
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是_______________________
________________________________________________________________________________。
(3)同学们在探究0.01mol/L KMnO4溶液与0.2mol/L H2C2O4溶液发生反应2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O时发现,反应前阶段KMnO4溶液褪色速率非常缓慢,但后阶段的褪色速率却非常快,同学们分析后阶段褪色速率却非常快是因为某物质对上述反应起了______作用,该物质可能是_________。
(4)受上述探究实验的启发,同学们顺利提出了“铝与稀盐酸和稀硫酸反应差异的原因”。你能对该问题原因做出某些假设或猜想吗?(列出两种即可,Al3+的影响已经排除)
假设一:________________________________________________________________________;
假设二:________________________________________________________________________;
如何设计实验验证你的假设,请简述你设计的实验的要点:
_______________________________________________________________________________。
21.(10分)如下图是实验室制取酚醛树脂的装置图。
(1)装置中的一处错误是_____________________________。
(2)试管上方长玻璃管的作用是_______________________。
(3)该实验不须使用温度计的原因是___________________。
(4)水浴加热的特点是_______________________________。
(5)实验完毕后,若试管用水不易洗涤,可以加入少量_______浸泡几分钟,然后洗净。
(6)写出实验室制取酚醛树脂的化学方程式_________________,
此有机反应类型是_____________________。
20.用饱和NaHCO3溶液能把括号内杂质除去的是( )
A.CO2(HCl) B.C6H6(C6H5OH)
C.CH3COOC2H5(CH3COOH) D.HCOOH(HCOONa)
19.实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④10%NaOH溶液洗 ⑤水洗,正确的操作顺序是( )
A.①②③④⑤ B.②④⑤③①
C.④②③①⑤ D.②④①⑤③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com