
题目列表(包括答案和解析)
1.水资源非常重要,联合国确定2003年为国际淡水年。下列关于水的说法中错误的是
A 蒸馏法是海水淡化的方法之一
B 淡水的密度小于海水的密度
C 融化的雪水中矿物质含量比深井水中的少
D 0℃以上,温度越高,水的密度越小
24、(9分)将W g木炭与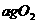 同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为
同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为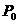 ,高温下容器中木炭与
,高温下容器中木炭与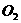 均完全反应后恢复到原温度,压力表的示数为
均完全反应后恢复到原温度,压力表的示数为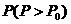 ,试求:
,试求:
(1)当W取值发生变化时,反应后压强P也发生变化,P的最大值(以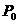 表示)是______。
表示)是______。
(2)以W表示满足题设条件的a的取值范围__________。
(3)在题设条件下,W、a、P、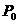 之间必须满足函数系W=f(a、
之间必须满足函数系W=f(a、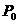 、P),写出该函数表达式:__________________。
、P),写出该函数表达式:__________________。
23.(8分)在25℃时,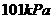 条件下,将
条件下,将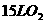 通入
通入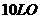 和
和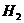 的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和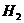 的混合气中V(CO)=__________L,
的混合气中V(CO)=__________L,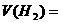 ___________L。
___________L。
(2)若剩余气体的体积是aL,则原CO和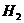 的混合气中
的混合气中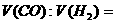 _________。
_________。
(3)若剩余气体的体积是aL,则a的取值范围是___________。
22.(12分)材料科学是近年来与化学有关的科学研究的热点。某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性。它是以中学化学中的常见物质为原料来生产的,图8-5虚线框外为其生产过程;线框内的其它转化是为探究C的组成而设,G、F、H均为难溶于水的白色固体;图中C、M、K均含A元素,其余物质均为中学化学中常见的物质。
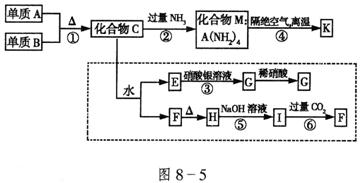
请回答下列问题:
(1)指出K可能所属的晶体类型_______,K晶体中A原子周围化学键的键角均相等,键角值为_______。
(2)写出化学式,化合物C_______,化合物F_______。
(3)写出反应的离子反应方程式:③__________;⑤__________。
(4)写出反应④的化学方程式___________。
21.(10分)由主要成分是碳酸钡、碳酸钙组成的矿石样品,某课处活动小组欲从该样品中分离出碳酸钡,尽可能除去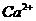 。供实验参考的数据见下表。
。供实验参考的数据见下表。
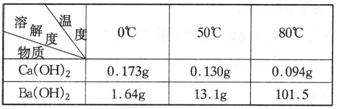
分离要求:原料是矿石;试剂只有水,不能再用其他试剂;要求将矿石经四步反应或操作后得到较纯净的碳酸钡(如图8-4所示)。
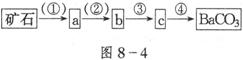
试回答下列问题:
(1)在括号中填入实验的条件或方式:①________;②________。
(2)在方框中填入对应物质的化学式:a_________;b_________。
(3)写出有关反应的化学方程式。
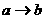 :______________________;
:______________________;
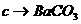 :_________________。
:_________________。
20.(10分)氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定。工业上普遍采用高纯硅与纯氮在1300℃反应获得氮化硅。
(1)根据性质,推测氮化硅属于________晶体。
(2)根据性质,推测氮化硅陶瓷的用途是_________(填序号)。
A.制汽轮机叶子 B.制有色玻璃
C.制永久性模具 D.制造柴油机
(3)根据化合价规律,推测氮化硅的化学式为_________。
(4)氮化硅陶瓷抗腐蚀性强,除氢氟酸外,它不与其他无机酸反应。试写出该陶瓷被氢氟酸腐蚀的化学方程式_____________。
(5)现用四氯化硅和氮气在氢气保护下加强热反应,可得较高纯度的氮化硅,反应的化学方程式为____________________。
19、(12分)锡、铅两种元素的主要化合价是+2价和+4价,其中+2价锡元素和+4价铅元素的化合物均是不稳定的,+2价锡元素有强还原性,+4价铅元素的化合物有强氧化性,例如: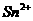 还原性比
还原性比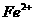 还原性强,
还原性强,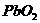 的氧化性比
的氧化性比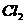 的氧化性强,根据以上的叙述,回答有关的问题:
的氧化性强,根据以上的叙述,回答有关的问题:
(1)写出下列反应的化学方程式:
①氯气与锡共热______________;
②氯气与铅共热______________;
③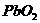 与浓盐酸共热_________________。
与浓盐酸共热_________________。
(2)能说明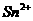 还原性比
还原性比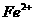 还原性强的离子方程式为______________________________
还原性强的离子方程式为______________________________
(3)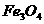 可以写成
可以写成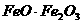 ,若把它看作一种盐时,又可写成
,若把它看作一种盐时,又可写成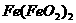 。据化合价规律和这种书写方法,可将
。据化合价规律和这种书写方法,可将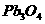 用上述氧化物形式表示,其化学式可写成________,若看成盐时可写成________。
用上述氧化物形式表示,其化学式可写成________,若看成盐时可写成________。
18、(9分)(1)绿色植物可以通过________作用吸收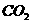 ,可以通过________作用将
,可以通过________作用将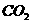 释放到大气中。
释放到大气中。
(2)人类活动可以由多种途径增加大气中的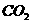 ,请写出下列会产生
,请写出下列会产生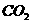 的化学方程式。
的化学方程式。
①石灰窑生产石灰__________;
②煤炭燃烧________________;
③汽油燃烧________________;
17、(12分)在半导体工业中,有一道工序叫烧氢。烧氢的工艺流程如图8-3所示。工作时,是将石英管D出口处氢气点燃。半导体硅片、焊片和金属零件从石英管口送入加热区,在氢气还原气氛中加热使焊片熔化,将单晶硅与金属零件焊接在一起。焊接后再将零件拉至冷却区,冷却后取出。烧氢工艺中的氢气纯度要求极高,工业氢气虽含氢量达99.9%,但仍含有极微量的水蒸气和氧气,所以点燃氢气前应检验氢气的纯度。试回答下列问题。
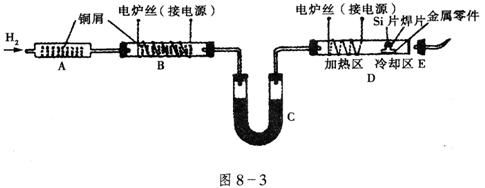
(1)装置B的作用是__________________;B中发生反应的化学方程式是___________。
(2)装置C中的物质是__________;C的作用是___________。
(3)点燃氢气前将E(带导管胶塞)接在D的出口处,目的是___________________。
(4)装置A是安全瓶,可以防止氢气燃烧回火,引起爆炸,其中填充大量纯铜屑的作用是___________________。
16、(8分)在没有现成的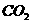 气体发生器的情况下,请你选用图8-2中的部分仪器,装配成一个简易并且能随用、随关、随停的
气体发生器的情况下,请你选用图8-2中的部分仪器,装配成一个简易并且能随用、随关、随停的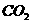 气体发生装置。
气体发生装置。
(1)应用的仪器是_________(填入仪器的编号)。
(2)若用上述装置制取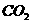 气体,而实验室只有稀
气体,而实验室只有稀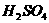 、浓
、浓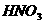 、水、纯碱、块状石灰,比较合理的方案应选用的药品是_________。
、水、纯碱、块状石灰,比较合理的方案应选用的药品是_________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com