
题目列表(包括答案和解析)
8.T℃时,将一定量的混合气体在密闭容器中发生反应:aA(g)+bB(g)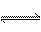 cC(g)+dD(g),平衡后测得B气体浓度为0.6mol·L-1,恒温下,将密闭容器的容积扩大1倍,重新达到平衡后,测得B气体浓度为0.4mol·L-1,下列叙述正确的是
cC(g)+dD(g),平衡后测得B气体浓度为0.6mol·L-1,恒温下,将密闭容器的容积扩大1倍,重新达到平衡后,测得B气体浓度为0.4mol·L-1,下列叙述正确的是
A.重新达到平衡时,D的体积分数减小 B.a+b<c+d
C.平衡向右移动 D.重新达到平衡时,A气体浓度增大
7.仅能在水溶液中导电的电解质是
A.SO3 B.NaCl C.Na2CO3 D.NH4Cl
6.下列变化属于物理变化的是
A.苏打晶体风化 B.浓硝酸“发烟” C.O2在放电条件下变成O3
D.漂白的草帽久置于空气中变黄
5.“绿色化学”对化学反应提出了“原子经济性”(即节约原子)的新概念及要求。理想原子经济性反应是原料分子中原子全部转化为所得到的产物中,不产生副反应,实现零排放。下列反应可能符合这一要求的是
①取代反应;②化合反应;③消去反应;④加成反应;⑤水解反应;⑥加聚反应;
A.①③⑤ B.②④⑥ C.①②③ D.④⑤⑥
4.光缆通讯能同时传输大量信息,一条光缆通路可同时容纳十亿人通话,也可以同时传送多套电视节目,是一种现代化通讯手段,制造电缆主要材料是
A.光导纤维 B.氧化铝陶瓷 C.人造纤维 D.天然有机高分子
3.一定温度下,某纯净物溶于水形成的溶液中,由水电离出来的c(H+)=10-10mol·L-1,该溶液的溶质不可能是
A.NaHSO4 B.Al2(SO4)3 C.NaOH D.HCl
2.下列有关性质判断正确的是
A.沸点:HBr<HCl B.水中溶解性: CH3CH2Br<C2H5OH
C.熔点:Li<Na<K D.密度:氨水>水
1.据最新科技报导,用10B合成的10B20有非常好的抗癌、治癌作用,下列有关说法正确的是
A.10B和10B20互为同位素 B.10B20是一种高熔点硬度大的物质
C.10B和10B20互为同分异构体 D.10B中子数与核外电子数相同
13.室温时,向一定量的稀氨水中逐滴加入某物质的量浓度的稀盐酸,直到盐酸过量。请分析上述实验过程中①所发生的反应 ②溶液的成分 ③溶液pH的变化并回答下列问题:
(1)该反应的离子方程式为___________________________________
(2)在实验过程中水的电离程度的变化趋势是先______后______(选填 大、小或不变)
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH,请将表中空格部分填上相应的内容,将表格补充完整
|
序号 |
离子浓度由大到小的顺序 |
溶质(化学式) |
溶液的pH |
|
1 |
C(NH4+)>C(OH-)>C(Cl-)>C(H+) |
|
|
|
2 |
C(NH4+)>C(Cl-)=C(OH-)>C(H+) |
|
|
|
3 |
C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
|
|
|
4 |
C(NH4+)=C(Cl-)>C(H+)=C(OH-) |
|
|
|
5 |
C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
|
=7 |
|
6 |
C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
|
|
|
7 |
C(Cl-)>C(NH4+)=C(H+)>C(OH-) |
|
|
|
8 |
C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
|
|
|
9 |
C(Cl-)>C(H+)>C(NH4+)>C(OH-) |
|
|
12.常温下,将0.01 mol CH3COONa和0.002 mol HCl溶解于水,配成1L混合溶液。请填写下列空白:
(1)该溶液中存在着以下三个平衡体系:_________、__________、________________
(2)溶液中共有________种不同的粒子(只计分子离子)
(3)这些粒子中,浓度为0.01mol/L的是__________,浓度为0.002 mol/L的是________
(4)________和______两种粒子的物质的量之和为0.01mol
(5)______和_____两种粒子的物质的量之和比H+的物质的量多0.008mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com