
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
15£ÆÕ®“‘œ‡µ»µƒµÁ¡ø£¨∑÷±µÁΩ‚µ»≈®∂»µƒœÀ·“¯£¨œÀ·—«πØ(—«πصƒªØ∫œºğŒ™+1)»İ“∫£¨»Ù±ªªπ‘≠µƒœÀ·“¯∫ÕœÀ·—«πصƒŒÔ÷ µƒ¡ø÷Ʊ»n(œÀ·“¯)£∫n(œÀ·—«πØ)=2£∫1£¨‘Úœ¬¡–±Ì ˆ’˝»∑µƒ «(°° )
°°°° A£Æ‘Ğ¡Ω∏ˆ“º´…œµ√µΩµƒ“¯∫ÕπصƒŒÔ÷ µƒ¡ø÷Ʊ»n(“¯)£∫n(πØ)=2£∫1
°°°° B£Æ‘Ğ¡Ω∏ˆ—Ùº´…œµ√µΩµƒ≤˙ŒÔµƒŒÔ÷ µƒ¡ø≤ªœ‡µ»
°°°° C£ÆœÀ·—«πصƒ∑÷◊” ΩŒ™HgNO3
°°°° D£ÆœÀ·—«πصƒ∑÷◊” ΩŒ™Hg2(NO3)2
14£Æ◊ÓΩ¸£¨ø∆—ߺ“‘Ğ µ—È “≥…π¶µÿ‘Ğ∏ş—πœ¬Ω´CO2◊™ªØŒ™¿‡À∆SiO2µƒ‘≠◊”æßÃÂΩ·ππ£¨œ¬¡–πÿ”ĞCO2æßõƒ– ˆ÷–≤ª’˝»∑µƒ «(°° )
A£ÆæßÃÂ÷–C°¢O‘≠◊”∏ˆ ˝±»Œ™1£∫2°°°°°°°°°°°°
B£Æ∏√æßõƒ»ğ°¢∑–µ„∏ş°¢”≤∂»¥Û
C£ÆæßÃÂ÷–O-C-Oº¸Ω«Œ™180°„°°°°°°°°°°°°°°°°
D£ÆæßÃÂ÷–C°¢O‘≠◊”◊ÓÕ‚≤„∂º¬˙◊„8µÁ◊”Ω·ππ
13£Æ»Ùa g FeS2‘Ğø’∆¯÷–≥‰∑÷»º…’£¨π≤◊™“∆n∏ˆµÁ◊”£¨‘Ú∞¢∑¸º”µ¬¬Ş≥£ ˝÷µø…±Ì 挙(°° )
°°°° A£Æ12n/a°°°°°°°°°°°°°°°°°°°° B£Æ120n/11a°°°°°°°°°°°°°°°° C£Æ60n/a°°°°°°°°°°°°°°°°°°°°°° D£Æ11a/120n
11£Æ÷ÿ∏À·Ôß[(NH4)2Cr2O7] «“ª÷÷ İ»»“◊∑÷Ω‚µƒ—Œ£¨œ¬¡–∏˜◊È∂‘÷ÿ∏À·Ôß İ»»∑÷Ω‚≤˙ŒÔµƒ≈–∂œ£¨∑˚∫œ—ªØªπ‘≠∑¥”¶‘≠¿Ìµƒ «(°° )
°°°° A£ÆCrO3+NO+H2O°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£ÆCr2O3+NH3+H2O
°°°° C£ÆCrO3+N2+H2O°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° D£ÆCr2O3+N2+H2O
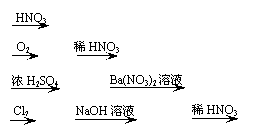 °°12£Æ°∞¬Ã…´ªØ—ß°±“™«Û¥”æ≠º√£¨ª∑±£∫Õºº …œ…˺∆∑˚∫œ°∞‘≠◊”æ≠º√–‘°±(‘≠◊”ΩĞ‘º)“™«ÛµƒªØ—ß∑¥”¶£¨¿ÌœÎµƒ‘≠◊”æ≠º√∑¥”¶ «‘≠¡œ∑÷◊”÷–µƒ‘≠◊”»´≤ø◊™±‰≥…À˘–Ë≤˙ŒÔ£¨≤ª≤˙…˙∏±≤˙ŒÔ£¨ µœ÷¡„≈≈∑≈£¨œ¬¡–º∏÷÷…˙≤˙Mg(NO3)2µƒ∑Ω∑®÷–£¨◊Ó∑˚∫œ°∞¬Ã…´ªØ—ß°±–¬¿ÌƒÓµƒ «(°° )
°°12£Æ°∞¬Ã…´ªØ—ß°±“™«Û¥”æ≠º√£¨ª∑±£∫Õºº …œ…˺∆∑˚∫œ°∞‘≠◊”æ≠º√–‘°±(‘≠◊”ΩĞ‘º)“™«ÛµƒªØ—ß∑¥”¶£¨¿ÌœÎµƒ‘≠◊”æ≠º√∑¥”¶ «‘≠¡œ∑÷◊”÷–µƒ‘≠◊”»´≤ø◊™±‰≥…À˘–Ë≤˙ŒÔ£¨≤ª≤˙…˙∏±≤˙ŒÔ£¨ µœ÷¡„≈≈∑≈£¨œ¬¡–º∏÷÷…˙≤˙Mg(NO3)2µƒ∑Ω∑®÷–£¨◊Ó∑˚∫œ°∞¬Ã…´ªØ—ß°±–¬¿ÌƒÓµƒ «(°° )
°°°° A£ÆMg°°°°°° Mg(NO3)2°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
B£ÆMg°°°° MgO°°°°°° Mg(NO3)2
°°°° C£ÆMg°°°°°°°° MgSO4°°°°°°°°°°°° Mg(NO3)2°°°°°°°°°°°°
D£ÆMg°°°° MgCl2°°°°°°°° Mg(OH)2°°°°°° Mg(NO3)2
10£Æœ¬¡–◊ˆ∑®÷–≤ª’˝»∑µƒ «(°° )
°°°° A£ÆÀÆ“¯Œ¬∂»º∆≤ª…˜À§∆∆∫Û£¨‘Ğ…¢¬‰µƒπصŒ…œ∏≤∏«¡Ú∑ğ
°°°° B£Æ±Ω∑”»İ“∫≤ª…˜’¥µΩ∆§∑Ù…œ£¨¡¢º¥”√æ∆æ´œ¥µ”
°°°° C£Æ≈®H2SO4≤ª…˜’¥µΩ∆§∑Ù…œ£¨æ°øÏ”√ÀÆ≥Âœ¥
°°°° D£Æ◊ˆπ˝“¯æµ∑¥”¶µƒ ‘πİ”√∞±ÀÆœ¥µ”
9£Æœ¬¡–– ˆ÷–µƒÀƒ÷÷∑«Ω Ù‘™Àÿ£¨À˘–Œ≥…µƒ∆¯Ã¨«‚ªØŒÔµƒŒ»∂®–‘◊Ó≤Óµƒ «(°° )
°°°° A£Æππ≥…øÛŒÔ∫Õ—“ صƒ÷˜“™‘™Àÿ°°°° °°°°°°°°°°°° B£Æø’∆¯÷–÷ ¡ø∑÷ ˝◊Ó∏şµƒ‘™Àÿ
°°°° C£Æµ•÷ ‘Ğ≥£Œ¬œ¬≥ “∫赃‘™Àÿ°°°° °°°°°°°°°°°° D£Æ–Œ≥…ªØ∫œŒÔ÷÷¿‡◊Ó∂‡µƒ‘™Àÿ
8£Æœ¬¡–æş”–Ãÿ ‚–‘ƒİµƒ≤ƒ¡œ÷–£¨”…÷˜◊‘™Àÿ∫Õ∏±◊‘™Àÿ–Œ≥…µƒªØ∫œŒÔ «(°° )
°°°° A£ÆŒ¸«‚≤ƒ¡œÔÁƒ¯∫œΩ°°°° °°°°°°°°°°°°°°°°°°°°°°°°°° B£Æ∞εºÃÂ≤ƒ¡œ…ȪØÔÿ
°°°° C£ÆÕ∏√˜Ã’¥…≤ƒ¡œŒ¯ªØ–ø°° °°°° °°°°°°°°°°°°°°°°°° D£Æ∏şŒ¬Ω·ππÃ’¥…≤ƒ¡œµ™ªØπË
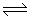 °° 6£Æ∫„Œ¬∫„—πœ¬£¨‘Ğ»ıª˝ø…±‰µƒ∆˜√Û÷–£¨∑¥”¶2NO2(g)°° °°N2O4(g) ¥ÔµΩ∆Ω∫‚∫Û£¨‘ŸœÚ»ı∆˜÷–Õ®»Î“ª∂®¡øNO2£¨”÷¥ÔµΩ∆Ω∫‚ ±£¨N2O4µƒÃª˝∑÷ ˝(°° )
°° 6£Æ∫„Œ¬∫„—πœ¬£¨‘Ğ»ıª˝ø…±‰µƒ∆˜√Û÷–£¨∑¥”¶2NO2(g)°° °°N2O4(g) ¥ÔµΩ∆Ω∫‚∫Û£¨‘ŸœÚ»ı∆˜÷–Õ®»Î“ª∂®¡øNO2£¨”÷¥ÔµΩ∆Ω∫‚ ±£¨N2O4µƒÃª˝∑÷ ˝(°° )
°°°° A£Æ≤ª±‰°°°°°°°°°°°°°°°°°°°° B£Æ‘ˆ¥Û°°°°°°°°°°°°°°°°°°°°°° C£Æº–°°°°°°°°°°°°°°°°°°°°°°° D£ÆŒŞ∑®≈–∂œ
7£Æœ¬¡–ŒÔ÷ ∞¥’’¥ø檌԰¢ªÏ∫œŒÔ°¢µÁΩ‚÷ ∫Õ∑«µÁΩ‚÷ À≥–Ú≈≈¡–µƒ «(°° )
°°°° A£Æ—ŒÀ·°¢ÀÆ√∫∆¯°¢¥◊À·°¢∏…±˘°°°° °°°°°°°°°°°° B£Æ±˘¥◊À·°¢∏£∂˚¬Ì¡÷°¢¡ÚÀ·ƒ∆°¢““¥º
°°°° C£Æµ•∏ ”Õ•°¢ªÏ∏ ”Õ•°¢ø¡–‘ºÿ°¢ ت“ Ø°° D£Æµ®∑Ø°¢∆Ø∞◊∑𰢬»ªØºÿ°¢¬»∆¯
5£Æ‘Ğ“ª∂®Ãº˛œ¬£¨RO3n£≠∫Õ∑˙∆¯ø…∑¢…˙»Áœ¬∑¥”¶£∫RO3n£≠+F2+2OH£≠=RO4£≠+2F£≠+H2O£¨¥”∂¯ø…÷™‘ĞRO3n£≠÷–£¨‘™ÀÿRµƒªØ∫œºğ «(°° )
°°°° A£Æ+4°°°°°°°°°°°°°°°°°°°°°°°° B£Æ+5°°°°°°°°°°°°°°°°°°°°°°°°°° C£Æ+6°°°°°°°°°°°°°°°°°°°°°°°°°° D£Æ+7
4£ÆR°¢X°¢Y∫ÕZ «4÷÷‘™Àÿ£¨∆‰≥£º˚ªØ∫œºğæ˘Œ™+2ºğ£¨«“X2+”ε•÷ R≤ª∑¥”¶£ªX2++Z=X+Z2+£ªY+Z2+=Y2++Z°£’‚4÷÷¿Î◊”±ªªπ‘≠≥…0ºğ ±±Ìœ÷µƒ—ªØ–‘¥Û–°∑˚∫œ(°° )
°°°° A£ÆR2+>X2+>Z2+>Y2+°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£ÆX2+>R2+>Y2+>Z2+
°°°° C£ÆY2+>Z2+>R2+>X2+°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° D£ÆZ2+>X2+>R2+>Y2+
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒŞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com