
题目列表(包括答案和解析)
9.A、B、C、D四种短周期元素,原子半径依次减小,A与C的核电荷数之比为3:4;D
可分别与A、B、C形成电子数相等的分子X、Y、Z。下列叙述正确的是 ( )
A.X、Y、Z的稳定性逐渐减弱
B.A、B、C、D只能形成4种单质
C.X、Y、Z三种化合和物的溶沸点逐渐升高。
D.A、B、C、D之间只能形成共价化合物
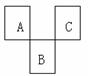 10.如图所示为元素周期表短周期的一部分,A、B、C三种元素原子核外电子数之和等于B元素原子的质量数,B元素原子核贩质子数和中子数相等。下列说法错误的是 ( )
10.如图所示为元素周期表短周期的一部分,A、B、C三种元素原子核外电子数之和等于B元素原子的质量数,B元素原子核贩质子数和中子数相等。下列说法错误的是 ( )
A.三种元素分别属于二、三周期
B.元素的原子半径大小关系是B>A>C
C.1molC与水反应时,转移的电子数为2mol
D.最高价氧化物对应的水化物具有氧化性和不稳定性的是B
8.单质Ti的机械强度高,抗蚀能力强,
有“未来金属”之称。工业上常用硫酸分解钛铁矿(FeTiO3)的方法来制取TiO2,再由
 TiO2制金属Ti。由TiO2制金属Ti的反应为
TiO2制金属Ti。由TiO2制金属Ti的反应为
①TiO2+2C+2Cl2 TiCl4+2CO ②TiCl4+2Mg 2MgCl2+Ti
则下列叙述正确的是 ( )
A.由反应①可知,Cl2是氧化剂,TiCl4是氧化产物
B.由反应①可知,可用CO在高温下把TiO2还原成Ti
C.由反应②可知,若有24gMg参加反应,就可生成1molTi
D.由反应②可知,金属Mg还原性比金属Ti的还原性强
6.化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学
键时释放(或吸收)出的能量。
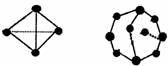 已知白磷和P4O6的分子结构如图所示:
已知白磷和P4O6的分子结构如图所示:
现提供以下化学键的键能(kJ·mol-1)
P-P 198 P-O 360 O-O 498
则反应P4(白磷)+3O2→P4O6的反应热△H为 ( )
A.-1638kJ/mol B.+1638kJ/mol
C.-126kJ/mol D.+126kJ/mol
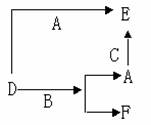 7.A、B、C分别是三种常见的金属或非金属的单质;D、E、F则是常见的三种氧化物,且
7.A、B、C分别是三种常见的金属或非金属的单质;D、E、F则是常见的三种氧化物,且
有如下所示的转化关系。下列说法中错误的是 ( )
A.D、E中一定都含有A元素
B.单质B肯定是氧化剂
C.A、B、C中一定有一种是O2
D.若A是非金属,则B一定为金属
5.在密闭容器中加少量水,常压下通氨气至饱和,则会建立下列平衡:
 NH3+H2O NH4++OH-。若要使该反应中的OH-浓度增大,应采取的措施是( )
NH3+H2O NH4++OH-。若要使该反应中的OH-浓度增大,应采取的措施是( )
A.水
B.加NH4Cl晶体
C.将氨气的压强增大1倍后,再通入密闭容器中
D.通HCl气体
4.NA代表阿伏加德罗常数,下列说法正确的是 ( )
A.1.0L1.0mol·L-1的FeCl3滴入沸水中,制得的Fe(OH)3胶体粒子数为NA
B.9gD2O中含有的电子数为5NA
C.22.4L的N2和CO的混合气体中所含的原子数为2NA
D.Na2O2与水反应生成1.12LO2(标准状况),反应中转移的电子数为0.1NA
3.下列说法中正确的是 ( )
A.能自发进行的反应都是放热反应 B.凡是熵增加的反应一定能自发进行
C.在一定条件下,吸热反应可自发进行 D.放热的熵增加的反应不一定能够自发进行
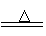
2.已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、
M分子的元素原子序数均小于10,如下图,则下列判断错误的是 ( )
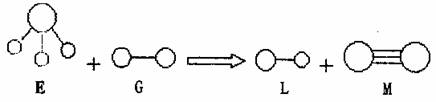
A.G是最活泼的非金属单质 B.L是极性分子
C.E能使紫色石蕊试液变蓝色 D.M化学性质活泼
1.2005年9月16日(国际臭氧层日),我省签署了“加速淘汰消耗臭氧层物质行动,创建
国家臭氧层友好省倡议书”,向国际社会庄严承诺;提前1年完成我省淘汰CFCs(全氯
氟烃)两类消耗臭氧层的物质。 ( )
A.无氟冰箱是由于使用不含氟的制冷剂,因而是环保型的。
B.我国目前已投入批量生产的哈龙(灭火剂)替代品一七氟丙烷的化学式是C3HF7
C.汽车尾气、超音速飞机排出的废气及工业废气也可以破坏臭氧层
D.人类广泛脾于制致冷剂、喷雾剂、发泡剂、清洗剂的氟氯烃类化学物质是破坏臭氢层的主要原因。
24.(12分)某种发动机燃料由A、B两种物质混合而成,A、B两种物质含有C、H、O三种元素中的两种或三种。
已知常温下A、B及CO、H2的燃烧热如下:
|
物 质 |
A |
B |
CO |
H2 |
|
燃烧热/kJ·mol-1 |
725 |
5518 |
283 |
286 |
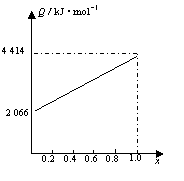 A、B按不同比例混合的燃料91.2g,在足量的氧气中燃烧时,放出的热量Q与B的物质的量分数x的关系如右图。
A、B按不同比例混合的燃料91.2g,在足量的氧气中燃烧时,放出的热量Q与B的物质的量分数x的关系如右图。
⑴A、B的相对分子质量为A________,B_______。
⑵等物质的量的A、B混合的燃料73g,在160LO2中完全燃烧,得到104L气体,通过碱石灰吸收后剩余3.2L(气体体积均在标准状况下测定)。由此可推得混合物中N(C)∶N(H)∶N(O)=____________,A分子式为_________,B分子式为_________。
⑶1mol等物质的量的A、B混合的燃料,在一定量的氧气中
燃烧,放出热量2980kJ,则反应中生成CO________mol。
23.(6分)小涛同学通过滴定法对某洗衣粉中Na5P3O10(相对分子质量为368)的含量进行测定。首先称取5.1g样品溶于一定量的硝酸中,加热使其充分酸解:Na5P3O10+5HNO3+2H2O=5NaNO3+3H3PO4;再调节溶液的pH使磷酸全部以磷酸二氢根离子形式存在;最后用0.5mol/L NaOH溶液滴定至磷酸二氢根离子全部转变成磷酸一氢根离子,消耗NaOH溶液体积16.80mL。
⑴大量使用该类洗衣粉,可能造成的环境问题是 。
⑵计算该洗衣粉中Na5P3O10的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com