
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
8ЃЎМИжжЖЬжмЦкдЊЫиЕФдзгАыОЖМАжївЊЛЏКЯМлМћЯТБэЃК
|
дЊЫиДњКХ |
L |
M |
Q |
R |
T |
|
дзгАыОЖ/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
жївЊЛЏКЯМл |
+2 |
+3 |
+6ЁЂЃ2 |
+2 |
Ѓ2 |
ЯТСаа№Ъіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎLЁЂRЕФЕЅжЪгыЯЁбЮЫсЗДгІRБШLИќОчСв
BЃЎMгыTаЮГЩЕФЛЏКЯЮягаСНад
CЃЎQЁЂTСНдЊЫиЕФЧтЛЏЮяЮШЖЈадQЃОTЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
DЃЎLгыTаЮГЩЛЏКЯЮяЙЬЬЌЪБЪЧдзгОЇЬх
7ЃЎЪвЮТЪБЃЌЯђЬхЛ§ЮЊV1ЁЂХЈЖШЮЊc1ЁЂpHЃНaЕФCH3COOHШмвКжаМгШыЬхЛ§ЮЊV2ЁЂХЈЖШЮЊc2ЁЂpHЃНbЕФNaOHШмвКЃЌГфЗжЗДгІЁЃЯТСаЙигкЗДгІКѓЛьКЯвКЕФа№ЪівЛЖЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎШєpHЃН7ЃЌЧвV1ЃНV2ЃЌдђc1ЃОc2
BЃЎШєpHЃМ7ЃЌдђc(CH3COOЃ)ЃОc(Na+)ЃОc(H+)ЃОc(OHЃ)
CЃЎШєc1ЃНc2ЃЌЧвV1ЃНV2ЃЌдђa+bЃН14
DЃЎШєpHЃО7ЃЌЧвV1ЃНV2ЃЌдђc1ЃМc2
6ЃЎгУNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎ1mol ЃOH(єЧЛљ)жаКЌгаЕчзгЪ§ЮЊ9NA
BЃЎ1 L 1mol/L ЕФТШЛЏЬњШмвКжаКЌгаЬњРызгЕФЪ§ФПЮЊNA
CЃЎ7.1gТШЦјгызуСПЧтбѕЛЏФЦШмвКЗДгІзЊвЦЕФЕчзгЪ§ЮЊ0.2NA
DЃЎБъзМзДПіЯТЃЌ11.2 L SO3ЫљКЌЕФЗжзгЪ§ЮЊ0.5NA
5ЃЎФме§ШЗБэЪОЯТСаЛЏбЇЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎБЅКЭЪЏЛвЫЎИњЯЁЯѕЫсЗДгІЁЁ Ca(OH)2+2H+ЃН Ca2++2H2O
BЃЎСђЫсТСШмвКМгЙ§СПЕФЧтбѕЛЏФЦЁЁЁЁ ЁЁAl3+ + 3OHЃ ЃН Al(OH)3Ё§
CЃЎНЋСђЫсЧтФЦЕЮМгЕНЧтбѕЛЏБЕШмвКжажСШмвКГЪжаад
Ba2++2OHЃ+2H++SO42ЃЃН BaSO4Ё§+ 2H2O
DЃЎгУДѓРэЪЏгыбЮЫсжЦШЁЖўбѕЛЏЬМЃКCO32Ѓ+2H+ЃНH2O+CO2Ёќ
4ЃЎЯТСаРызгвЛЖЈФмЙЛДѓСПЙВДцЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎNa+ЁЂAl3+ЁЂClЃЁЂHCO3ЃЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎNa+ЁЂOHЃЁЂNH4+ЁЂBa2+
CЃЎH3O+ЁЂNO3ЃЁЂFe2+ЁЂNa+ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎK+ЁЂAlO2ЃЁЂNO3ЃЁЂOHЃ
3ЃЎвбжЊ2KMnO4+16HCl(ХЈ)ЃН2KCl+2MnCl2+5Cl2Ёќ+8H2OЃЛЯТСаа№ЪіВЛе§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎЪЕбщЪвжаВЛФмгУбЮЫсРДЫсЛЏИпУЬЫсМи
BЃЎРћгУИУЗДгІжЦШЁТШЦјЪБЃЌгыгУЖўбѕЛЏУЬКЭХЈбЮЫсжЦТШЦјЪЕбщзАжУЭъШЋЯрЭЌ
CЃЎНсКЯвбгажЊЪЖПЩвдХаЖЯбѕЛЏадЧПШѕЫГађЮЊЃКMnO4ЃЃОMnO2ЃОCl2ЃОFe3+
DЃЎИУЗДгІжа1molЛЙдМСЪЇШЅ1molЕчзг
2ЃЎЩйСПЬњЗлгы100mL 0.01mol/LЕФЯЁбЮЫсЗДгІЃЌЗДгІЫйТЪЬЋТ§ЁЃЮЊСЫМгПьДЫЗДгІЫйТЪЖјВЛИФБф H2 ЕФВњСПЃЌПЩвдЪЙгУШчЯТЗНЗЈжаЕФЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЂйМгH2O ЂкМгNaOH ЙЬЬхЂлЕЮШыМИЕЮХЈбЮЫсЂмМгCH3COONa ЙЬЬхЂнМгNaCl ШмвКЁЁ
ЂоЕЮШыМИЕЮСђЫсЭШмвКЂпЩ§ИпЮТЖШ(ВЛПМТЧбЮЫсЛгЗЂ)ЂрИФгУ10mL 0.1mol/LбЮЫс
AЃЎЂйЂоЂп ЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂлЂнЂрЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂлЂпЂрЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂнЂоЂр
1ЃЎЯТСагаЙиа№ЪіжаЃЌВЛе§ШЗЕФЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎПЩЮќШыПХСЃ(Р§ШчЙшЫсбЮЗлГО)аЮГЩЦјШмНКЃЌЖдШЫРрНЁПЕЮЃКІМЋДѓ
BЃЎПЊЗЂРћгУТЬЩЋФмдД(Р§ШчЬЋбєФм)ЬцДњЛЏЪЏШМСЯЪЧШЫРрПЩГжајЗЂеЙЕФБигЩжЎТЗ
CЃЎЦЄЗєЩЯВЛЩїеДСЫБНЗгЃЌгІСЂМДгУОЦОЋЧхЯД
DЃЎЪЏгЭеєСѓЪЕбщжаЃЌЮТЖШМЦБиаыВхШывКЬхжаВП
29ЃЎ(17Зж)вбжЊЃК
|
УћГЦ |
ЛЏбЇЪН |
беЩЋЁЂзДЬЌ |
ШмНтад(g) |
ШлЕу(Ёц) |
УмЖШ(g/cm3) |
|
ввЖўЫс |
H2C2O4 |
- |
8.6(20Ёц) |
189.5 |
1.900 |
|
ЖўЫЎКЯввЖўЫс |
H2C2O4ЁЄ2H2O |
ЮоЩЋОЇЬх |
- |
101.5 |
1.650 |
зЂЃКввЖўЫс( HOOC-COOH)ЫзГЦВнЫсЃЌДј2ИіНсОЇЫЎЕФввЖўЫсЫзГЦВнЫсОЇЬхЃЌВнЫсОЇЬхЪЇШЅНсОЇЫЎЕУЮоЫЎВнЫсЃЌдкдМ157ЁцЪБЩ§ЛЊЃЌЦфбЮВнЫсИЦКЭВнЫсЧтИЦОљЮЊАзЩЋВЛШмЮяЁЃ
ИљОнЩЯЪіаХЯЂЃЌЛиД№ЯТСаЮЪЬтЁЃ
(1)ЯђЪЂгаNa2CO3ЗлФЉЕФЪдЙмРяМгШыдМ3mLввЖўЫсШмвКЃЌЙлВьЕНЕФЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЫЕУїввЖўЫсЕФЫсадБШЬМЫсЁЁЁЁЁЁ (ЬюЁАЧПЁБЛђЁАШѕЁБ)ЁЃ
(2)ЯђЪЂга5mLввЖўЫсБЅКЭШмвКЕФЪдЙмРяЕЮШы3ЕЮгУСђЫсЫсЛЏЕФ0.5%(жЪСПЗжЪ§)ЕФИпУЬЫсМиШмвКЃЌеёЕДЃЌЙлВьЕНЕФЯжЯѓЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЫЕУїввЖўЫс
гаЁЁЁЁЁЁЁЁЁЁ адЁЃ
(3)ЯђAЪдЙмжаМгШы3mLввДМЃЌШЛКѓБпеёЕДЪдЙмБпМгШы2mLХЈСђЫсКЭ2mLввЖўЫсЃЌАДЯТЭММзСЌНгКУзАжУЃЌМгШШ3-5minЃЌдкBЙмжагагЭзДЧвДјгаЯуЮЖЕФвКЬхВњЩњЃЌИУЯжЯѓЫЕУїЗЂЩњ
СЫЁЁЁЁ ЗДгІ(ЬюгаЛњЗДгІРраЭ)ЁЃдкBЪдЙмжаМгШыБЅКЭNa2CO3ШмвКЕФФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
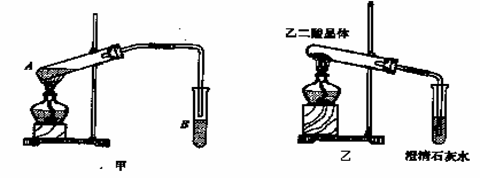 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЃЌЕМЙмдквКУцЩЯЕФдвђЪЧЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЃЌЕМЙмдквКУцЩЯЕФдвђЪЧЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(4)вбжЊВнЫсЗжНтЕФЛЏбЇЗНГЬЪНЮЊЃК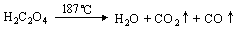 ЃЌ
ЃЌ
гУЭМввзАжУМгШШВнЫсОЇЬхЃЌбщжЄВнЫсЪмШШЗжНтМАЦфВњЮяЃЌЕЋгаШЫШЯЮЊИУзАжУВЛКЯРэЁЃЧыФуИљОнВнЫсОЇЬхЕФФГаЉЮяРэГЃЪ§КЭЪЕбщФПЕФЃЌЗжЮіВЛКЯРэдвђЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ДгЯТСаађКХжабЁдё)ЁЃ
a.ВнЫсОЇЬхЕФШлЕуЕЭЃЌЮДЗжНтжЎЧАОЭвбШкЛЏВЂСїЕНЪдЙмПкЃЌВЛРћгкЛЏбЇЗДгІЕФНјааМАЪЕбщЯжЯѓЕФЙлВь
b.вђЮЊМгШШЕФЪЧВнЫсОЇЬхЃЌЫљвдИУзАжУзюЖржЛФмМьбщвЛжжЗжНтВњЮяЃЌВЛФмМьбщЪЧЗёЛЙгаЦфЫћЗжНтВњЮя
c.дкЮДЯДЦјЕФЧщПіЯТЭЈШыЪЏЛвЫЎЃЌЛЙПЩФмвђВнЫсеєЦјгыЪЏЛвЫЎЗДгІЩњГЩВнЫсИЦГСЕэЃЌЖдЪЕбщгаИЩШХ
(5)ИУзАжУвВВЛЗћКЯТЬЩЋЛЏбЇЕФвЊЧѓЃЌЪдЫЕУїдвђЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
28ЃЎ(14Зж)УОЁЂТСЁЂЬњЪЧживЊЕФН№ЪєЃЌдкЙЄвЕЩњВњжагУЭОЙуЗКЁЃ
ЁЁ (1)УОгыЯЁСђЫсЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁ (2)ТСгыбѕЛЏЬњЗЂЩњТСШШЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁ (3)дкГБЪЊЕФПеЦјРяЃЌИжЬњБэУцгавЛВуЫЎФЄЃЌКмШнвзЗЂЩњЕчЛЏбЇИЏЪДЁЃЦфжае§МЋЕФЕчМЋЗДгІЮЊЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
ЁЁ (4)дкКЃбѓЙЄГЬЩЯЃЌЭЈГЃгУТСКЯН№(Al-Zn-Cd)
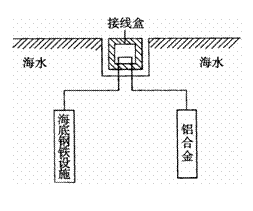 БЃЛЄКЃЕзИжЬњЩшЪЉЃЌЦфдРэШчЭМ18ЫљЪОЃК
БЃЛЄКЃЕзИжЬњЩшЪЉЃЌЦфдРэШчЭМ18ЫљЪОЃК
ЁЁЁЁ ЦфжаИКМЋЗЂЩњЕФЕчМЋЗДгІЮЊ
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
ЁЁЁЁ дкЪЕМЪгІгУжаЃЌгУТСКЯН№ЖјВЛбЁгУДПТСЁЃ
ДПТСВЛФмКмКУЕиЦ№ЕНБЃЛЄзїгУЃЌЦфдвђЪЧ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЃ
ЁЁ (5)НЋ11.9g Mg-Al-FeзщГЩЕФКЯН№ШмгкзуСПNaOHШмвКжаЃЌКЯН№жЪСПМѕЩй2.7gЁЃСэШЁЕШжЪСПЕФКЯН№ШмгкЙ§СПЕФЯЁЯѕЫсжаЃЌЩњГЩ6.72L(БъзМзДПі)NOЃЌЯђЗДгІКѓЕФШмвКжаМгШыЪЪСПЕФNaOHШмвКЧЁКУЪЙMg2+ЁЂAl3+ЁЂFe3+ЭъШЋзЊЛЏЮЊГСЕэЃЌдђГСЕэЕФжЪСПЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ g
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com