
题目列表(包括答案和解析)
22、(12分)(1)已知下列反应在一定条件下可以发生:
H2O2+4Fe2++2H+ 2Fe3++2H2O H2O2+2Fe3+ 2Fe2++O2↑+2H+
在以上反应中Fe2+实际上起着 作用,总反应为 。
(2)I2与Fe2+一样也能发生上述类似反应,类比(1)写出合适的化学反应方程式:
H2O2+I2 2HIO,
,总反应为
。
(3)在H2SO4和KI的混合溶液中加入足量的H2O2,放出大量的无色气体,溶液呈棕色,
并可以使淀粉溶液变蓝。有学生认为该反应的离子方程式为:H2O2+2I- I2+O2↑+2H+,
这个方程式正确吗? 。若正确,理由是(若认为不正确,该步不必作答) 。若不正确,写出正确的化学反应方程式(若是离子反应,写出离子反应方程式,没有离子反应的,写出化学反应方程式):
。
21、(8分)某校化学课外活动小组组装了下列仪器,如图所示。欲经过简单连接,制备中学化学中几种常见气体。
 请填写下列表格中的空白:
请填写下列表格中的空白:
|
序号 |
气体 |
装置的连接顺序(用编号表示) |
按要求填试剂名称 |
实验室制备该气体的化学反应方程式(是离子反应的要写出离子反应方程式) |
|
(1) |
CO2 |
制备→收集 ( )→( ) |
|
|
|
(2) |
NH3 |
制备→收集→尾气处理 ( )→( )→( ) |
若干燥NH3可选用的试剂 |
|
|
(3) |
Cl2 |
制备→净化→干燥→收集 →尾气处理 ( )→( )→( ) →( )→( ) |
处理尾气的试剂 |
|
20、(7分)位于短周期的四种主族元素A、B、C、D原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。根据你的推断回答下列问题:
(1)写出由上述元素形成的具有漂白作用的四种物质的化学式 , , , 。
(2)C与D形成D的最低价化合物的电子式:______
(3)仅由B、C、D三种元素形成的一种盐,溶于水后呈碱性,请用一个离子方程式表示其呈碱性的原因:______ 。
19、(6分)可用于分离或提纯物质的方法有:
A、分馏 B、盐析 C、过滤 D、重结晶 E、升华 F、渗析 G、电解
H、加热分解 I、蒸馏 J、灼热氧化。如欲分离或提纯下列各组混合物,请选择上
述方法中最合适者,并将相应字母填入题后空格内:
(1)从石油中分离出汽油和煤油等成分
(2)除去淀粉溶液中的少量碘化钠
(3)从油脂皂化反应后的混合液中分离出高级脂肪酸钠
(4)除去粗铜中锌、银等金属
(5)除去水中的Na+、SO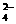 、Cl-等杂质
、Cl-等杂质
(6)除去KNO3晶体中混有的少量NaCl
18、有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为(还原性I->Fe2+>Br->Cl-)
A、7∶1 B、7∶2 C、7∶3 D、7∶4
17、下列各组溶液,不用其他试剂就不能鉴别的是
A.FeCl3、NaNO3、Na2CO3、NaCl B.NaOH、MgSO4、Na2CO3、NaHSO4
C.AgNO3、KNO3、KCl、NaI D.HCl、BaCl2、NaOH、CuSO4
16、200C时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1,则下列说法不正确的是
A、250C时,饱和KCl溶液的浓度大于4.0 mol·L-1
B、此溶液中KCl的质量分数为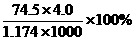
C、200C时,密度小于1.174g·cm-3的KCl溶液是不饱和溶液
D、将此溶液蒸发部分水,再恢复到200C时,溶液密度一定大于1.174g·cm-3
15、下列反应的离子方程式书写正确的是
A、碳酸氢钙溶液中加入过量的NaOH溶液:
Ca2++HCO3-+OH-=CaCO3↓+H2O
B、溶液中NH4HSO3与NaOH等物质的量混合:
NH4++HSO3-+2OH-=SO32-+NH3·H2O+H2O
C、过量的CO2通入NaAlO2溶液中:
CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-
D、硫化钠溶于水中:S2-+H2O=HS-+OH-
14、质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为
A.等于2c mol/L B.大于2c mol/L
C.小于2c mol/L D.在c mol/L∽2c mol/L之间
13、下列各项实验操作中,正确的是
A.为使制取H2的速率加快,可向H2SO4中加少量CuSO4溶液
B.为加快过滤速度,可用玻璃棒搅拌过滤器中的食盐水
C.配制一定物质的量浓度的溶液时,容量瓶用水洗涤后再用所配溶液洗涤
D.为除去试管内壁上的“银镜”,可用氨水洗涤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com