
题目列表(包括答案和解析)
5. 25 ℃时,水的电离达到平衡:H2O H++OH-;DH>0,下列叙述正确的是 ( )
H++OH-;DH>0,下列叙述正确的是 ( )
A. 向水中加入稀氨水,平衡向逆反应方向移动,c(OH-)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C. 向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低
D. 将水加热,KW增大,pH不变
4. 下列关于盐酸与醋酸两种稀溶液的说法正确的是 ( )
A. 相同浓度的两溶液中c(H+)相同
B. 100 mL 0.1 mol/L的两溶液能中和等物质的量的氢氧化钠
C. pH=3的两溶液稀释100倍,pH都为5
D.两溶液中分别加入少量对应的钠盐,c(H+)均明显减小
3. 下列叙述正确的是 ( )
A. 95 ℃纯水的pH<7,说明加热可导致水呈酸性
B. pH = 3的醋酸溶液,稀释至10倍后pH = 4
C. 0.2 mol·L-1的盐酸,与等体积水混合后pH = 1
D. pH = 3的醋酸溶液,与pH = 11的氢氧化钠溶液等体积混合后pH>7
2. 用食用白醋(醋酸浓度约为1 mol/L)进行下列实验,能证明醋酸为弱电解质的是 ( )
A. 白醋中滴入石蕊试液呈红色
B. 白醋加入豆浆中有沉淀产生
C. 蛋壳浸泡在白醋中有气体放出
D. pH试纸显示醋酸的pH为2-3
1. 下列可用于测定溶液pH且精确度最高的是( )
A. 酸碱指示剂 B. pH计 C. 精密pH试纸 D. 广泛pH试纸
2.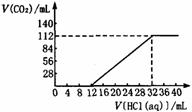 (14分)今有碱金属的两种碳酸盐组成的混合物6.14g,加水溶解后,取所得溶液的十分之一,向其中缓慢滴加一定浓度的盐酸,并同时记录放出CO2的体积(标准状况)和消耗盐酸的体积,得到右图所示的曲线。试计算:
(14分)今有碱金属的两种碳酸盐组成的混合物6.14g,加水溶解后,取所得溶液的十分之一,向其中缓慢滴加一定浓度的盐酸,并同时记录放出CO2的体积(标准状况)和消耗盐酸的体积,得到右图所示的曲线。试计算:
(1)混合物中碳元素的质量分数。
(2)所滴加盐酸的物质的量浓度。
1.(10分)现有一种碱金属的碳酸正盐和另一种碱金属的酸式碳酸盐组成的混合物,取0.506g该混合物加热至质量不再发生变化为止。把放出的气体通入足量的澄清石灰水中,得到0.200g白色沉淀。把加热后残留的固体与足量稀硫酸充分反应,生成的气体经充分干燥后通过足量的过氧化钠粉末,结果过氧化钠粉末增重0.084g。问: (1)混合物中酸式碳酸盐有_________g(不用写计算过程) (2)加热灼烧后残留固体含碳酸盐___________g(不用写计算过程) (3)通过计算,确定这两种盐的化学式,写出计算和推理过程。
3.(10分) 草木灰中含有碳酸钾,海草灰中含有碘盐,从草木灰中提取碳酸钾,
从海草灰中提取碘,并作有关检验操作:
(1)用石蕊试纸检验溶液的酸碱性,正确的操作方法
(2) 从草木灰中提取钾盐,过滤后的溶液在蒸发皿里加热以得到钾盐晶体,加热过程中要 ,当加热到
时停止加热。
(3)某学生用灼烧后的无锈铁丝沾上了钾盐,但在酒精灯上灼烧时看到火焰是黄色而看不到紫色,这是因为
(4) 将氯气通入海藻灰溶液,溶液变为浅棕色,将CCl4加入该溶液中,充分振荡静置
分层后,下层液体的颜色是
2.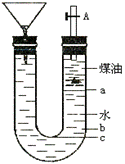 (10分)用右图的实验装置可以进行钠跟水的反应实验,并可收集、检验生成的气体。Na的密度为0.97g/mL,煤油的密度为0.87g/mL,请回答下列问题:
(10分)用右图的实验装置可以进行钠跟水的反应实验,并可收集、检验生成的气体。Na的密度为0.97g/mL,煤油的密度为0.87g/mL,请回答下列问题:
(1)液体物质添加完毕后,关闭活栓,打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,反应开始前钠的位置在_____处(填a、b、c);
(2)反应后,钠在煤油层和水层界面之间上下跳动,反应平缓连续进行。试说明产生上述现象的原因:
(3)写出Na跟水反应的离子方程式
(4)装置中的漏斗在反应过程中的主要作用是_______________;
(5)本实验除能使反应平缓连续进行、收集并检验气体外,还有一个优点是
。
这是因为___________________________________________ _。
1. (8分) 现有失去标签的四瓶无色溶液A.B.C.D,只知它们是K2CO3、K2SO4、NaHSO4和Ba(NO3)2,为鉴别它们,进行如下实验.
①A+D 溶液+气体; ②B+C
溶液+气体; ②B+C 溶液+沉淀;
溶液+沉淀;
③B+D 溶液+沉淀; ④A+B
溶液+沉淀; ④A+B 溶液+沉淀.
溶液+沉淀.
将④得到的沉淀物加入③所得的溶液中,沉淀很快溶解并产生无色无味的气体.根据以上实验事实,请回答如下问题:
(1)A.B.C.D四种无色溶液分别为:________、________、________、________.(用化学式表示)
(2)离子方程式为:①__________________
⑤___________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com