
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
16ΓΔ(Ι≤10Ζ÷)(1)Na+[ ]Θ≠ΓΓ OΘΫCΘΫOΓΓ Fe(OH)3(Ης1Ζ÷)
(2)¬»ΦνΙΛ“ΒΓΓ 2NaCl+2H2O
]Θ≠ΓΓ OΘΫCΘΫOΓΓ Fe(OH)3(Ης1Ζ÷)
(2)¬»ΦνΙΛ“ΒΓΓ 2NaCl+2H2O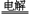 2NaOH+H2Γϋ+Cl2Γϋ(«ΑΩ’1Ζ÷Θ§ΚσΩ’2Ζ÷)
(3)2Fe2++Cl2ΘΫ2Fe3++2ClΘ≠ΓΓ FeO+2H+ΘΫ2Fe2++H2O(Ης1Ζ÷)
(4)FeC2O4(2Ζ÷)
2NaOH+H2Γϋ+Cl2Γϋ(«ΑΩ’1Ζ÷Θ§ΚσΩ’2Ζ÷)
(3)2Fe2++Cl2ΘΫ2Fe3++2ClΘ≠ΓΓ FeO+2H+ΘΫ2Fe2++H2O(Ης1Ζ÷)
(4)FeC2O4(2Ζ÷)
15ΓΔ(ΟΩΩ’1Ζ÷Θ§Ι≤6Ζ÷)NO2ΘΜ Br2ΘΜ HClΘΜ NH3ΘΜ HClΓΔCO2ΘΜ CH4
9ΓΔBCΓΓ 10ΓΔDΓΓ 11ΓΔBΓΓ 12ΓΔCDΓΓ 13ΓΔBCΓΓ 14ΓΔAC
1ΓΔΓΓ BΓΓ 2ΓΔCΓΓ 3ΓΔBΓΓ 4ΓΔCΓΓ 5ΓΔDΓΓ 6ΓΔCΓΓ 7ΓΔDΓΓ 8ΓΔD
21ΓΔ ( Β―ιΜ·―ß)Ρ≥ΩΈΆβΜνΕ·–ΓΉι―ß…ζΡΘΡβΚτΈϋΟφΨΏ÷–ΒΡ‘≠άμ(Ιΐ―θΜ·ΡΤ”κ≥± ΣΕΰ―θΜ·ΧΦΖ¥”Π)Θ§…ηΦΤ”Οœ¬ΆΦΥυ ΨΒΡ“«Τςά¥÷Τ»Γ―θΤχ≤Δ≤βΝΩ―θΤχΒΡΧεΜΐΓΘ
ΓΓ
ΓΓ
( Β―ιΜ·―ß)Ρ≥ΩΈΆβΜνΕ·–ΓΉι―ß…ζΡΘΡβΚτΈϋΟφΨΏ÷–ΒΡ‘≠άμ(Ιΐ―θΜ·ΡΤ”κ≥± ΣΕΰ―θΜ·ΧΦΖ¥”Π)Θ§…ηΦΤ”Οœ¬ΆΦΥυ ΨΒΡ“«Τςά¥÷Τ»Γ―θΤχ≤Δ≤βΝΩ―θΤχΒΡΧεΜΐΓΘ
ΓΓ
ΓΓ
ΓΓ…œΆΦ÷–ΝΩΤχΉΑ÷ΟE «”…ΦΉΓΔ““ΝΫΗυ≤ΘΝßΙήΉι≥…Θ§ΥϋΟ«”ΟœπΤΛΙήΝ§Ά®Θ§≤ΔΉΑ»κ ΝΩΥ°ΓΘΦΉΙή”–ΩΧΕ»(0-50mL)Θ§Ι©ΝΩΤχ”ΟΘΜ““ΙήΩ……œœ¬“ΤΕ·Θ§“‘ΒςΫΎ“ΚΟφΗΏΒΆΓΘ ΓΓ Β―ι “Ω…Ι©―Γ”ΟΒΡ“©ΤΖΜΙ”–ΘΚœΓΝρΥαΓΔ―ΈΥαΓΔΙΐ―θΜ·ΡΤΓΔΧΦΥαΡΤΓΔ¥σάμ ·ΓΔΥ° ΓΓ ‘ΜΊ¥πΘΚ(1)…œ ωΉΑ÷ΟΒΡΝ§Ϋ”Υ≥–ρ «(ΧνΗςΫ”ΩΎΒΡ±ύΚ≈Θ§Τδ÷–Ν§Ϋ”ΫΚΙήΦΑΦ–≥÷ΉΑ÷ΟΨυ Γ¬‘)ΘΚ___________ΓΘ ΓΓ(2)ΉΑ÷ΟC÷–Ζ≈»κΒΡΖ¥”ΠΈο «__________ΚΆ__________ΓΘ ΓΓ(3)ΉΑ÷ΟAΒΡΉς”Ο «__________Θ§ΉΑ÷ΟBΒΡΉς”Ο «__________ΓΘ ΓΓ(4)ΈΣΝΥΫœΉΦ»ΖΒΊ≤βΝΩ―θΤχΒΡΧεΜΐΘ§≥ΐΝΥ±Ί–κΦλ≤ι’ϊΗωΉΑ÷ΟΒΡΤχΟή–‘÷°ΆβΘ§‘ΎΕΝ»ΓΖ¥”Π«ΑΚσΦΉΙή÷–“ΚΟφΒΡΕΝ ΐΘ§«σΤδ≤ν÷ΒΒΡΙΐ≥Χ÷–Θ§”ΠΉΔ“β____________ΚΆ____________(Χν–¥Ή÷ΡΗ±ύΚ≈)ΓΘ ΓΓaΘ° ”œΏ”κΑΦ“ΚΟφΉνΒΆ ΐœύΤΫ ΓΓbΘ°Β»¥ΐΤ§ΩΧΘ§¥ΐ““Ιή÷–“ΚΟφ≤Μ‘Ό…œ…ΐ ±Θ§ΝΔΩΧΕΝ ΐ ΓΓcΘ°ΕΝ ΐ ±”Π…œœ¬“ΤΕ·““ΙήΘ§ ΙΦΉΓΔ““ΝΫΙή“ΚΟφœύΤΫ ΓΓdΘ°ΕΝ ΐ ±≤Μ“ΜΕ® ΙΦΉΓΔ““Ιή“ΚΟφœύΤΫ
¥πΑΗ≤ΩΖ÷ΘΚ
21ΓΔ(Έο÷ ΫαΙΙ”κ–‘÷ )–¬–ΆΫΎΡή≤ΡΝœΗΏΈ¬≥§ΒΦΧεΒΡΉνœ»ΆΜΤΤ «‘Ύ1987Ρξ¥”–¬ΒΡνΤ±ΒΆ≠―θ≤ΡΝœΒΡ―–ΨΩΩΣ ΦΒΡΓΘ‘Ύ÷Τ±ΗνΤ±ΒΆ≠―θΗΏΈ¬≥§ΒΦΧεΒΡΆ§ ±Θ§≈Φ»ΜΒΟΒΫΝΥΗ±≤ζΤΖ--Ήœ…ΪΒΡΙηΥαΆ≠±ΒΓΘ¥’«…ΒΡ «Θ§Κσ’Ώ’ΐ «ΖΔœ÷”Ύ÷–ΚΙ¥ζΤςΈο…œΒΡ±Μ≥ΤΈΣΓΑΚΙΉœΓ±ΒΡ―’ΝœΘ§ΜΙΖΔœ÷”Ύ«ΊΌΗ≤ ΜφΓΘ
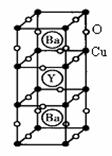 νΤ±ΒΆ≠―θΒΡΨßΑϊΫαΙΙ»γΆΦΓΘ―–ΨΩΖΔœ÷Θ§¥ΥΗΏΈ¬≥§ΒΦΧε÷–ΒΡΆ≠‘ΣΥΊ”–ΝΫ÷÷ΦέΧ§Θ§+2ΦέΚΆ+3ΦέΓΘ
νΤ±ΒΆ≠―θΒΡΨßΑϊΫαΙΙ»γΆΦΓΘ―–ΨΩΖΔœ÷Θ§¥ΥΗΏΈ¬≥§ΒΦΧε÷–ΒΡΆ≠‘ΣΥΊ”–ΝΫ÷÷ΦέΧ§Θ§+2ΦέΚΆ+3ΦέΓΘ
(1)Ηχ≥ωΆ≠‘Ύ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο(÷ήΤΎΚΆΉε)ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(2)–¥≥ωCu3+ΒΡΚΥΆβΒγΉ”≈≈≤ΦΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ
(3)ΗυΨίΆΦ ΨΨßΑϊΫαΙΙΘ§ΆΤΥψΨßΧε÷–YΘ§CuΘ§BaΚΆO‘≠Ή”Ηω ΐ±»Θ§»ΖΕ®ΤδΜ·―ß ΫΈΣΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ
(4)ΗυΨί(3)ΥυΆΤ≥ωΒΡΜ·ΚœΈοΒΡΉι≥…Θ§ΦΤΥψ≥ωΤδ÷–Cu‘≠Ή”ΒΡΤΫΨυΜ·ΚœΦέ(ΗΟΜ·ΚœΈο÷–Ης‘ΣΥΊΒΡΜ·ΚœΦέΈΣY+3ΓΔBa+2)Θ§ΉνΚσΦΤΥψΜ·ΚœΈο÷–’βΝΫ÷÷ΦέΧ§Cu‘≠Ή”Ηω ΐ±»ΈΣΘΚ_______________ΓΘ
(5)‘ΎΝρΥαΆ≠»ή“Κ÷–Ά®»κΙΐΝΩΒΡΑ±ΤχΘ§–Γ–Ρ’τΖΔΘ§Ήν÷’ΒΟΒΫΒΡΘέCu(NH3)4ΘίSO4ΨßΧε÷–Κ§”–ΒΡΜ·―ßΦϋ≥ΐΝΥΤ’Ά®Ι≤ΦέΦϋΆβΘ§ΜΙ”–ΓΓΓΓΓΓΓΓΓΓΓΓ ΚΆΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
20ΓΔœ÷”–Κ§CaO‘”÷ ΒΡCaC2 ‘―υΓΘΡ≥―–ΨΩ–‘―ßœΑ–ΓΉιΒΡΆ§―ßΡβ”Ο“‘œ¬»ΐ÷÷ΖΫΑΗ≤βΕ®CaC2 ‘―υΒΡ¥ΩΕ»ΓΘ«κΧν–¥œ¬Ν–Ω’ΑΉΘΚ
(1)ΒΎ“Μ÷÷ΖΫΑΗΘΚ«κ¥”œ¬ΆΦ÷–―Γ”Ο Β±ΒΡΉΑ÷ΟΘ§…ηΦΤ“ΜΗω Β―ιΘ§≤βΕ®CaC2 ‘―υΒΡ¥ΩΕ»ΓΘ
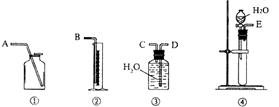
Υυ―ÔϹΑ÷ΟΒΡΝ§Ϋ”Υ≥–ρ”Π «(ΧνΗςΫ”ΩΎΒΡΉ÷ΡΗ)ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
|
ΓΓ |
ΕΝ ΐ¥Έ ΐ |
÷ ΝΩ/g |
|
ΉΕ–ΈΤΩ+Υ°+ ‘―υ |
ΒΎ1¥Έ |
196.30 |
|
ΒΎ2¥Έ |
196.15 |
|
|
ΒΎ3¥Έ |
196.05 |
|
|
ΒΎ4¥Έ |
196.00 |
|
|
ΒΎ5¥Έ |
196.00 |
(2)ΒΎΕΰ÷÷ΖΫΑΗΘΚΗυΨί ‘―υΚΆΥ°‘ΎΉΕ–ΈΤΩ÷–Ζ¥”Π«ΑΚσ÷ ΝΩΒΡ±δΜ·Θ§≤βΕ®CaC2ΒΡ÷ ΝΩΖ÷ ΐΓΘœ»≥Τ»Γ ‘―υ1.50gΓΔΉΕ–ΈΤΩΚΆΥ°ΒΡ÷ ΝΩΈΣ195.00gΘ§‘ΌΫΪ ‘―υΦ”»κΉΕ–ΈΤΩ÷–Θ§Ζ¥”ΠΙΐ≥Χ÷–ΟΩΗτœύΆ§ ±Φδ≤βΒΟΒΡ ΐΨί»γ”“±μΘΚ
ΦΤΥψCaC2ΒΡ÷ ΝΩΖ÷ ΐ ±Θ§±Ί–η”ΟΒΡ ΐΨί «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ≤Μ±ΊΉςΒΎ6¥ΈΕΝ ΐΒΡ‘≠“ρ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ¥Υ ‘―υ÷–CaC2ΒΡ÷ ΝΩΖ÷ ΐΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3)ΒΎ»ΐ÷÷ΖΫΑΗΘΚ≥Τ»Γ“ΜΕ®÷ ΝΩΒΡ ‘―υ(1.60g)Θ§≤ΌΉςΝς≥Χ»γœ¬ΘΚ
ΔΌ≤ΌΉςΔρΒΡΟϊ≥Τ «ΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎΜΙ–η÷±Ϋ”≤βΕ®ΒΡΈοάμΝΩ «ΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
Δέ‘ΎΉΣ“Τ»ή“Κ ±Θ§»γ»ή“ΚΉΣ“Τ≤ΜΆξ»ΪΘ§‘ρCaC2÷ ΝΩΖ÷ ΐΒΡ≤βΕ®ΫαΙϊΓΓΓΓΓΓΓΓ (ΧνΓΑΤΪ¥σΓ±ΓΔΓΑΤΪ–ΓΓ±ΜρΓΑ≤Μ±δΓ±)ΓΘ
Δή«κ÷Η≥ωΗΟ Β―ιΖΫΑΗΒΡ2Ηω≤ΜΉψ÷°¥ΠΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
Δί«κΗΡΫχ’βΗω Β―ιΖΫΑΗΘ§÷Ν…ΌΫβΨωΤδ÷–1Ηω≤ΜΉψ÷°¥Π
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓ
19ΓΔ“―÷ΣΘΚ
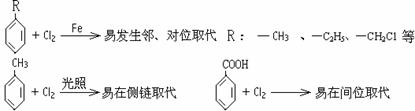
Ρ≥”–ΜζΈοAΒΡœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ198.5Θ§AΗ欻ΤχΖ¥”ΠΘ§‘ΎΧζΖέ¥φ‘Ύœ¬÷Μ”–“ΜΗω«β‘≠Ή”±Μ»Γ¥ζ ±ΡήΒΟΒΫΝΫ÷÷”–Μζ≤ζΈοΘ§Εχ‘ΎΙβ’’œ¬÷Μ”–“ΜΗω«β‘≠Ή”±Μ»Γ¥ζ ±Θ§÷ΜΡήΒΟΒΫ“Μ÷÷”–Μζ≤ζΈοΘΜAΗζNaHCO3Ζ¥”ΠΘ§≤ζ…ζ Ι ·Μ“Υ°±δΜκΉ«ΒΡΈό…ΪΤχΧεΘΜA‘ΎNaOH¥φ‘Ύœ¬Υ°ΫβΚσΒΡ»ή“Κ”ΟœθΥαΥαΜ·Θ§‘ΌΦ”»κœθΥα“χ»ή“ΚΘ§ΜαΝΔΦ¥…ζ≥…ΑΉ…Ϊ≥ΝΒμΓΘ
A‘Ύ“ΜΕ®ΧθΦΰœ¬Ω…ΖΔ…ζœ¬Ν–“ΜœΒΝ–Ζ¥”ΠΘ§Ήν÷’…ζ≥…DΚΆFΘΜ
 (1)–¥≥ωœ¬Ν–Έο÷ ΒΡΫαΙΙΦρ ΫΘΚ
(1)–¥≥ωœ¬Ν–Έο÷ ΒΡΫαΙΙΦρ ΫΘΚ
AΘΚΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓCΘΚΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓDΘΚΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓFΘΚ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(2)÷Η≥ωœ¬Ν–±δΜ·ΒΡΖ¥”Πάύ–ΆΘΚΔΌAΓζBΘΚΓΓΓΓ ΓΓΓΓΓΓΔΎCΓζDΘΚ ΓΓΓΓΓΓΓΓΔέCΓζEΘΚΓΓ ΓΓΓΓΓΓ
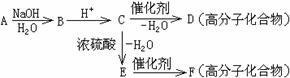
18ΓΔAΈΣΖΦœψΧΰΒΡ―ή…ζΈοΘ§÷ΜΚ§CΓΔHΓΔO»ΐ÷÷‘ΣΥΊΘ§±ΫΜΖ…œ÷Μ”–ΝΫ÷÷»Γ¥ζΜυΘ§≤Δ«“’βΝΫ÷÷»Γ¥ζΜυ¥Π”ΎΝΎΈΜΘ§AΒΡœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ164ΓΘA≤ΜΡή ΙFeCl3»ή“Κ±δ…ΪΘ§ΒΪΩ…±Μ“χΑ±»ή“Κ―θΜ·ΈΣBΘΜBΡή‘Ύ≈®H2SO4¥φ‘ΎΚΆΦ”»»ΧθΦΰœ¬ΖΔ…ζΖ÷Ή”ΡΎΒΡθΞΜ·Ζ¥”Π…ζ≥…CΘ§CΖ÷Ή”÷–≥ΐ±ΫΜΖΆβΜΙ”–“ΜΗωΚ§―θΒΡΝυ‘ΣΜΖ(”κ±ΫΜΖΙ≤”Ο2ΗωC‘≠Ή”)ΓΘ
(1)BΖ÷Ή”÷–ΒΡΚ§―θΙΌΡήΆ≈ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2)AΒΡ±ΫΜΖ…œΝΫΗω»Γ¥ζΜυ÷–ΒΡΧΦ‘≠Ή”Ήή ΐ «(Χν ΐΉ÷)ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3) ‘–¥≥ωΤδ÷–ΒΡ»Έ“βΝΫ÷÷AΦΑΤδΕ‘”ΠΒΡCΒΡΫαΙΙΦρ Ϋ(«κΑ¥Ε‘”ΠΙΊœΒΖ÷ΉιΧν–¥)
ΓΓΓΓΓΓ ΒΎ“ΜΉιAΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓCΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓ ΒΎΕΰΉιAΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓCΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
17ΓΔ–ΘΑλ≥ßΤ·ΑΉ≥ΒΦδ–η22.4L(±ξΉΦΉ¥Ωω)SO2ΓΘΜ·―ß–ΓΉιΆ§―ß“άΨίΜ·―ßΖΫ≥Χ ΫZn+2H2SO4(≈®) ZnSO4+SO2Γϋ+2H2OΦΤΥψΚσΘ§»Γ65.0g–ΩΝΘ”κ98%ΒΡ≈®H2SO4(Π―ΘΫ1.84g/cm3)110mL≥δΖ÷Ζ¥”ΠΘ§–Ω»Ϊ≤Ω»ήΫβΚσΘ§Φ¥ΫΪ ’Φ·ΥυΒΟΤχΧε»γ ΐΥΆ÷Ν≥ΒΦδΘ§≤ΜΝœΨ≠÷ ΦλΩΤΦλ―ι¥φ‘Ύ―œ÷Ί÷ ΝΩΈ ΧβΘ§ΤχΧεΥφΦ¥±ΜΆΥΜΊΓΘ
ZnSO4+SO2Γϋ+2H2OΦΤΥψΚσΘ§»Γ65.0g–ΩΝΘ”κ98%ΒΡ≈®H2SO4(Π―ΘΫ1.84g/cm3)110mL≥δΖ÷Ζ¥”ΠΘ§–Ω»Ϊ≤Ω»ήΫβΚσΘ§Φ¥ΫΪ ’Φ·ΥυΒΟΤχΧε»γ ΐΥΆ÷Ν≥ΒΦδΘ§≤ΜΝœΨ≠÷ ΦλΩΤΦλ―ι¥φ‘Ύ―œ÷Ί÷ ΝΩΈ ΧβΘ§ΤχΧεΥφΦ¥±ΜΆΥΜΊΓΘ
(1)Μ·―ß–ΓΉιΥυ÷ΤΒΟΒΡΤχΧε÷–Μλ”–ΒΡ÷ς“Σ‘”÷ ΤχΧεΩ…Ρή «ΓΓΓΓΓΓΓΓ (ΧνΖ÷Ή” Ϋ)ΓΘ≤ζ…ζ’β÷÷ΫαΙϊΒΡ÷ς“Σ‘≠“ρ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2)ΈΣ÷Λ ΒœύΙΊΖ÷ΈωΘ§Μ·―ß–ΓΉιΒΡΆ§―ß…ηΦΤΝΥ»γœ¬ Β―ιΘ§Ε‘ΆΥΜΊΤχΧε(X)»Γ―υΫχ––»œ’φΧΫΨΩ(”ω”–ΤχΧεΈϋ ’Ιΐ≥ΧΘ§ ”ΈΣ»ΪΈϋ ’)ΓΘ
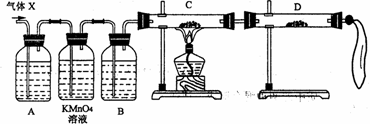
ΔΌΉιΉΑΚΟ“«ΤςΚσΘ§ ΔΖ≈“©ΤΖ«ΑΘ§±Ί“ΣΒΡ“ΜΗω≤ΌΉς «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎA÷–Φ”»κΒΡ ‘ΦΝΩ…Ρή «ΘΚΓΓ ΓΓΓΓΓΓΓΓΓΓΘ§Ής”Ο «ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
B÷–Φ”»κΒΡ ‘ΦΝΩ…Ρή «ΘΚΓΓΓΓΓΓΓΓΓΓ Θ§Ής”Ο «ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔέΩ…÷Λ ΒΤχΧεX÷–Μλ”–ΫœΕύΝΩΡ≥‘”÷ ΤχΧεΒΡ Β―ιœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3)Ε‘…œ ωΉΑ÷Ο¬‘Φ”ΗΡΫχΘ§Ω…¥÷¬‘≤βΕ®XΤχΧε÷–SO2ΒΡΧεΜΐΖ÷ ΐΓΘΗΡΫχ ±Ω…―Γ”ΟΒΡœ¬Ν–“«ΤςΈΣΓΓΓΓΓΓΓΓΓΓ (Χν¥ζΚ≈)ΓΘ
AΓΓ ΒΦΙήΓΓ BΓΓ Υ°≤έΓΓ CΓΓ ΙψΩΎΤΩΓΓ DΓΓ »ίΝΩΤΩΓΓ EΓΓ ΝΩΆ≤ ΓΓFΓΓ ΒΞΩΉ»ϊΓΓ GΓΓ ΥΪΩΉ»ϊ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com