
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
24ЃЎКЃЫЎЕФзлКЯРћгУПЩвджЦБИН№ЪєУОЃЌЦфСїГЬШчЯТЭМЫљЪОЃК

ЁЁ (1)ШєдкПеЦјжаМгШШMgCl2ЁЄ6H2OЃЌЩњГЩЕФЪЧMg(OH)ClЛђMgOЃЌаДГіЯргІЗДгІЕФЛЏбЇЗНГЬЪНЁЃЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)гУЕчНтЗЈжЦШЁН№ЪєУОЪБЃЌашвЊЮоЫЎТШЛЏУОЁЃдкИЩдяЕФHClЦјСїжаМгШШMgCl2ЁЄ6H2OЪБЃЌФмЕУЕНЮоЫЎMgCl2ЃЌЦфдвђЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ (3)Mg(OH)2ГСЕэжаЛьгаЕФCa(OH)2гІдѕбљГ§ШЅЃПаДГіЪЕбщВНжшЁЃ
ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
22ЃЎдкЪЕбщЪвРяПЩгУЯТЭМЫљЪОзАжУжЦШЁТШЫсМиЁЂДЮТШМиФЦКЭЬНОПТШЫЎЕФаджЪЁЃ
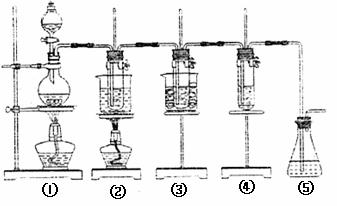
ЁЁЁЁ ЭМжаЃКЂйЮЊТШЦјЗЂЩњзАжУЃЛЂкЕФЪдЙмРяЪЂга15mL 30%KOHШмвКЃЌВЂжУгкЫЎдЁжаЃЛЂлЕФЪдЙмРяЪЂга15mL 8% NaOHШмвКЃЌВЂжУгкБљЫЎдЁжаЃЛЂмЕФЪдЙмРяМггазЯЩЋЪЏШяЪдвКЃЛЂнЮЊЮВЦјЮќЪезАжУЁЃ
ЁЁЁЁ ЧыЬюаДЯТСаПеАзЃК
ЁЁ (1)жЦШЁТШЦјЪБЃЌЯђЩеЦПжаМгШыЪЪСПХЈбЮЫсЕФВйзїЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)БШНЯжЦШЁТШЫсМиКЭДЮТШЫсФЦЕФЬѕМўЃЌЖўепЕФВювьЪЧЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁЁЁЁЁЁЁ ЗДгІЭъБЯОРфШДКѓЃЌЂкЕФЪдЙмжагаДѓСПОЇЬхЮіГіЁЃЯТЭМжаЗћКЯИУОЇЬхШмНтЖШЧњЯпЕФЪЧЁЁЁЁЁЁЁЁЁЁ (ЬюаДБрКХзжФИ)ЃЛДгЂкЕФЪдЙмжаЗжРыГіИУОЇЬхЕФЗНЗЈЪЧЁЁЁЁЁЁ (ЬюаДЪЕбщУћГЦ)ЁЃ
ЁЁ (3)БОЪЕбщжажЦШЁТШЫсМиЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (4)ЪЕбщжаПЩЙлВьЕНЂмЕФЪдЙмРяШмвКЕФбеЩЋЗЂЩњСЫШчЯТБфЛЏЃЌЧыЬюаДЯТБэжаЕФПеАзЃК
|
ЪЕбщЯжЯѓ |
двђ |
|
ШмвКГПГѕДгзЯЩЋж№НЅБфЮЊЁЁЁЁЁЁ ЩЋ |
ТШЦјгыЫЎЗДгІЩњГЩЕФH+ЪЙЪЏШяБфЩЋ |
|
ЫцКѓШмвКж№НЅБфЮЊЮоЩЋ |
ЁЁ |
|
ШЛКѓШмвКДгЮоЩЋж№НЅБфЮЊЁЁЁЁЁЁ ЩЋ |
ЁЁ |
21ЃЎФГбаОПаЁзщГЩдБдкЬжТлМјБ№ХЈСђЫсКЭЯЁСђЫсЕФЗНАИЪБЃЌЩшМЦШчЯТЗНАИЃК
|
ЁЁ |
Вйзї |
дЄВтЯжЯѓВЂзіГіНсТл |
|
Мз |
ЗжБ№НЋСђЫсЕЮдкЛ№ВёЙЃЩЯ |
БфКкепЮЊХЈСђЫс |
|
вв |
ЗжБ№МгШыаЁПщН№ЪєТСЦЌ |
ВњЩњДЬМЄадЦјЮЖепЮЊХЈСђЫс |
|
Бћ |
ЗжБ№МгШыЕНЪЂЫЎЕФЪдЙмжа |
ЗХШШепЮЊХЈСђЫс |
|
ЖЁ |
ЗжБ№гУВЃСЇАєеКХЈАБЫЎППНќЫсЕФЦППк |
УААзбЬепЮЊХЈСђЫс |
|
Юь |
ЗжБ№МгЕНCuSO4ЁЄ5H2OОЇЬхжа |
ОЇЬхБэУцгЩРЖБфАзепЮЊХЈСђЫс |
ЁЁ (1)ЦфжаПЩааЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)ЦфжавЛИіЩдзїИФНјОЭФмГЩЮЊПЩааЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌИФНјЗНЗЈЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (3)ЭъШЋДэЮѓЕФЪЧЁЁЁЁЁЁЁЁЁЁ ЃЌвђЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЃ
ЁЁ (4)гУ98%(Іб=1.84g/mL)ЕФХЈСђЫсХфжЦ4.60mol/LЕФЯЁСђЫс100mLЃЌдђгІгУСПЭВСПШЁ98%ЕФХЈСђЫсЕФЬхЛ§ЪЧЁЁЁЁЁЁЁЁЁЁ mL
20ЃЎa mol FeSгыb mol FeOЭЖШыЕНVLЁЂc molЁЄLЃ1ЕФЯѕЫсШмвКжаГфЗжЗДгІЃЌВњЩњNOЦјЬхЃЌЫљЕУГЮЧхШмвКЕФГЩЗжПЩПДзїЪЧFe(NO3)3ЁЂH2SO4ЕФЛьКЯвКЃЌдђЗДгІжаЮДБЛЛЙдЕФЯѕЫсПЩФмЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎ(a+b)ЁС63gЁЁЁЁЁЁЁЁ BЃЎ(a+b)ЁС189gЁЁЁЁЁЁЁЁ CЃЎ(a+b)molЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ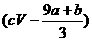 mol
mol
|
|
19ЃЎЯТСагаЙиЛЗОГЮЪЬтЕФЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎШМУКЪБМгШыЪЪСПЪЏЛвЪЏЃЌПЩМѕЩйЗЯЦјжаSO2ЕФСП
ЁЁЁЁЁЁ BЃЎГєбѕЕФЬхЛ§ЗжЪ§ГЌЙ§10Ѓ4%ЕФПеЦјгаРћгкШЫЬхНЁПЕ
ЁЁЁЁЁЁ CЃЎpHаЁгк5.6ЕФНЕЫЎЭЈГЃГЦЮЊЫсгъ
ЁЁЁЁЁЁ DЃЎКЌСзКЯГЩЯДЕгМСвзгкБЛЯИОњЗжНтЃЌЙЪВЛЛсЕМжТЫЎЬхЮлШО
18ЃЎЕШЮяжЪЕФСПЕФЯТСаЮяжЪЃКЂйNaHSO4 ЂкCa(H2PO4)2 ЂлSi ЂмAl2(SO4)3
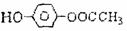 ЁЁ
ЁЁ
ЂнЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЗжБ№гызуСПЕФNaOHШмвКЗДгІЃЌКФМюзюгЩЖрЕНЩйЕФЫГађе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЂкЂнЂмЂлЂйЁЁЁЁЁЁЁЁ BЃЎЂмЂкЂлЂнЂйЁЁЁЁЁЁЁЁ CЃЎЂмЂкЂнЂлЂйЁЁЁЁЁЁЁЁ DЃЎЂмЂнЂкЂлЂй
17ЃЎИпЬњЫсМи(K2FeO4)ЪЧвЛжжаТаЭЁЂИпаЇЁЂЖрЙІФмЫЎДІРэМСЃЌЦфгыЫЎЕФРызгЗДгІЪЧЃК
4FeO2Ѓ4+10H2O = 4Fe(OH)3(НКЬх)+3O2Ёќ+8OHЃ
ЙЄвЕЩЯЯШжЦЕУИпЬњЫсФЦЃЌШЛКѓдкЕЭЮТЯТЃЌЯђИпЬњЫсФЦШмвКжаМгШывЛЖЈСПЕФKOHОЭПЩжЦЕУИпЬњЫсМиЁЃжЦБИИпЬњЫсФЦЕФСНжжЗНЗЈЕФжївЊЗДгІдРэШчЯТЃК
ЪЊЗЈжЦБИ--2Fe(OH)3+3ClOЃ+4OHЃ= 2FeO2Ѓ4+3ClЃ+5H2O
ИЩЗЈжЦБИ--2FeSO4+6Na2O2 = 2Na2FeO4+2Na2O+2Na2SO4+O2Ёќ
ЯТСагаЙиЫЕЗЈжае§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁ AЃЎИпЬњЫсМигыЫЎЗДгІЪБЃЌЫЎЗЂЩњЛЙдЗДгІ
ЁЁЁЁ BЃЎЪЊЗЈжаУПЩњГЩ1molNa2FeO4ЙВзЊвЦ3molЕчзг
ЁЁЁЁ CЃЎИЩЗЈжаУПЩњГЩ1molNa2FeO4ЙВзЊвЦ4molЕчзг
ЁЁЁЁ DЃЎK2FeO4ДІРэЫЎЪБЃЌВЛНіФмЩБОњЃЌЛЙФмГ§ШЅH2SЁЂNH3ЕШЃЌВЂЪЙаќИЁдгжЪГСНЕ
16ЃЎгаЙиЮяжЪШМЩеЪБЛ№бцбеЩЋУшЪіДэЮѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЧтЦјдкТШЦјжаШМЩе--ВдАзЩЋЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎФЦдкПеЦјжаШМЩе--ЛЦЩЋ
ЁЁЁЁЁЁ CЃЎввДМдкПеЦјжаШМЩе--ЕРЖЩЋЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎСђдкбѕЦјжаШМЩе--ТЬЩЋ
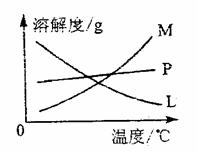
15ЃЎЭЁЂвјЁЂН№ЪЧШЫРрШЯЪЖзюдчЕФШ§жжН№ЪєЃЌвђЮЊКмдчОЭБЛШЫУЧгУзїЧЎБвЃЌвђЖјгаЁАЛѕБвН№ЪєЁБжЎГЦЁЃгЩгкЬњЕФН№ЪєадБШЭЁЂвјЁЂН№ЧПЃЌЯрЖдЖјбдЃЌШЫРрШЯЪЖЬњЩдЭэЁЃФГбаОПадбЇЯАаЁзщЮЊСЫжЄУїЬњЕФН№ЪєЛюЖЏадБШЭЧПЃЌЫћУЧЩшМЦСЫШчЯТЗНАИЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ (1)ЬњЦЌжУгкСђЫсЭШмвКжагаЭЮіГі
ЁЁ (2)ЬњЁЂЭКЭТШЦјЗДгІЗжБ№ЩњГЩFeCl3КЭCuCl2
ЁЁ (3)зуСПЕФЬњЗлКЭЭЗлКЭХЈСђЫсЗДгІЩњГЩFeSO4КЭCuSO4
ЁЁ (4)ЭЦЌжУгкFeCl3ШмвКжаЭЦЌж№НЅШмНт
ЁЁ (5)АбЬњЦЌКЭЭЦЌжУгкЪЂгаЯЁСђЫсЕФЩеБжаЃЌНЛгУЕМЯпСЌНгЃЌЬњЦЌЩЯЮоЦјХнВњЩњЃЌЖјЭЦЌЩЯгаЦјХнВњЩњ
ЁЁ (6)АбЬњЦЌКЭЭЦЌжУгкЪЂгаХЈЯѕЫсЕФЩеБжаЃЌВЂгУЕМЯпСЌНгЃЌЬњЦЌЩЯгаЦјХнВњЩњЃЌЖјЭЦЌЩЯЮоЦјХнВњЩњЁЃвдЩЯЩшМЦКЯРэЕФгаЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎСНжжЗНАИЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎШ§жжЗНАИЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЫФжжЗНАИЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЮхжжЗНАИ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com