
题目列表(包括答案和解析)
13.下列有关物质性质的比较正确的是 ( )
①同主族元素的单质从上到下,非金属性减弱,熔点增高
②元素的最高正化合价在数值上等于它所在的族序数
③同周期主族元素的原子半径越小,越难失去电子
④元素的非金属性越强,它的气态氢化物水溶液的酸性越强
⑤还原性:S2->Se2->Cl-
⑥酸性:HClO4>H2SO4>H3PO4>H2SiO3
 A.①③ B.②④
C.③⑥ D.⑤⑥
A.①③ B.②④
C.③⑥ D.⑤⑥
12.国际无机化学命名委员会在1989年做出决定,把长式元素周期表原先的主、副族及族号取消,由左至右改为第1-18列,碱金属为第1列,稀有气体为第18列。据此规定,下列说法中不正确的是 ( )
A.第15列元素的最高价氧化物为R2O5 B.第2列元素中肯定没有非金属元素
C.第17列元素的第一种元素无含氧酸 D.第16、17列元素都是非金属元素
11.Cl2通入一定量浓KOH溶液中,完全参与反应后经测定体积分数为a的氯气被氧化。若溶液中含有Cl-、ClO-、ClO3-,且c(Cl-)与c(ClO3-)之比为6∶1,则a为( )
A.0.25 B.0.50 C.0.75 D.0.80
10.对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:
1lP+15CuS04+24H20=5Cu3P+6H3P04+15H2S04下列关于该反应说法正确的是 ( )
A.CuS04发生了氧化反应 B.生成1 mol H3P04时,有10 mol电子转移
C.氧化产物和还原产物的物质的量之比为6:5
D.白磷只作还原剂
9.已知反应:①Cl2+2KBr=2KCl+Br2, ②KClO3 +6HCl=3Cl2+KCl +3H2O,
③2KBrO3 +Cl2=Br2 + 2KClO3,下列说法正确的是( )
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C.反应②中还原剂与氧化剂的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为5mol
8.下列不存在丁达尔效应的分散系是①有尘埃的空气、②溴水、③蒸馏水、④沸水中加几滴FeCl3浓溶液、⑤淀粉溶液( )
A.② B.②③⑤ C.②③ D.①②③⑤
7.用密度为ρ1g/cm3,质量分数是ω的浓盐酸,配制成体积比为1:4的稀盐酸,密度为ρ2g/cm3,则所配制稀盐酸的物质的量浓度为( )
A.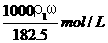 B.
B.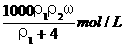
C.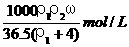 D.
D.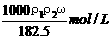
6.下列反应的离子方程式正确的是 ( )
A.向硅酸钠溶液中通入过量的二氧化碳气体:
SiO32―+H2O+CO2=H2SiO3↓+CO32―
B.氟气和水反应: 2F2+2H2O===4H++4F-+O2
C.向澄清石灰水中加入少量小苏打溶液:
Ca2++OH-+HCO3-===CaCO3↓+H2O
D.向明矾溶液中加入Ba(OH)2溶液至A13+刚好完全沉淀:
Al3++ SO42-+3OH-+Ba2+===BaSO4↓+ A1(OH)3↓
5.某溶液能使红色的石蕊试纸先变蓝色后褪色,则该溶液中可能大量共存的离子组是 ( )
A.K+、I-、AlO2-、HCO3-、MnO4- B.Na+、S2- 、NO3-、SO32-、SO42-
C.Fe2+、Al3+、NH4+、NO3-、F- D.K+、Na+、Cl-、ClO-、CO32-
4.下列各组离子中,在碱性溶液中共存,且加入盐酸过程中会产生气体和沉淀( )
A、Na+ NO3- AlO2- SO42- B、Na+ NO3- SO42- K+
C、K+ Cl- AlO2- CO32- D、Na+ Cl- HCO3- Ca2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com