
题目列表(包括答案和解析)
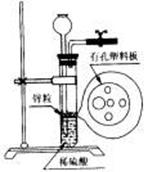
4.右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
 ①食盐水
②KNO3溶液 ③适量稀硫酸铜溶液 ④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
①食盐水
②KNO3溶液 ③适量稀硫酸铜溶液 ④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
A.①③⑤
B.①②⑥
C.①②⑤
D.①②④
3.下列各组物质的分类正确的是 ( )
A.同位素:H、D、T
B.非极性分子:C60、CO2、CH2C12
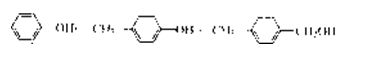 C.电解质:H2O、CH3CH2OH、NH4HCO3
C.电解质:H2O、CH3CH2OH、NH4HCO3
D.同系物:
2.将NH3气体通入饱和食盐水中,没有沉淀生成,再通入适量CO2有晶体析出,该晶体是( )
A.Na2CO3 B.NaHCO3 C.NaCl D.NaOH
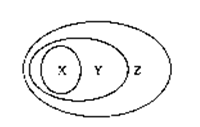
1.用右图表示的一些物质或概念之间的从属或包含关系中不正确的是( )
|
|
X |
Y |
 Z Z |
|
例 |
氧化物 |
化合物 |
纯净物 |
|
A |
苯 |
芳香烃 |
有机化合物 |
|
B |
溶液 |
分散系 |
混合物 |
|
C |
强电解质 |
电解质 |
化合物 |
|
D |
置换反应 |
氧化还原反应 |
离子反应 |
26.(16分)铝土矿(主要成分为Al2O3、SiO2、Fe2O3)是提取氧化铝的原料。提取氧化铝的工艺流程
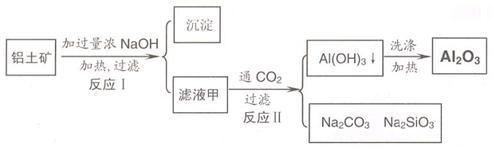 如下:
如下:
(1)滤液甲的主要成分是(写化学式)
(2)写出反应 II 的离子方程式:
(3)结合反应II,判断下列微粒结合质子 ( H+) 的能力,由强到弱的顺序是
(填字母序号)
a.AlO2― 或 [Al(OH)4]- b.OH― c.SiO32―
(4)取滤液甲少许,加入过量盐酸,过滤;再用惰性电极电解其滤液,两极均有气体产生,且全部逸出,在阴极区还有沉淀生成,最后沉淀消失。沉淀消失的原因可用离子方程式表示为:
(5)取 (4) 电解以后的溶液 10.0 mL,经分析,该溶液中只含有两种等物质的量浓度的碱性溶质,向其中逐滴加入0.100 mol• L-1 盐酸溶液,当加入50.0mL 盐酸溶液时,生成的沉淀恰好溶解。
①加入50.0mL 盐酸溶液发生的离子反应的先后顺序依次为:
。
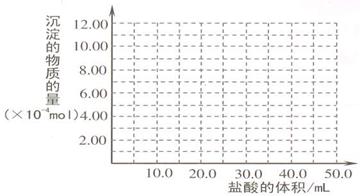 ②请画出生成沉淀的物质的量与加入盐酸体积的关系图。
②请画出生成沉淀的物质的量与加入盐酸体积的关系图。
25.(10分)在一定量的石灰乳中通入一定量
的氯气,二者恰好完全反应(发生的反应
 均为放热反应)。生成物中含有Cl-、C1O-、
均为放热反应)。生成物中含有Cl-、C1O-、
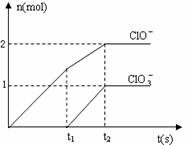
C1O3-三种含氯元素的离子,其中C1O-、
C1O3-两种离子的物质的量(n)与反应时
间(t)的曲线如右图所示。
(1)t2时,Ca(OH)2与Cl2发生反应的总的化
学方程式为:______________________ 。
(2)该石灰乳中含有Ca(OH)2的物质的量是______ mol。
(3)据分析,生成Ca(C1O3)2的反应是由温度升高引起的,通入Cl2的速度不同,C1O-和C1O3-的比例也不同。
若在原石灰乳中通入氯气的速度加快,则反应后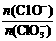 2(填“>”、“<”或“=”);
2(填“>”、“<”或“=”);
若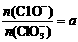 ,则n(C1-)= mol(用含a的代数式来表示)。
,则n(C1-)= mol(用含a的代数式来表示)。
24.(9分)铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4·5H2O呈蓝色等。研究性学习小组甲为检测实验室的Cu2O试样中是否含有Cu进行了认真的探究。
Ⅰ.查阅资料:①Cu2O属于碱性氧化物; ②在空气中灼烧Cu2O生成CuO;③Cu2O在酸性条件下能发生自身氧化还原反应(Cu2O+2H+=Cu+Cu2++H2O)。
Ⅱ.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察是否有残渣
方案3:称得干燥坩埚的质量为a g ,取红色试样置于坩埚中称得总质量为b g,在空气中充分灼烧至完全变黑,并在干燥器中冷却,再称量。如此反复多次直到质量不变,称得最后质量为c g。分析数据,作出合理判断。
(1)请你评价方案1和方案2。如果你认为该方案合理,请简述其工作原理;如果你认为该方案不合理,请简述原因。
(2)方案3中,如果a、b、c的关系符合c= 可确认红色粉末是Cu2O。
23. (12分) 已知SiO2、SO2、CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性(提示:2Mg+CO2====2MgO+C)
(12分) 已知SiO2、SO2、CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性(提示:2Mg+CO2====2MgO+C)
 Ⅰ、用如图所示的装置进行Mg和SO2的实验:
Ⅰ、用如图所示的装置进行Mg和SO2的实验:
(1)选择制取SO2的合适试剂 。
①10%的H2SO4溶液;
②80%的H2SO4溶液;
③Na2SO3固体;
④CaSO3固体
(2)写出装置B中发生的主要反应的化学方
程式:
(3)你认为该装置是否有不足之处? ,如果有,请列出两点:
。
Ⅱ、某研究性学习小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料后得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si; ②Mg在高温的条件下即可与SiO2反应;
③金属硅化物与稀H2SO4反应生成硫酸盐和SiH4;④Si和SiO2均不与稀H2SO4反应; ⑤SiH4在空气中自燃。
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀H2SO4溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀H2SO4溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制“Si”的化学方程式是
(5)你估计“用稀H2SO4溶解固体产物时,发现有爆鸣声和火花”的原因是
22.(10分)某同学利用铁与水蒸气反应后的固体物质进行了如下实验:

(1)固体溶于稀盐酸的化学方程式为 。
(2)试剂1的化学式是 。
(3)加入新制氯水后溶液红色加深的原因是(用离子方程式表示):
(4)某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设:
假设1:溶液中的+3价铁被氧化为更高的价态;
假设2: ;
②设计方案:
为了对你所提出的假设2进行验证,你设计的实验方案是
。
21.(8分)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一氧化还原反应的体系中,共有KCl、Cl2、浓H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
(1)该氧化还原反应的体系中,还原剂是______,化合价没有发生变化的反应物是___ 。
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平):
________________________________________________________。
(3)上述反应中,1 mol氧化剂在反应中转移的电子为_______ mol。
(4)如果在反应后的溶液中加入NaBiO3,溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。证明NaBiO3的一个性质是:_______________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com