
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
1£®ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡(¡¡¡¡ )
A£®¸Õ¸Õ½áÊøµÄ¸ç±¾¹þ¸ùÆøºò·å»á£¬Ö÷ÌâÊǵÍ̼¸ÅÄî
B£®ËáÓêÇÖÊ´½¨ÖþÎֻ·¢ÉúÁËÎïÀí±ä»¯
C£®ËÜÁÏ´ü¡¢·ÏÖ½µÈÊôÓÚÎÞ»ú»¯ºÏÎï¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
D£®Éúʯ»ÒÓöË®³ÉΪÊìʯ»Ò£¬ÊÇCaO±ä³ÉÁËCaCO3
2£®(14·Ö)ijѧϰС×é̽¾¿Å¨¡¢Ï¡ÏõËáÑõ»¯ÐÔµÄÏà¶ÔÇ¿Èõ£¬°´ÏÂͼװÖýøÐÐʵÑé(¼Ð³ÖÒÇÆ÷ÒÑÂÔÈ¥)¡£ÊµÑé±íÃ÷ŨÏõËáÄܽ«NOÑõ»¯³ÉNO2£¬¶øÏ¡ÏõËá²»ÄÜÑõ»¯NO¡£Óɴ˵óöµÄ½áÂÛÊÇŨÏõËáµÄÑõ»¯ÐÔÇ¿ÓÚÏ¡ÏõËá¡£

¿ÉÑ¡Ò©Æ·£ºÅ¨ÏõËá¡¢3 mol£¯LÏ¡ÏõËá¡¢ÕôÁóË®¡¢Å¨ÁòËá¡¢ÇâÑõ»¯ÄÆÈÜÒº¼°¶þÑõ»¯Ì¼
ÒÑÖª£ºÇâÑõ»¯ÄÆÈÜÒº²»ÓëNO·´Ó¦£¬ÄÜÓëNO2·´Ó¦¡£
¡¡¡¡ 2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)ʵÑéÓ¦±ÜÃâÓк¦ÆøÌåÅŷŵ½¿ÕÆøÖС£×°Öâۡ¢¢Ü¡¢¢ÞÖÐÊ¢·ÅµÄÒ©Æ·ÒÀ´ÎÊÇ
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)µÎ¼ÓŨÏõËá֮ǰµÄ²Ù×÷ÊǼìÑé×°ÖõÄÆøÃÜÐÔ£¬¼ÓÈëÒ©Æ·£¬´ò¿ªµ¯»É¼Ðºó
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)×°ÖâÙÖз¢Éú·´Ó¦µÄ»¯Ñ§·½³ÌʽÊÇ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
(4)×°ÖâڵÄ×÷ÓÃÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £¬·¢Éú·´Ó¦µÄ»¯Ñ§·½³ÌʽÊÇ
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(5)¸ÃС×éµÃ³öµÄ½áÂÛËùÒÀ¾ÝµÄʵÑéÏÖÏóÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(6)ʵÑé½áÊøºó£¬Í¬Ñ§ÃÇ·¢ÏÖ×°ÖâÙÖÐÈÜÒº³ÊÂÌÉ«£¬¶ø²»ÏÔÀ¶É«¡£¼×ͬѧÈÏΪÊǸÃÈÜÒºÖÐÏõËá͵ÄÖÊÁ¿·ÖÊý½Ï¸ßËùÖ£¬¶øÒÒͬѧÈÏΪÊǸÃÈÜÒºÖÐÈܽâÁËÉú³ÉµÄÆøÌ塣ͬѧÃÇ·Ö±ðÉè¼ÆÁËÒÔÏÂ4¸öʵÑéÀ´ÅжÏÁ½ÖÖ¿´·¨ÊÇ·ñÕýÈ·¡£ÕâЩ·½°¸ÖпÉÐеÄÊÇ(Ñ¡ÌîÐòºÅ×Öĸ)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
a£®¼ÓÈȸÃÂÌÉ«ÈÜÒº£¬¹Û²ìÑÕÉ«±ä»¯
b£®¼ÓˮϡÊ͸ÃÂÌÉ«ÈÜÒº£¬¹Û²ìÑÕÉ«±ä»¯
c£®Ïò¸ÃÂÌÉ«ÈÜÒºÖÐͨÈ뵪Æø£¬¹Û²ìÑÕÉ«±ä»¯
d£®Ïò±¥ºÍÏõËáÍÈÜÒºÖÐͨÈËŨÏõËáÓëÍ·´Ó¦²úÉúµÄÆøÌ壬¹Û²ìÑÕÉ«±ä»¯
Ìì½òÊкÍƽÇø09-10ѧÄê¸ßÒ»ÉÏѧÆÚ»¯Ñ§ÆÚÄ©ÊÔ¾í
1£® (6·Ö)
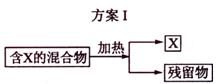
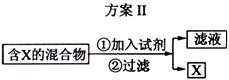
ÏÂͼ±íʾ´Ó¹ÌÌå»ìºÏÎïÖзÖÀëXµÄ2ÖÖ·½°¸£¬Çë»Ø´ðÓйØÎÊÌâ¡£
 ¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡ 
(1)Ñ¡Ó÷½°¸Iʱ£¬XÓ¦¸Ã¾ßÓеÄÐÔÖÊÊÇ¡¡¡¡¡¡¡¡¡¡ £¬²ÐÁôÎïÓ¦¸Ã¾ßÓеÄÐÔÖÊÊÇ¡¡¡¡¡¡¡¡¡¡ £»
(2)ΪÌᴿijFe2O3ÑùÆ·(Ö÷ÒªÔÓÖÊÓÐSiO2¡¢A12O3)£¬Éè¼Æ·½°¸ÈçÏ£¬ÇëÌîдA¡¢B¡¢C¡¢DÖк¬ÓеÄÎïÖʵĻ¯Ñ§Ê½A¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¢B ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¢C¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¢D¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£

29£® ÏòVmLº¬ÓÐ0.26nolµÄÏõËáÈÜÒºÖмÓÈë3.2gCu·Û£¬¼ÙÉèHNO3µÄ»¹Ô²úÎïÖ»ÓÐNO2ºÍNO¡£·´Ó¦½áÊøºó£¬½«ÈÜÒº¼ÓˮϡÊÍÖÁ1000mL¡£²âµÃc(NO3-)=0.2mol¡¤L-1¡£Ôò
(1)Ï¡ÊͺóµÄÈÜÒºÖÐHNO3µÄÎïÖʵÄÁ¿µÄŨ¶ÈΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)±»»¹ÔµÄÏõËáµÃµ½µÄµç×ÓµÄÎïÖʵÄÁ¿Îª¡¡¡¡¡¡¡¡¡¡¡¡¡¡ mol¡£
¸½¼ÓÌâ
28£®¢¡.(11·Ö)ʵÑéÊÒÖƱ¸ÉÙÁ¿ÁòËáÑÇÌúÆ·ÌåµÄʵÑé²½ÖèÈçÏ£ºÈ¡¹ýÁ¿½à¾»µÄÌúм£¬¼ÓÈë20%%-30%µÄÏ¡ÁòËáÈÜÒº£¬ÔÚ50¡æ-80¡æˮԡÖмÓÈÈÖÁ²»ÔÙ²úÉúÆøÅÝ¡£½«ÈÜÒº³ÃÈȹýÂË£¬ÂËÒºÒÆÖÁÊÔ¹ÜÖУ¬ÓÃÏð½ºÈûÈû½ôÊԹܿڣ®¾²Öá¢ÀäÈ´Ò»¶Îʱ¼äºóÊÕ¼¯²úÆ·£®
(1)д³ö¸ÃʵÑéÖƱ¸ÁòËáÑÇÌúµÄ»¯Ñ§·½³Ìʽ£º____________________________________¡£
(2)²ÉÓÃˮԡ¼ÓÈȵÄÔÒòÊÇ____________________________________________________¡£
(3)·´Ó¦Ê±Ìúм¹ýÁ¿µÄÄ¿µÄÊÇ(ÓÃÀë×Ó·½³Ìʽ±íʾ)______________________________¡£
(4)ÈÜÒº³ÃÈȹýÂ˵ÄÔÒòÊÇ____________________________________________________¡£
Èû½ôÊԹܿڵÄÄ¿µÄÊÇ______________________________________________________¡£
(5)¾²ÖÃÀäÈ´Ò»¶Îʱ¼äºó£¬ÔÚÊÔ¹ÜÖй۲쵽µÄÏÖÏóÊÇ______________________________¡£
¢¢. 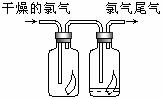 (1)ÈçͼËùʾ£¬½«ÂÈÆøÒÀ´Îͨ¹ýÊ¢ÓиÉÔïÓÐÉ«²¼ÌõµÄ¹ã¿ÚÆ¿ºÍ
(1)ÈçͼËùʾ£¬½«ÂÈÆøÒÀ´Îͨ¹ýÊ¢ÓиÉÔïÓÐÉ«²¼ÌõµÄ¹ã¿ÚÆ¿ºÍ
Ê¢Óг±ÊªÓÐÉ«²¼ÌõµÄ¹ã¿ÚÆ¿£¬¿É¹Û²ìµ½µÄÏÖÏóÊÇ£º
_______¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ _________________________¡£
(2)Ϊ·ÀÖ¹ÂÈÆøβÆøÎÛȾ¿ÕÆø£¬¸ù¾ÝÂÈË®ÏÔËáÐÔµÄÐÔÖÊ£¬¡¡
¿ÉÓÃNaOHÈÜÒºÎüÊÕ¶àÓàµÄÂÈÆø£¬ÔÀíÊÇ(Óû¯Ñ§·½³Ìʽ
±íʾ)_________________________________¡£¸ù¾ÝÕâÒ»ÔÀí£¬¹¤ÒµÉϳ£ÓÃÁ®¼ÛµÄʯ»ÒÈéÎüÊÕ¹¤ÒµÂÈÆøβÆøÖƵÃƯ°×·Û£¬Æ¯°×·ÛµÄÓÐЧ³É·ÖÊÇ__________(Ìѧʽ),³¤ÆÚ¶ÖÃÓÚ¿ÕÆøÖеÄƯ°×·Û£¬¼ÓÏ¡ÑÎËáºó²úÉúµÄÆøÌåÊÇ__________(ÓÃ×Öĸ´úºÅÌî)¡£
A£®O2¡¡¡¡¡¡ B£®Cl2¡¡¡¡¡¡ C£®CO2¡¡¡¡¡¡ D£®HClO
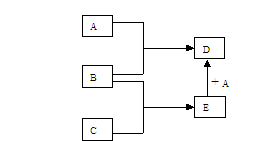
27£®(14·Ö)ÒÑÖªA¡¢B¡¢C¡¢D¡¢E¾ùΪÖÐѧ»¯Ñ§Öг£¼ûÎïÖÊ£¬ÔÚÒ»¶¨Ìõ¼þÏÂÏ໥ת»¯¹ØϵÈçÏÂͼËùʾ(·´Ó¦Ìõ¼þºÍ²¿·Ö²úÎïÒÑÊ¡ÂÔ)¡£
¡¡ Çë»Ø´ð£º
¡¡ (1)ÈôAΪ½ðÊôµ¥ÖÊ£¬B¡¢CΪ·Ç½ðÊôµ¥ÖÊ£¬ÇÒ³£ÎÂÏÂB¡¢C¾ùΪÎÞÉ«ÆøÌ壬DΪºÚÉ«¹ÌÌ壬ÔòBµÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡¡¡ £¬AÓëEÔÚÒ»¶¨Ìõ¼þÏ·´Ó¦Éú³ÉDµÄ»¯Ñ§·½³ÌʽΪ
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)ÈôAΪ·Ç½ðÊôµ¥ÖÊ£¬ÇÒ³£ÎÂÏÂΪ»ÆÂÌÉ«ÆøÌ壬BΪ½ðÊôµ¥ÖÊ£¬CΪËᣬÇÒCµÄ×é³ÉÖк¬ÓÐÓëAÏàͬµÄÔªËØ¡£ÔòCµÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡¡¡ £¬½«ÉÙÁ¿µ¥ÖÊAͨÈëÊ¢Óеí·ÛKIÈÜÒºµÄÊÔ¹ÜÖУ¬ÒºÌå±äΪÀ¶É«¡£¸Ã·´Ó¦µÄÀë×Ó·½³ÌʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£Õâ˵Ã÷µ¥ÖÊAµÄÑõ»¯ÐÔ¡¡¡¡¡¡¡¡ ÓÚµ¥Öʵâ(Ìî¡°Ç¿¡±»ò¡°Èõ¡±)¡£AÓëEÔÚÒ»¶¨Ìõ¼þÏ·´Ó¦Éú³ÉDµÄÀë×Ó·½³ÌʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)ÏòEÈÜÒºÖеÎÈëNaOHÈÜҺʱ£¬Éú³ÉµÄ»Ò°×É«³ÁµíѸËÙ±ä³É»ÒÂÌÉ«£¬×îºó±ä³ÉºìºÖÉ«¡£Ð´³ö³ÁµíÓɻҰ×É«±ä³ÉºìºÖÉ«µÄ»¯Ñ§·½³Ìʽ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
26£®(12·Ö)
¢¡.ij´ý²âÒºÖпÉÄܺ¬ÓÐAg+¡¢Fe3+¡¢K+¡¢Ba2+¡¢NH4+µÈÀë×Ó£¬½øÐÐÈçÏÂʵÑ飺
¢Ù¼ÓÈë¹ýÁ¿µÄÏ¡ÑÎËᣬÓа×É«³ÁµíÉú³É¡£
¢Ú¹ýÂË£¬ÔÚÂËÒºÖмÓÈë¹ýÁ¿µÄÏ¡ÁòËᣬÓÖÓа×É«³ÁµíÉú³É¡£
¢Û¹ýÂË£¬È¡ÉÙÁ¿ÂËÒº£¬µÎÈë2µÎKSCNÈÜÒº£¬Ã»ÓÐÃ÷ÏÔµÄÏÖÏó³öÏÖ¡£
¢ÜÁíÈ¡ÉÙÁ¿²½Öè(3)ÖеÄÂËÒº£¬¼ÓÈëNaOHÈÜÒºÖÁʹÈÜÒº³Ê¼îÐÔ£¬¼ÓÈÈ£¬¿É²úÉúʹ
ʪÈóµÄºìɫʯÈïÊÔÖ½±äÀ¶É«µÄÆøÌå¡£
¢Å¸ù¾ÝʵÑéÏÖÏó»Ø´ð£º´ý²âÒºÖÐÒ»¶¨º¬ÓС¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ Àë×Ó£¬Ò»¶¨²»º¬ÓÐ__________Àë×Ó£¬»¹ÓÐÒ»ÖÖÀë×Ó²»ÄÜÈ·¶¨ÊÇ·ñ´æÔÚ£¬Òª¼ìÑéÕâÖÖÀë×ÓµÄʵÑé·½·¨ÊÇ(ÌîдʵÑéÃû³ÆºÍ¹Û²ìµ½µÄÏÖÏ󣬲»ÒªÇóдʵÑé²Ù×÷¹ý³Ì)¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
¢Æд³ö¢ÜÖз¢Éú·´Ó¦µÄÀë×Ó·½³Ìʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
¢¢. ÄƺÍÂÁÊÇÁ½ÖÖÖØÒªµÄ½ðÊô¡£Çë»Ø´ð£º
(1)ÄÆÔªËصĽðÊôÐÔ±ÈÂÁµÄ_________(Ìî¡°Ç¿¡±»ò¡°Èõ¡±)£»³£ÎÂÏ£¬¿ÉÓÃ_________(Ìî¡°ÄÆ¡±»ò¡°ÂÁ¡±)ÖƳɵÄÈÝÆ÷ʢװŨÁòËá»òŨÏõËá¡£
(2)½«Ò»Ð¡¿é½ðÊôÄÆͶÈëË®ÖУ¬·¢Éú·´Ó¦µÄ»¯Ñ§·½³ÌʽΪ¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡£»
¡¡(3)ÂÁÓëÇâÑõ»¯ÄÆÈÜÒº·´Ó¦µÄÀë×Ó·½³ÌʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
25£®ÔÚaLAl2(SO4)3ºÍ(NH4)2SO4µÄ»ìºÏÈÜÒºÖмÓÈëbmolBaCl2ÈÜÒº£¬Ç¡ºÃʹÈÜÒºÖеÄSO42-ÍêÈ«³Áµí£»Èç¼ÓÈë×ãÁ¿Ç¿¼î²¢¼ÓÈȿɵõ½cmolNH3£¬ÔòÔ»ìºÏÈËÔ±ÖеÄAl3+µÄÎïÖʵÄÁ¿µÄŨ¶ÈΪ(¡¡¡¡¡¡ )
A.2b-c/2a¡¡¡¡¡¡ B. 2b-c/a¡¡¡¡¡¡ C. 2b-c/3a¡¡¡¡¡¡¡¡ D. 2b-c/6a
Ç뽫ѡÔñÌâµÄ´ð°¸ÌîдÔÚÒÔϱí¸ñ£º(±íÒ»)
±í¶þ£º
µÚ¢ò¾í¡¡ ·ÇÑ¡ÔñÌâ(¹²50·Ö)
23£®Ä³ÈÜÒºÖÐÓÐNa+¡¢Mg2+¡¢Fe2+ºÍAl3+ËÄÖÖÑôÀë×Ó£¬ÈôÏòÆäÖмÓÈë¹ýÁ¿µÄÇâÑõ»¯ÄÆÈÜÒº£¬Î¢ÈȲ¢²»¶Ï½Á°è£¬ÔÙ¼ÓÈë¹ýÁ¿ÑÎËᣬÈÜÒºÖдóÁ¿¼õÉÙµÄÑôÀë×ÓÊÇ(¡¡¡¡¡¡ ¡¡)
A. Na+¡¡¡¡¡¡¡¡ B. Mg2+¡¡¡¡¡¡¡¡ C. Fe2+¡¡¡¡¡¡¡¡ D. Al3+
24ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ(Éè°¢·ü¼ÓµÂÂÞ³£ÊýµÄÊýֵΪ6.02¡Á1023) (¡¡¡¡¡¡ ¡¡)
¡¡ A£®ÔÚ±ê×¼×´¿öÏ£¬22.4LË®Ëùº¬·Ö×ÓÊýĿΪ6.02¡Á1023
¡¡ B£®1mol/LK2SO4ÈÜÒºËùº¬K+ÊýĿΪ2¡Á6.02¡Á1023
¡¡ C£®ÔÚ³£Î³£Ñ¹Ï£¬16gO2ºÍO3µÄ»ìºÏÆøÌåËùº¬Ô×ÓÊýĿΪ6.02¡Á1023
¡¡ D£®2.4gMgÓë×ãÁ¿ÑÎËáÍêÈ«·´Ó¦Ê±£¬Ê§È¥µç×ÓÊýĿΪ0.1¡Á6.02¡Á1023
22£®ÏÂÁÐʵÑé·½·¨ºÏÀíµÄÊÇ(¡¡¡¡¡¡ ¡¡)
A£®ÓÃÊÊÁ¿NaOHÈÜÒº³ýÈ¥KClÈÜÒºÖеÄÉÙÁ¿MgCl2 B£®FeCl2ÈÜÒºÖлìÓÐFeCl3ÈÜÒº¼ÓÈë×ãÁ¿Ìú·Û
C£®ÓóÎÇåʯ»ÒË®¼ø±ðNa2CO3¡¢NaHCO3Á½ÖÖÈÜÒº D£®Í¨¹ýÊ¢Óб¥ºÍNa2CO3ÈÜÒºµÄÏ´ÆøÆ¿³ýÈ¥CO2ÖÐÉÙÁ¿µÄHCl
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com