
题目列表(包括答案和解析)
(1)下列仪器或装置在使用前一定要检查气密性的是__________(填序号,下同)。
A.容量瓶 B.洗气瓶
C.分液漏斗 D.酸(碱)式滴定管
(2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是__________。
A.收集不到气体 B.造成环境污染
C.观察到的实验现象有误 D.引发爆炸事故
(3)为检查下图所示简易气体发生装置的气密性,甲、乙两位同学进行了以下操作和方案设计。

①甲同学认为,只要往漏斗中加水,便可检验其气密性是否良好。经检验他的方案可行。则甲同学的操作方法、现象和结论是____________________________________。
②乙同学设计的方案是:往漏斗中注入一定量的水至浸没长颈漏头下端。
关闭活塞,用手捂住试管中上部,待漏斗中液面上升一定高度,打开活塞让液面回落后,迅速关闭活塞,松开手,见漏斗中液面低于试管中液面且不再升降,说明气密性良好。乙同学设计方案的原理是______________________________________________________________。
用图示装置制取PCl3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃)。已知:PCl3和 PCl5遇水强烈反应,它们熔沸点数据如下:
| | 熔点 | 沸点 |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |

 ,则F中盛有 ,作用是______________________。
,则F中盛有 ,作用是______________________。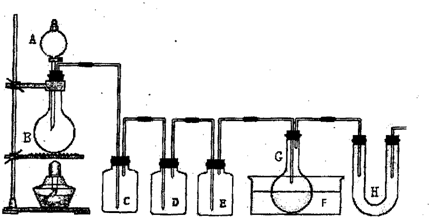
| 熔点 | 沸点 | |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |

| 熔点 | 沸点 | |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |
用图示装置制取PCl3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃)。已知:PCl3和 PCl5遇水强烈反应,
 它们熔沸点数据如下:
它们熔沸点数据如下:
| 熔点 | 沸点 | |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |
|
| ||||||
| |||||||
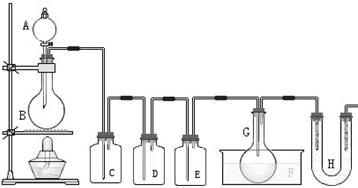
请根据图中装置回答下列问题:
(1)检查该装置气密性的方法是 。
(2)为得到氯气,若B中加入MnO2,则A中应加入 ,反应的化学方程式为___________________________________ 。
(3)若发现C中气泡产生过猛,需要进行的操作或对装置进行的改进是 。
(4)在反应开始时主要生成PCl3,而后来主要生成PCl5,原因可能是 ;从PCl3和PCl5的混合物中分离出PCl3的方法是 (选填序号)。
a.蒸馏 b.过滤 c.分液 d.升华
(5)生成的PCl3在G中收集,则F中盛有 ,作用是___________________________。
(6)C、D、H所盛的试剂分别是(选填序号):C ; D ; H 。
a.饱和食盐水 b.浓硫酸 c.无水氯化钙 d.碱石灰
(7)如果E中反应放热较多,G处的导管可能发生堵塞,其原因是 。
命题人:李孝平 审题人:李白仲
一、二选择题:(1―10题每题2分,11-18每题3分,共44分)
题 号
1
2
3
4
5
6
7
8
9
10
答 案
B
D
A
B
D
C
C
B
B
C
题 号
11
12
13
14
15
16
17
18
答 案
D
B
B
C
C
D
A
A
三、填空题:(本题共5小题,共46分)
19、①、③、⑧; ②、④; ⑤; ⑥、⑦;(每空1分)
20、(1) 略 3分 ;(2)略 4分
(3)c3>c1>c2;CH3COOH; D。(各2分)
21、(1)、4;(2分) (2)、大于(1分);因为升温水的电离平衡右移,离子浓度增大,Kw增大;(2分)
22、(1)H-O-O-H(2分) (2)N2H4(l)+H2O2(l) == N2(g) +2H2O(l) △H=-644.25 KJ/mol(3分)(3)产物不会造成环境污染。(1分)
23、(10分)(1)1 (2分) (2)否、(2分) 大于(1分) 因为
试卷.files/image027.gif)
试卷.files/image029.jpg)
试卷.files/image031.jpg)
= = <K平衡向右移动(3分)
(3)增大 减小(各1分)
24、(1)加快 (2)D (3)40% 试卷.files/image033.gif) L (各2分)
L (各2分)
25、(10分)⑴、反应产生气泡快慢或反应完成的先后或试管壁的冷热程度 ;
控制阴离子相同,排除阴离子的干扰 ; 将FeCl3改为Fe2(SO4)3
⑵、关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 一定时间内收集到的气体体积或收集一定体积的气体所需要的时间 ( 合理答案同样给分) 各2分
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com