
题目列表(包括答案和解析)
(本题共15分)空气中CO2浓度的持续走高引起人们的高度重视。一些科学家认为,人类不仅要努力减少CO2的排放,还要尽快想办法清除空气中过多的CO2。为此,他们设想了一系列“捕捉”和“封存” CO2的方法。
【小题1】方法Ⅰ:一些科学家利用太阳能加热的反应器“捕捉”空气中的CO2,如下图所示。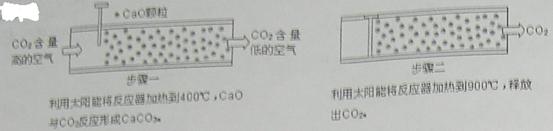
(1)步骤一中的CaO俗称 。
(2)步骤二中发生反应的化学方程式是 ,该反应 (填“是”或“不是”)步骤一中反应的逆反应。
【小题2】方法Ⅱ:另一些科学家利用NaOH溶液的喷淋“捕捉”空气中的CO2,如右图所示。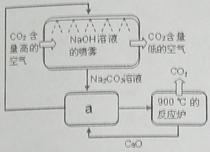
(1)NaOH溶液喷成雾状是为了 。
(2)右图a环节中,物质分离的基本操作是 。
(3)为了尽量减少成本,在整个流程中,循环利用的物质有CaO和 。
【小题3】下列溶液中,同样能用于“捕捉”二氧化碳的是( )。
| A.KNO3溶液 | B.CaCl2溶液 | C.CuSO4溶液 | D.Na2CO3溶液 |
| A.①③ | B.①② | C.②④ | D.③④ |
(本题共15分)空气中CO2浓度的持续走高引起人们的高度重视。一些科学家认为,人类不仅要努力减少CO2的排放,还要尽快想办法清除空气中过多的CO2。为此,他们设想了一系列“捕捉”和“封存” CO2的方法。
1.方法Ⅰ:一些科学家利用太阳能加热的反应器“捕捉”空气中的CO2,如下图所示。
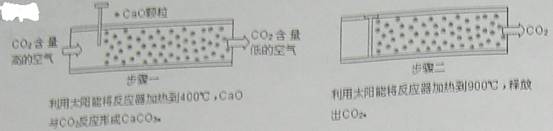
(1)步骤一中的CaO俗称 。
(2)步骤二中发生反应的化学方程式是 ,该反应 (填“是”或“不是”)步骤一中反应的逆反应。
2.方法Ⅱ:另一些科学家利用NaOH溶液的喷淋“捕捉”空气中的CO2,如右图所示。
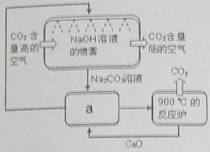
(1)NaOH溶液喷成雾状是为了 。
(2)右图a环节中,物质分离的基本操作是 。
(3)为了尽量减少成本,在整个流程中,循环利用的物质有CaO和 。
3.下列溶液中,同样能用于“捕捉”二氧化碳的是( )。
A.KNO3溶液 B.CaCl2溶液 C.CuSO4溶液 D.Na2CO3溶液
4.研究发现,上述两种方法虽然在化学原理上都是可行的,但在实际应用中仍存在很多问题,例如:( )。
①方法Ⅰ将受到地域的限制
②方法Ⅱ的能耗太大
③方法Ⅰ中使用的是氧化钙颗粒而不是氧化钙粉末
④方法Ⅱ中的物质可以循环利用,但方法Ⅰ中的却不能
A.①③ B.①② C.②④ D.③④
5.“捕捉”到的二氧化碳,一部分可以用于生产;一部分则设想注入深海中“封存”起来。但过多的二氧化碳会导致海水水质的变化,最终殃及海洋生物,其原因是 (用化学方程式表示)。
可见,要真正实现“碳捕捉”和“碳封存”的设想,科学家任重而道远。
.(15分)下图中,化合物A, B,G,M, L, J 均由两种元素组成,其中A是一种无色液体, G是极易溶于水的常见气体,L分子中的电子数为18(L的相对分子量不超过34)。反应⑤是工业上制X的主要反应之一,化合物H具有强的氧化性,可由常见卤素气体与苛性钾溶液在常温下反应而制得。N的溶液呈浅绿色。(注;有些反应的水也略去)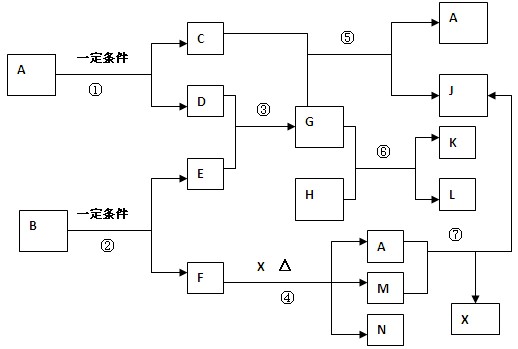
请按要求填空:
(1)写出下列物质的化学式:
L: ,X: 。
(2)反应④的离子方程式为: 。
(3)反应⑥的离子方程式为: 。
(4)略过量的H溶液与N溶液混合有大量的沉淀产生,其离子方程式为:
。
(5)B中F的质量分数为30.77%,则B的化学式为: 。
.(15分)下图中,化合物A, B,G,M, L, J 均由两种元素组成,其中A是一种无色液体, G是极易溶于水的常见气体,L分子中的电子数为18(L的相对分子量不超过34)。反应⑤是工业上制X的主要反应之一,化合物H具有强的氧化性,可由常见卤素气体与苛性钾溶液在常温下反应而制得。N的溶液呈浅绿色。(注;有些反应的水也略去)
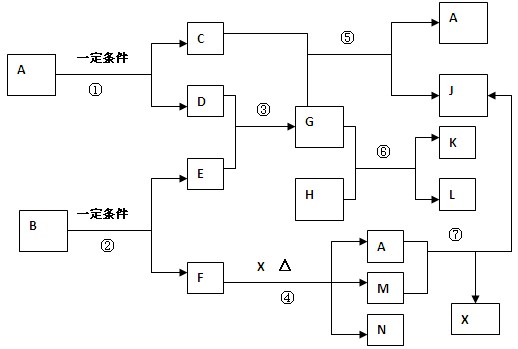
请按要求填空:
(1)写出下列物质的化学式:
L: ,X: 。
(2)反应④的离子方程式为: 。
(3)反应⑥的离子方程式为: 。
(4)略过量的H溶液与N溶液混合有大量的沉淀产生,其离子方程式为:
。
(5)B中F的质量分数为30.77%,则B的化学式为: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com