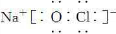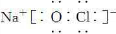(2013?红桥区一模)已知A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如下图所示(某些条件已略去).

请回答:
(1)单质B的组成元素在周期表中的位置是
第2周期第ⅤA族
第2周期第ⅤA族
.
(2)戊的化学式为
Al(OH)3
Al(OH)3
.戊与强碱反应的离子方程式:
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.
(3)NaClO的电子式为
.
(4)甲与水反应的化学方程式为
AlN+3H2O=Al(OH)3↓+NH3↑
AlN+3H2O=Al(OH)3↓+NH3↑
.
(5)反应②中,0.5molNaClO参加反应时,转移1mol电子,其化学方程式为:
2NH3+NaClO═N2H4+NaCl+H2O
2NH3+NaClO═N2H4+NaCl+H2O
.
(6)一定条件下,A与TiO
2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分.已知,该反应生成1mol乙时放出536kJ热量,其热化学方程式为:
4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1072kJ/mol
4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1072kJ/mol
.

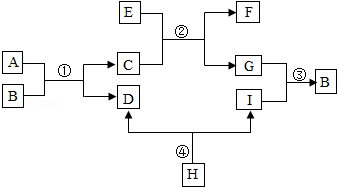 (2013?张家口一模)已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见金属,E是目前世界上产量最高的金属,G呈紫红色;I是地壳中含量最高的元素所形成的常见气体单质;人体胃液中含有A,可帮助消化.根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出)
(2013?张家口一模)已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见金属,E是目前世界上产量最高的金属,G呈紫红色;I是地壳中含量最高的元素所形成的常见气体单质;人体胃液中含有A,可帮助消化.根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出)