
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
ĻĀĮŠĻÖĻóŅņ·¢ÉśČ”“ś·“Ó¦¶ų²śÉśµÄŹĒ ( )
A£®ŅŅĻ©Ź¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«
B£®½«±½¼ÓČĖäåĖ®ÖŠ£¬Õńµ“ŗóĖ®²ć½Ó½üĪŽÉ«
C£®¼×ĶéÓėĀČĘų»ģŗĻ£¬¹āÕÕŅ»¶ĪŹ±¼äŗó»ĘĀĢÉ«ĻūŹ§
D£®ŅŅĻ©Ź¹ĖįŠŌKmnO4ČÜŅŗĶŹÉ«
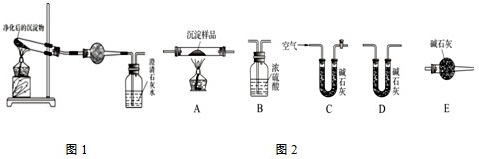
”¾½āĪö”æAÖŠŅŅĻ©ŗĶäåĖ®·¢ÉśµÄŹĒ¼Ó³É·“Ó¦£¬BÖŠŹĒŻĶČ”£¬ŹōÓŚĪļĄķ±ä»Æ”£DÖŠŹĒ±»Ńõ»Æ£¬ŹōÓŚŃõ»Æ·“Ó¦”£ĖłŅŌÕżČ·µÄ“š°øŹĒC”£
ĻĀĮŠĻÖĻóŅņ·¢ÉśČ”“ś·“Ó¦¶ų²śÉśµÄŹĒ ( )
A£®ŅŅĻ©Ź¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«
B£®½«±½¼ÓČĖäåĖ®ÖŠ£¬Õńµ“ŗóĖ®²ć½Ó½üĪŽÉ«
C£®¼×ĶéÓėĀČĘų»ģŗĻ£¬¹āÕÕŅ»¶ĪŹ±¼äŗó»ĘĀĢÉ«ĻūŹ§
D£®ŅŅĻ©Ź¹ĖįŠŌKmnO4ČÜŅŗĶŹÉ«
”¾½āĪö”æAÖŠŅŅĻ©ŗĶäåĖ®·¢ÉśµÄŹĒ¼Ó³É·“Ó¦£¬BÖŠŹĒŻĶČ”£¬ŹōÓŚĪļĄķ±ä»Æ”£DÖŠŹĒ±»Ńõ»Æ£¬ŹōÓŚŃõ»Æ·“Ó¦”£ĖłŅŌÕżČ·µÄ“š°øŹĒC”£
| 49n |
| 9m |
| 49n |
| 9m |

| ||
| ||
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com