
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
| ĪļÖŹ | NaCl | MgCl2 | AlCl3 | SiCl4 | µ„ÖŹB |
| ČŪµć/”ę | 810 | 710 | 190 | -68 | 2 300 |
| ·Šµć/”ę | 1 465 | 1 418 | 182.7 | 57 | 2 500 |
| A”¢SiCl4ŹĒ·Ö×Ó¾§Ģå |
| B”¢µ„ÖŹBŹĒŌ×Ó¾§Ģå |
| C”¢AlCl3¼ÓČČÄÜÉż»Ŗ |
| D”¢MgCl2Ėłŗ¬Ąė×Ó¼üµÄĒæ¶Č±ČNaCl“ó |
øł¾ŻĻĀĮŠ¼øÖÖĪļÖŹµÄČŪµćŗĶ·ŠµćŹż¾Ż£¬ÅŠ¶ĻĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ“ķĪóµÄŹĒ £Ø £©
| NaCl | MgCl2 | AlCl3 | SiCl4 | µ„ÖŹÅš | |
| ČŪµć£Æ”ę | 801 | 710 | 190 | ”Ŗ68 | 2 300 |
| ·Šµć£Æ”ę | 1 465 | 1 418 | 182.7 | 57 | 2 500 |
A£®SiCl4ŹĒ·Ö×Ó¾§Ģå B£®µ„ÖŹÅšŹĒŌ×Ó¾§Ģå
C£®A1C13¼ÓČČÄÜÉż»Ŗ D£®MgCl2Ėłŗ¬Ąė×Ó¼üµÄĒæ¶Č±ČNaCl“ó
A.SiCl4ŹĒ·Ö×Ó¾§Ģå B.µ„ÖŹBŹĒŌ×Ó¾§Ģå
C.AlCl3¼ÓČČÄÜÉż»Ŗ D.MgCl2Ėłŗ¬Ąė×Ó¼üµÄĒæ¶Č±ČNaCl“ó
| NaCl | MgCl2 | AlCl3 | SiCl4 | µ„ÖŹB |
ČŪµć/”ę | 810 | 710 | 190 | -68 | 2 300 |
·Šµć/”ę | 1 465 | 1 418 | 182.7 | 57 | 2 500 |
×¢£ŗAlCl3ČŪµćŌŚ2.5”Į105 PaĢõ¼žĻĀ²ā¶Ø”£
| ¾§Ģå | NaCl | MgCl2 | AlCl3 | SiCl4 | µ„ÖŹR |
| ČŪµć | 810”ę | 710”ę | 180”ę | -70”ę | 2300”ę |
| ·Šµć | 1465”ę | 1418”ę | 177.8”ę | 57”ę | 2500”ę |
| A”¢SiCl4ŹĒ·Ö×Ó¾§Ģå |
| B”¢MgCl2ÖŠ¼üµÄĒæ¶Č±ČNaClÖŠ¼üµÄĒæ¶ČŠ” |
| C”¢µ„ÖŹRŹĒŌ×Ó¾§Ģå |
| D”¢AlCl3ĪŖĄė×Ó¾§Ģå |
øł¾ŻĻĀ±ķøų³öµÄ¼øÖÖĪļÖŹµÄČŪµć”¢·ŠµćŹż¾ŻÅŠ¶ĻĖµ·ØÖŠ“ķĪóµÄŹĒ
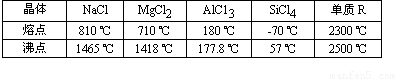
A£®SiCl4ŹĒ·Ö×Ó¾§Ģå
B£®MgCl2ÖŠ¼üµÄĒæ¶Č±ČNaClÖŠ¼üµÄĒæ¶ČŠ”
C£®µ„ÖŹRŹĒŌ×Ó¾§Ģå
D£®AlCl3ĪŖĄė×Ó¾§Ģå
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com