
题目列表(包括答案和解析)


| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
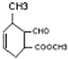

 I2+O2+H2O
I2+O2+H2O I2+O2+H2O
I2+O2+H2O


| 编号 | 反应物 | 反应前pH | 反应后pH |
| 第1组 | O3+I- | 5.2 | 11.0 |
| 第2组 | O3+I-+Fe2- | 5.2 | 4.1 |
 I2+O2+H2O可知消耗酸,所以pH升高
I2+O2+H2O可知消耗酸,所以pH升高 I2+O2+H2O可知消耗酸,所以pH升高
I2+O2+H2O可知消耗酸,所以pH升高| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液加入试管中,加入过量的2 mol?L-1盐酸,再滴加适量l mol?L-1BaCl2溶液. 取少量待测液加入试管中,加入过量的2 mol?L-1盐酸,再滴加适量l mol?L-1BaCl2溶液. |
有白色沉淀生成,证明待测液中含SO42-. |
| 步骤② | 方法1:取出步骤①中适量上层清液于试管中,加入适量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可) 方法2:另取少量待测液加入试管中,加入足量的2 mol?L-1盐酸直到不产生气泡为止,再加入少量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可) 方法1:取出步骤①中适量上层清液于试管中,加入适量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可) 方法2:另取少量待测液加入试管中,加入足量的2 mol?L-1盐酸直到不产生气泡为止,再加入少量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可) |
溶液呈橙黄色,证明待测液中含Br-.(下层液体呈橙红色,证明待测液中含Br-.) 溶液呈橙黄色,证明待测液中含Br-.(下层液体呈橙红色,证明待测液中含Br-.) |
| … |





 或
或
 或
或
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com