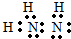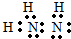(2013?资阳二模)A、B、C、D、E、F为前四周期的元素.其中,A元素和B元素的原子都有一个未成对电子,A
3+比B
-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为紫红色固体,可通过“湿法冶金”而得.请回答下列问题:
(1)CB
3分子中心原子的杂化类型是
sp3
sp3
.

(2)F元素的原子的外围电子排布式为
3d104s1
3d104s1
;如图所示为F与Au以3:1形成的合金晶胞图,在图中的括号内写出对应的元素符号.
(3)B、D元素最高价氧化物对应的水化物的酸性强弱:
HClO4>H2SO4
HClO4>H2SO4
(填化学式).
(4)用导线将A和F的单质做成的电极连接起来,插入到盛有C的最高价氧化物的水化物的浓溶液中构成原电池,试写出在单质A表面发生反应的电极反应式:
2H++NO3-+e-=NO2↑+H2O
2H++NO3-+e-=NO2↑+H2O
.
(5)分子R是由C元素与氢元素形成的18电子分子,R的电子式为
.
(6)24g E的单质在33.6L氧气(标准状况)中燃烧,至反应物全部耗尽,放出x kJ热量.则1mol E与O
2反应生成E的低价氧化物时的热化学方程式为
C(s)+
O
2(g)=CO(g)△H=-(x-y)kJ/mol
C(s)+
O
2(g)=CO(g)△H=-(x-y)kJ/mol
(已知:E的燃烧热为y kJ/mol).

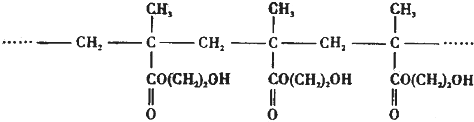
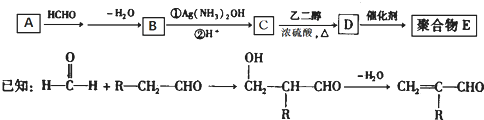
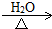 HOCH2CH2OH+2NaBr
HOCH2CH2OH+2NaBr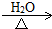 HOCH2CH2OH+2NaBr
HOCH2CH2OH+2NaBr