
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
| Β―ι≤Ϋ÷η | ‘ΛΤΎœ÷œσΚΆΫα¬έ |
| ΔΌ»ΓΆ≠”κ≈®ΝρΥαΖ¥”ΠΥυΒΟΒΡ¬Χ…Ϊ»ή“Κ”Ύ ‘Ιή÷–Θ§Εύ¥Έ’πΒ¥Θ§Ψ≤÷Ο ΔΎ»ΓΆ≠”κœΓœθΥαΖ¥”ΠΥυΒΟΒΡάΕ…Ϊ»ή“ΚΆ®NO2ΤχΧε Δέ |
»ή“Κ―’…Ϊ”…¬Χ…ΪΉΣ±δΈΣ…νάΕ…ΪΘ§÷ΛΟςΦΌ…ηΕΰ≥…ΝΔ άΕ…Ϊ»ή“Κ±δ≥…¬Χ…ΪΘ§÷ΛΟςΦΌ…ηΕΰ≥…ΝΔ |
Θ®8Ζ÷Θ©”–ΦΉΓΔ““ΝΫΈΜ―ß…ζΨυœκάϊ”Ο‘≠Βγ≥ΊΖ¥”ΠΦλ≤βΫπ τΒΡΜνΕ·–‘Υ≥–ρΘ§ΝΫ»ΥΨυ Ι”ΟΟΨΤ§”κ¬Ν
Τ§ΉςΒγΦΪΘ§ΒΪΦΉΆ§―ßΫΪΒγΦΪΖ≈»κ6 molΓΛLΘ≠1 H2SO4»ή“Κ÷–Θ§““Ά§―ßΫΪΒγΦΪΖ≈»κ6 molΓΛLΘ≠1
ΒΡNaOH»ή“Κ÷–Θ§»γœ¬ΆΦΥυ ΨΓΘ
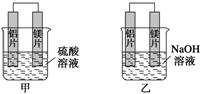
(1)–¥≥ωΦΉ≥Ί÷–’ΐΦΪΒΡΒγΦΪΖ¥”Π ΫΘΚ
’ΐΦΪΘΚ____________________________________________________________ΓΘ
(2)–¥≥ω““≥Ί÷–ΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΚΆΉήΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ
ΗΚΦΪΘΚ________________________________________________________________ΓΘ
(3Θ©ΦΉΆ§―ß”÷ΫΪΝρΥα»ή“ΚΜΜΈΣ≈®œθΥαΖΔœ÷”–ΚλΉΊ…ΪΤχΧε≤ζ…ζΘ§‘ρ‘≠Βγ≥ΊΒΡ’ΐΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ
(4)»γΙϊΦΉ”κ““Ά§―ßΨυ»œΈΣΓΑΙΙ≥…‘≠Βγ≥ΊΒΡΒγΦΪ≤ΡΝœ»γΙϊΕΦ «Ϋπ τΘ§‘ρΙΙ≥…ΗΚΦΪ≤ΡΝœΒΡΫπ τ”Π±»ΙΙ≥…’ΐΦΪ≤ΡΝœΒΡΫπ τΜνΤΟΓ±Θ§‘ρΦΉΜα≈–Εœ≥ω________ΜνΕ·–‘Ηϋ«ΩΘ§Εχ““Μα≈–Εœ≥ω________ΜνΕ·–‘Ηϋ«Ω(Χν–¥‘ΣΥΊΖϊΚ≈)ΓΘ
(5)”…¥Υ Β―ιΘ§Ω…ΒΟΒΫ»γœ¬ΡΡ–©’ΐ»ΖΫα¬έΘΩ(ΓΓΓΓ)
AΘ°άϊ”Ο‘≠Βγ≥ΊΖ¥”Π≈–ΕœΫπ τΜνΕ·Υ≥–ρ ±”ΠΉΔ“β―Γ‘ώΚœ ΒΡΫι÷
BΘ°ΟΨΒΡΫπ τ–‘≤Μ“ΜΕ®±»¬ΝΒΡΫπ τ–‘«Ω
CΘ°ΗΟ Β―ιΥΒΟςΫπ τΜνΕ·Υ≥–ρ±μ“―Ιΐ ±Θ§“―ΟΜ”– Β”ΟΦέ÷Β
DΘ°ΗΟ Β―ιΥΒΟςΜ·―ß―–ΨΩΕ‘œσΗ¥‘”ΓΔΖ¥”Π ήΧθΦΰ”ΑœλΫœ¥σΘ§“ρ¥Υ”ΠΨΏΧεΈ ΧβΨΏΧεΖ÷Έω
(6)…œ ω Β―ι“≤Ζ¥Ιΐά¥÷ΛΟςΝΥΓΑ÷±Ϋ”άϊ”ΟΫπ τΜνΕ·Υ≥–ρ±μ≈–Εœ‘≠Βγ≥Ί÷–ΒΡ’ΐΗΚΦΪΓ±’β÷÷ΉωΖ®________(Ω…ΩΩΜρ≤ΜΩ…ΩΩ)ΓΘ»γ≤ΜΩ…ΩΩΘ§«κΡψΧα≥ωΝμ“ΜΗω≈–Εœ‘≠Βγ≥Ί’ΐΗΚΦΪΒΡΩ…–– Β―ιΖΫΑΗ_________________________________________________________________(»γΩ…ΩΩΘ§¥ΥΩ’Ω…≤ΜΧν)ΓΘ
Θ®8Ζ÷Θ©”–ΦΉΓΔ““ΝΫΈΜ―ß…ζΨυœκάϊ”Ο‘≠Βγ≥ΊΖ¥”ΠΦλ≤βΫπ τΒΡΜνΕ·–‘Υ≥–ρΘ§ΝΫ»ΥΨυ Ι”ΟΟΨΤ§”κ¬Ν
Τ§ΉςΒγΦΪΘ§ΒΪΦΉΆ§―ßΫΪΒγΦΪΖ≈»κ6 molΓΛLΘ≠1 H2SO4»ή“Κ÷–Θ§““Ά§―ßΫΪΒγΦΪΖ≈»κ6 molΓΛLΘ≠1
ΒΡNaOH»ή“Κ÷–Θ§»γœ¬ΆΦΥυ ΨΓΘ
(1)–¥≥ωΦΉ≥Ί÷–’ΐΦΪΒΡΒγΦΪΖ¥”Π ΫΘΚ
’ΐΦΪΘΚ____________________________________________________________ΓΘ
(2)–¥≥ω““≥Ί÷–ΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΚΆΉήΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ
ΗΚΦΪΘΚ________________________________________________________________ΓΘ
(3Θ©ΦΉΆ§―ß”÷ΫΪΝρΥα»ή“ΚΜΜΈΣ≈®œθΥαΖΔœ÷”–ΚλΉΊ…ΪΤχΧε≤ζ…ζΘ§‘ρ‘≠Βγ≥ΊΒΡ’ΐΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ
(4)»γΙϊΦΉ”κ““Ά§―ßΨυ»œΈΣΓΑΙΙ≥…‘≠Βγ≥ΊΒΡΒγΦΪ≤ΡΝœ»γΙϊΕΦ «Ϋπ τΘ§‘ρΙΙ≥…ΗΚΦΪ≤ΡΝœΒΡΫπ τ”Π±»ΙΙ≥…’ΐΦΪ≤ΡΝœΒΡΫπ τΜνΤΟΓ±Θ§‘ρΦΉΜα≈–Εœ≥ω________ΜνΕ·–‘Ηϋ«ΩΘ§Εχ““Μα≈–Εœ≥ω________ΜνΕ·–‘Ηϋ«Ω(Χν–¥‘ΣΥΊΖϊΚ≈)ΓΘ
(5)”…¥Υ Β―ιΘ§Ω…ΒΟΒΫ»γœ¬ΡΡ–©’ΐ»ΖΫα¬έΘΩ(ΓΓΓΓ)
AΘ°άϊ”Ο‘≠Βγ≥ΊΖ¥”Π≈–ΕœΫπ τΜνΕ·Υ≥–ρ ±”ΠΉΔ“β―Γ‘ώΚœ ΒΡΫι÷
BΘ°ΟΨΒΡΫπ τ–‘≤Μ“ΜΕ®±»¬ΝΒΡΫπ τ–‘«Ω
CΘ°ΗΟ Β―ιΥΒΟςΫπ τΜνΕ·Υ≥–ρ±μ“―Ιΐ ±Θ§“―ΟΜ”– Β”ΟΦέ÷Β
DΘ°ΗΟ Β―ιΥΒΟςΜ·―ß―–ΨΩΕ‘œσΗ¥‘”ΓΔΖ¥”Π ήΧθΦΰ”ΑœλΫœ¥σΘ§“ρ¥Υ”ΠΨΏΧεΈ ΧβΨΏΧεΖ÷Έω
(6)…œ ω Β―ι“≤Ζ¥Ιΐά¥÷ΛΟςΝΥΓΑ÷±Ϋ”άϊ”ΟΫπ τΜνΕ·Υ≥–ρ±μ≈–Εœ‘≠Βγ≥Ί÷–ΒΡ’ΐΗΚΦΪΓ±’β÷÷ΉωΖ®________(Ω…ΩΩΜρ≤ΜΩ…ΩΩ)ΓΘ»γ≤ΜΩ…ΩΩΘ§«κΡψΧα≥ωΝμ“ΜΗω≈–Εœ‘≠Βγ≥Ί’ΐΗΚΦΪΒΡΩ…–– Β―ιΖΫΑΗ_________________________________________________________________(»γΩ…ΩΩΘ§¥ΥΩ’Ω…≤ΜΧν)ΓΘ
ΦΉΓΔ““ΝΫΆ§―ß”Οœ¬ΆΦΥυ ΨΉΑ÷ΟΫχ–– Β―ι,ΧΫΨΩœθΥα”κΧζΖ¥”ΠΒΡ≤ζΈοΓΘ
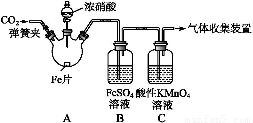
ΈΡœΉΦ«‘Ί:Δώ.‘Ύ≈®œθΥα”κΜνΤΟΫπ τΖ¥”ΠΙΐ≥Χ÷–,ΥφΉ≈œθΥα≈®Ε»ΒΡΫΒΒΆ,Τδ…ζ≥…ΒΡ≤ζΈο”–+4ΓΔ+2ΓΔ-3ΦέΒ»ΒΣΒΡΜ·ΚœΈοΓΘ
Δρ.FeSO4+NO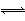 Fe(NO)SO4(ΉΊ…Ϊ)ΓΓΠΛH<0ΓΘ
Fe(NO)SO4(ΉΊ…Ϊ)ΓΓΠΛH<0ΓΘ
Δσ.NO2ΚΆNOΕΦΡή±ΜKMnO4―θΜ·Έϋ ’ΓΘ
ΦΉΒΡ Β―ι≤ΌΉςΚΆœ÷œσΦ«¬Φ»γœ¬:
Β―ι≤ΌΉς | Β―ιœ÷œσ |
¥ρΩΣΒ·Μ…Φ–,Ά®»κ“ΜΕΈ ±ΦδCO2,ΙΊ±’Β·Μ…Φ–ΓΘ |
|
¥ρΩΣΖ÷“Κ¬©ΕΖΜν»ϊ,ΫΪ≈®œθΥαΜΚ¬ΐΒΈ»κ…’ΤΩ÷–,ΙΊ±’Μν»ϊΓΘ | ΈόΟςœ‘œ÷œσΓΘ |
Φ”»»…’ΤΩ,Ζ¥”ΠΩΣ ΦΚσΆΘ÷ΙΦ”»»ΓΘ | ΔΌA÷–”–ΚλΉΊ…ΪΤχΧε≤ζ…ζ,“ΜΕΈ ±ΦδΚσ,ΤχΧε―’…Ϊ÷πΫΞ±δ«≥;B÷–»ή“Κ±δΉΊ…Ϊ;C÷–»ή“ΚΉœ…Ϊ±δ«≥ΓΘ ΔΎΖ¥”ΠΆΘ÷ΙΚσ,A÷–ΈόΙΧΧε Θ”ύΓΘ |
«κΜΊ¥πœ¬Ν–Έ Χβ:
(1)ΒΈ»κ≈®œθΥαΦ”»»«ΑΟΜ”–Οςœ‘œ÷œσΒΡ‘≠“ρ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
(2)Φλ―ι «Ζώ…ζ≥…-3ΦέΒΣΒΡΜ·ΚœΈο,”ΠΫχ––ΒΡ Β―ι≤ΌΉς « ΓΓΓΘ
(3)ΦΉ»Γ…ΌΝΩB÷–»ή“Κ,Φ”»», Β―ιœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ«κ”ΟΜ·―ßΤΫΚβ‘≠άμΫβ Ά‘≠“ρ:ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘΦΉ“άΨίΗΟœ÷œσΒΟ≥ωΒΡΫα¬έ «A÷–”–NO…ζ≥…ΓΘ
(4)““»œΈΣΦΉΒΟ≥ωA÷–”–NO…ζ≥…ΒΡ÷ΛΨί≤ΜΉψΓΘΈΣΜώ»Γ≥δΉψΒΡ÷ΛΨί,““»‘≤…”ΟΗΟΉΑ÷ΟΚΆ≤ΌΉςΫχ––Ε‘’’ Β―ι,““Ής≥ωΒΡΗΡ±δ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ,÷ΛΟς”–NO…ζ≥…ΒΡ Β―ιœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
(5)÷ΛΟςA»ή“Κ÷–Κ§”–Fe3+,―Γ‘ώΒΡ“©ΤΖ «(Χν–ρΚ≈)ΓΓΓΓΓΓΓΘ
A.ΧζΖέ?? B.δεΥ°????? C.Χζ«ηΜ·ΦΊ»ή“ΚD.Νρ«ηΜ·ΦΊ»ή“Κ
“―÷ΣœθΥαοΒ»ή“Κ―’…ΪΈΣάΕ…Ϊ.Ρ≥―ß–ΘΜ·―ßΩΈΆβ–ΓΉιΆ§―ßΟ«‘ΎΉωΆ≠”κ≈®œθΥαΓΔœΓœθΥαΖ¥”ΠΒΡ Β―ι÷–Θ§ΖΔœ÷Ά≠ΚΆ≈®œθΥαΖ¥”ΠΚσ»ή“ΚΈΣ¬Χ…ΪΒ©”–ΚλΉΊ…ΪΤχΧε≤ζ…ζΘ§ΕχΆ≠ΚΆœΓœθΥαΖ¥”ΠΚσ»ή“ΚΈΣάΕ…Ϊ,≤ζ…ζΈό…ΪΤχΧε.ΈΣ≈Σ«εΖ¥”ΠΚσ»ή“Κ―’…Ϊ≥ωœ÷≤ν“λΒΡ‘≠“ρΘ§ΥϊΟ«Ϋχ––ΝΥ Β―ιΧΫΨΩ.
ΓΨ Β―ιΓΩ‘ΎΝΫ÷ß ‘Ιή÷–ΗςΖ≈»κ“Μ–ΓΩιΒ»÷ ΝΩΒΡΆ≠Τ§Θ§Ζ÷±πΦ”»ΥΒ»ΧεΜΐΒΡ≈®HN03Θ®14 mol•
LΘ≠1Θ©ΚΆœΓHN03(4mol . LΘ≠1 ), ΝΔΦ¥”Ο’Κ”–NaOHΒΡΟόΜ®ΖβΉΓ ‘ΙήΩΎΓΘ≥δΖ÷Ζ¥”ΠΚσΆ≠ΨυΈό Θ”ύΓΘ
(1) Cu”κ≈®HNO3Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ______________________________
(2) ”Ο’Κ”–NaOHΒΡΟόΜ®ΖβΉΓ ‘ΙήΩΎΒΡ‘≠“ρ________________
ΓΨΧα≥ωΦΌ…ηΓΩΦΌ…η“ΜΓΔ“ρΈΣΆ≠άκΉ”≈®Ε»¥σ‘λ≥…ΒΡΓΘ
ΦΌ…ηΕΰΓΔ»ή“Κ≥ ¬Χ…Ϊ «“ρΈΣΆ≠”κ≈®œθΥαΖ¥”Π ±≤ζ…ζΒΡΕΰ―θΜ·ΒΣ»ή”ΎΙΐΝΩ≈®œθΥα,Φ”…œΚΆάΕ…ΪΒΡœθΥαΆ≠»ή“ΚΜλ‘Ύ“ΜΤπ, Ι»ή“Κ≥ ¬Χ…ΪΓΘ
ΓΨ…ηΦΤ Β―ιΖΫΑΗ,―ι÷ΛΦΌ…ηΓΩ
(3) …œ ω Β―ι________(ΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±Θ©÷ΛΟςΦΌ…η“Μ≤Μ≥…ΝΔ,‘≠“ρ________________
(4) ΦΉΆ§―ß…ηΦΤ Β―ι―ι÷ΛΦΌ…ηΕΰΘ§«κΑοΥϊΆξ≥…œ¬±μ÷–ΡΎ»ίΘ®Χα Ψ:NO3-‘Ύ≤ΜΆ§ΧθΦΰœ¬ΒΡΜΙ‘≠≤ζΈοΫœΗ¥‘”,”– ±Ρ―“‘Ιέ≤λΒΫΤχΧε≤ζ…ζΘ©

(5)Ά≠ΚΆœΓœθΥαΖ¥”ΠΚσ»ή“ΚΈΣάΕ…ΪΒΡ‘≠άμ_______________ _
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com