
题目列表(包括答案和解析)
| ||

| ||
| ||
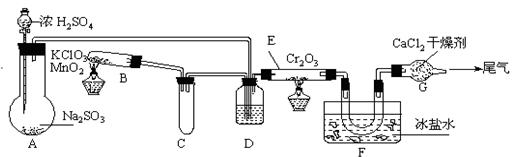
(08浙江省开化中学模拟)实验室中根据2SO2+O2![]() 2SO3;ΔH=-393.2 kJ?mol-1设计如下图所示实验装置来制备SO3固体。请回答下列问题。
2SO3;ΔH=-393.2 kJ?mol-1设计如下图所示实验装置来制备SO3固体。请回答下列问题。
(1)实验前,必须进行的操作是(填操作名称,不必写具体过程)
(2)在A装置中加入Na2SO3固体的同时,还需加几滴水,然后再滴加浓硫酸。加几滴水的作用是
(3)小试管C的作用是
(4)广口瓶D内盛的试剂是 。装置D的三个作用是 ①
② ③
(5)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防温度过高,这样做的原因是
(6)装置F中U型管内收集到的物质的颜色、状态是
(7)装置G的作用是
(8)从G装置导出的尾气处理方法是
2(08浙江省开化中学模拟)实验室中根据2SO2+O2![]() 2SO3;ΔH=-393.2 kJ?mol-1设计如下图所示实验装置来制备SO3固体。请回答下列问题。
2SO3;ΔH=-393.2 kJ?mol-1设计如下图所示实验装置来制备SO3固体。请回答下列问题。
 |
(1)实验前,必须进行的操作是(填操作名称,不必写具体过程)
(2)在A装置中加入Na2SO3固体的同时,还需加几滴水,然后再滴加浓硫酸。加几滴水的作用是
(3)小试管C的作用是
(4)广口瓶D内盛的试剂是 。装置D的三个作用是 ①
② ③
(5)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防温度过高,这样做的原因是
(6)装置F中U型管内收集到的物质的颜色、状态是
(7)装置G的作用是
(8)从G装置导出的尾气处理方法是
(08黄桥中学模拟)三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有: HF、 NO 和 HNO3 。则下列说法错误的是:( )
A.反应过程中,被氧化与被还原的元素的物质的量之比为1:2
B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉
C.一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染
D.若反应中生成1.0mol NO,转移的电子数目为6.02×1023
(08黄桥中学模拟)(8分)电荷相反的离子相互靠近时,由于相反电荷的相互作用,离子的电子云发生变化,称为极化。被异号离子极化而产生离子电子云变形的性质,称为该离子的变形性。阴阳离子都有极化作用和变形性两方面,但由于阳离子的半径小,电场集中,阴离子则相反,所以阳离子的极化作用较大,阴离子的变形性较大。一般说来,阳离子半径越小,电荷越高,极化作用越强;阴离子半径越大,负电荷越多,变形性越强。阴离子被极化后产生变形,正负电荷重心不重合,反过来又可对阳离子产生极化作用,称之为附加极化。附加极化的结果,使阴阳离子产生强烈变形,外层电子云发生重叠,键的极性减弱,键长变短,有离子键向共价键过渡,使物质的溶解度变小,热稳定性降低, 颜色加深…
含复杂阴离子的化合物中,复杂离子中的正态原子对负态原子有极化作用,化合物中的阳离子对阴离子中的负态原子也有极化作用,后一作用与前一作用方向相反,称之为反极化作用。反极化作用的存在表现为阳离子与阴离子中的正态原子共同整体争夺负性原子,使阴离子内部化学键削弱,易发生断键。
(1)BaCO3,FeCO3,ZnCO3,CaCO3分解温度由高到低的顺序是
(2)COF2,COBr2,COCl2,COI2颜色由浅到深的顺序是
(3)试解释Na2CO3的分解温度比NaHCO3高的原因。
(4)碳酸钠易溶于水,碳酸氢钠微溶于水,按理说向饱和的碳酸钠溶液中通入CO2气体应有晶体析出,流行试题就是依此编出来的,当你去做这个实验时,开始时向饱和的碳酸钠溶液中通入CO2气体却没有晶体析出为什么?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com