
题目列表(包括答案和解析)
二甲醚(CH3OCH3)被称为21世纪的清洁、高效能源.
Ⅰ、(1)合成二甲醚反应一:![]()
一定条件下该反应在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是________.
A、低温高压
B、加催化剂
C、体积不变充入N2
D、增加CO浓度
E、分离出二甲醚
(2)合成二甲醚反应二:2CH3OH(g)![]() CH3OCH3(g)+H2O(g).在不同温度下,分别在1 L密闭容器中加入不同物质的量的CH3OH,反应达到平衡,测得各组分的浓度如表:
CH3OCH3(g)+H2O(g).在不同温度下,分别在1 L密闭容器中加入不同物质的量的CH3OH,反应达到平衡,测得各组分的浓度如表:

该反应是________(填“放热”或“吸热”)反应,原因是________(从平衡常数角度说明).
Ⅱ、二甲醚燃料电池的工作原理如下图一所示.

(1)该电池正极的电极反应式为________.
电池在放电过程中,b对应的电极周凰溶液的pH________.(填“增大”、“减小”或“不变”)
(2)以上述电池为电源,通过导线与图二电解池相连.X、Y为石墨,a为1 L 0.1 mol/L KCl溶液,写出电解总反应的离子方程式为________.
(3)室温时,按上述(2)电解一段时间后,取25 mL上述电解后溶液,滴加0.2 mol/L醋酸得到图三(不考虑能量损失和气体溶于水,溶液体积变化忽略不计).
①若图三的B点pH=7,则滴定终点在________区间(填“AB”、“BC”或“CD”).
②C点溶液中各离子浓度大小关系是________.
| 实验组 | 温度/K | 平衡浓度mol/L | ||
| CH3OH | CH3OCH3 | H2O | ||
| 1 | 403 | 0.01 | 0.2 | 0.2 |
| 2 | 453 | 0.02 | 0.3 | 0.4 |
| 0.2×0.2 |
| (0.01)2 |
| 0.3×0.4 |
| (0.02)2 |
| 0.2×0.2 |
| (0.01)2 |
| 0.3×0.4 |
| (0.02)2 |

| ||
| ||
在一个固定体积的密闭容器中,向容器中充入2 mol A 和1 mol B,发生如下反应:2A(g) + B(g) 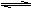 2C(g) + D(g),达到平衡时C的浓度为0.4 mol·L-。维持相同的温度和相同的容积,按下列四种配比作为起始物质,达到新平衡时C的浓度仍是1.2mol/L。
2C(g) + D(g),达到平衡时C的浓度为0.4 mol·L-。维持相同的温度和相同的容积,按下列四种配比作为起始物质,达到新平衡时C的浓度仍是1.2mol/L。
⑴若使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,则正反应为________(填“吸热”或“放热”)反应。
⑵若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度为1.2 mol/L的是_____ (用序号填空)。
| A.4 mol A+2 mol B | B.3mol C+1 mol D+1 mol B |
| C.3 mol C+ 2mol D | D.1.6mol A+0.8 mol B+0.6 mol C |
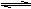 2C(g) + D(g),达到平衡时C的浓度为0.4 mol·L-。维持相同的温度和相同的容积,按下列四种配比作为起始物质,达到新平衡时C的浓度仍是1.2mol/L。
2C(g) + D(g),达到平衡时C的浓度为0.4 mol·L-。维持相同的温度和相同的容积,按下列四种配比作为起始物质,达到新平衡时C的浓度仍是1.2mol/L。| A.4 mol A+2 mol B | B.3mol C+1 mol D+1 mol B |
| C.3 mol C+ 2mol D | D.1.6mol A+0.8 mol B+0.6 mol C |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com