
题目列表(包括答案和解析)
(17分)卡托普利OE)是用于治疗各种原发性高血压的常用药物,可由下列路线合成:
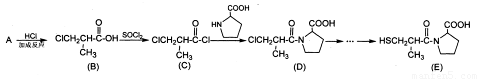
(1) A的结构简式是_______, B中含有官能团的名称是_______。
(2) C→D的反应类型是_______
(3) 已知: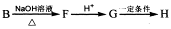 (高分子化合物),则
(高分子化合物),则
B→F的化学方程式为____________________________;
高分子化合物H的结构简式为_____________________。
(4) D的消去产物 有多种同分异构体,如
有多种同分异构体,如 等。写出其中满足下列条件的同分异构体:
等。写出其中满足下列条件的同分异构体:
(i) 含有苯环,不含甲基
(ii) 能与NaOH溶液以物质的量之比1:1完全中和
(iii) 苯环上一卤代物只有一种
___________________________________、 ____________________________
(5) 下列关于卡托普利(¾的说法正确的是_______。
a.能发生取代反应 b.在氧气中充分燃烧的产物有SO2
c.能与Na反应生成氢气 d. E的分子式为
(17分,每空1分,特别说明的除外)下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ______,⑥ ______,⑦ __ __。
(2)画出原子的结构示意图:④___ __ ___,⑧___ 。
(3)在①~12元素中,金属性最强的元素是_____,非金属性最强的元素是______,最不活泼的元素是____。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.常温下⑦的单质和⑧的单质状态不同b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是 (填序号),跟它同周期原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程如下: (2分)。
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:
(17分)
优良的有机溶剂对孟烷、耐热型特种高分子功能材料PMnMA的合成路线如下:
己知芳香化合物苯环上的氢原子可被卤代烷中的烷基取代。如:
(1)B为芳香烃。
①由B生成对孟烷的反应类型是
②(CH3 )2 CHCl与A生成B的化学方程武是
③A的同系物中相对分子质量最小的物质是
(2) 1.08g的C与饱和溴水完全反应生成3.45 g白色沉淀。E不能使Br2的CC14溶液褪色.
①F的官能团是
②C的结构简式是
③反应I的化学方程式是
(3)下列说法正确的是(选填字母)
a. B可使酸性高锰放钾溶液褪色 b. C不存在醛类同分异构体
c. D的酸性比E弱 d. E的沸点高于对孟烷
(4) G的核磁共振氢谱有3种峰,其峰面积之比为3:2:1。G与NaHCO3反应放出CO2。反应II的化学方程式是
(17分)某课外小组设计的实验室制取乙酸乙酯的装置如图14-2所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
第5页
请回答:
(1)浓硫酸的作用是 ;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示180位置的化学方程式: 。
(2)球形干燥管C的作用是 。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示) ;反应结束震荡静止后D中的现象是 .
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出 ;再加入(此空从下列选项中选择) ,然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
(4)有同学拟通过红外光谱仪鉴定所得产物中是否含有“-CH2CH3”, 来确定副产物中存在乙醚。请你对该同学的观点进行评价: 。
(17分)有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
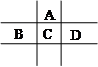
⑴五种元素的名称:A__________,B______________,C____________,D_____________,E______________。
(2)E的最高价氧化物的水化物和NaOH反应的离子方程式是__________________________________________________
(3) 将C的不稳定氧化物和D的单质等物质的量同时通入到品红溶液中,观察到的现象是___________________________,有关反应的离子方程式为________________。
(4)请设计一个简单实验比较A、C的非金属性的强弱:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com