
题目列表(包括答案和解析)
某学习小组在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。为了进一步研究硫酸铜的量对氢气生成速率的影响,该小组同学开始了实验探究。
⑴实验方案:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的锥形瓶中,收集产生的气体。记录单位时间氢气产生的体积。
| 实验混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
其中:V1= ,V6= ,V9= ;
⑵实验装置:甲同学拟选用下列实验装置完成实验:

①你认为最简易的装置其连接顺序是:A接( )( )接( )( )接( )(填接口字母,可不填满。)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶。请你帮助分析原因 。
③实验最后,在读取测量实验中生成氢气的总体积时,你认为合理的是 。
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
 ④ 乙同学认为可选用右图装置中的_____(填A或B)直接与锥形瓶的导管A相连用以测量氢气的体积,理由是 ;实验结束时量筒内的液面高于水槽中液面,立即读数会使氢气的总体积 (填“偏大”“偏小”或“不变”);应进行的操作是 ;
④ 乙同学认为可选用右图装置中的_____(填A或B)直接与锥形瓶的导管A相连用以测量氢气的体积,理由是 ;实验结束时量筒内的液面高于水槽中液面,立即读数会使氢气的总体积 (填“偏大”“偏小”或“不变”);应进行的操作是 ;
⑶实验现象与结论:反应一段时间后,实验A中的金属呈 色,实验E中的金属呈 色;该学习小组最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。
⑷问题讨论:实验室中现有![]() 、
、![]() 、
、![]() 、
、![]() 等4种溶液,可与实验中
等4种溶液,可与实验中![]() 溶液起相似作用的是 ;要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
溶液起相似作用的是 ;要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
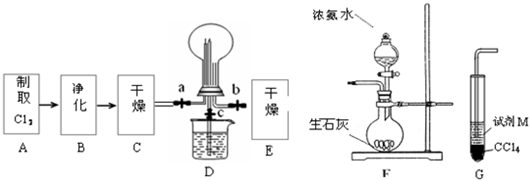

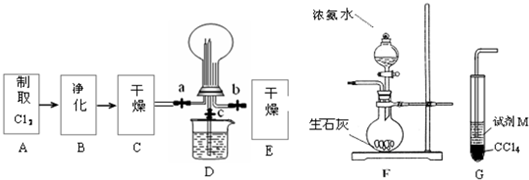

(1)某化学兴趣小组的同学进行Cl2、NH3的制备、性质等实验的流程和部分装置如下:
①请利用A、G装置设计一个简单的实验验证Cl2、Fe3+、I2 的氧化性强弱为Cl2>Fe3+>I2(实验中不断小心振荡G装置中的试管)。请回答A中发生反应的离子方程式 ,试剂M为 溶液,证明氧化性为Cl2>Fe3+>I2的 实验现象是 ;
②已知3Cl2 +2 NH3 = 6HCl + N2 ,当D的烧瓶中充满黄绿色气体后,关闭a、c打开b ,D中的现象为 ,反应一段时间后,关闭b打开c,观察到的现象为 ;
③为使实验顺利进行,请简述F中的分液漏斗的正确操作方法 ;
(2)某废水中含有一定量的Na+、SO32-,可能含有CO32-,某研究小组欲测定其中SO32-离子的浓度,设计如下实验方案:
①从下列试剂中选择试剂x为 (填序号):
A.0.1 mol·L-1 KMnO4(H2SO4酸化)溶液 B.0.5 mol·L-1 1NaOH溶液
C.新制氯水 D.KI溶液
②加入试剂x生成SO42-的离子方程式为 ;
③第ⅲ步的“系列操作”包含的操作名称为 、 、 ;
④证明该废水中是否含有CO32-的实验方案为 。
(15分)
(1)某化学兴趣小组的同学进行Cl2、NH3的制备、性质等实验的流程和部分装置如下: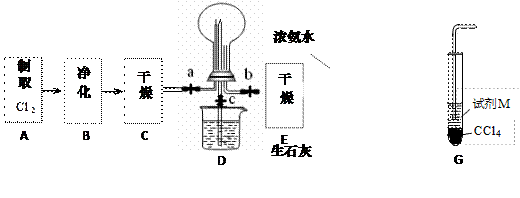
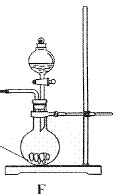
①请利用A、G装置设计一个简单的实验验证Cl2、Fe3+、I2 的氧化性强弱为Cl2>Fe3+>I2(实验中不断小心振荡G装置中的试管)。请回答A中发生反应的离子方程式 ,试剂M为 溶液,证明氧化性为Cl2>Fe3+>I2的 实验现象是 ;
②已知3Cl2 +2 NH3 =" 6HCl" + N2 ,当D的烧瓶中充满黄绿色气体后,关闭a、c打开b ,D中的现象为 ,反应一段时间后,关闭b打开c,观察到的现象为 ;
③为使实验顺利进行,请简述F中的分液漏斗的正确操作方法 ;
(2)某废水中含有一定量的Na+、SO32-,可能含有CO32-,某研究小组欲测定其中SO32-离子的浓度,设计如下实验方案: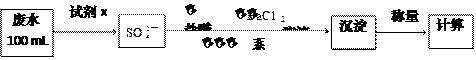
①从下列试剂中选择试剂x为 (填序号):
A.0.1 mol·L-1 KMnO4(H2SO4酸化)溶液 B.0.5 mol·L-1 1NaOH溶液
C.新制氯水 D.KI溶液
②加入试剂x生成SO42-的离子方程式为 ;
③第ⅲ步的“系列操作”包含的操作名称为 、 、 ;
④证明该废水中是否含有CO32-的实验方案为 。
评分说明:
1.本答案供阅卷评分时使用,考生若写出其它正确答案,可参照评分标准给分。
2.计算题只有最后答案而无演算过程的,不给分;只写出一般公式但未能与试题所给的具体条件联系的,不给分。
3.化学方程、离子方程式未配平的,都不给分。
生物部分
题号
1
2
3
4
5
答案
C
C
A
C
C
26.
|