
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
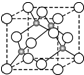 Έο÷ ΫαΙΙ”κ–‘÷
Έο÷ ΫαΙΙ”κ–‘÷ Θ®12Ζ÷Θ© ΓΑΈο÷ ΫαΙΙ”κ–‘÷ Γ±
Θ®1Θ©ΒΎΔσAΓΔΔθA‘ΣΥΊΉι≥…ΒΡΜ·ΚœΈοGaNΓΔGaPΓΔGaAsΒ» «»ΥΙΛΚœ≥…ΒΡ–¬–ΆΑκΒΦΧε≤ΡΝœΘ§ΤδΨßΧεΫαΙΙ”κΒΞΨßΙηœύΥΤΓΘGa‘≠Ή”ΒΡΒγΉ”≈≈≤Φ ΫΈΣ ΓΘ‘ΎGaNΨßΧε÷–Θ§”κΆ§“ΜΗωGa‘≠Ή”œύΝ§ΒΡN‘≠Ή”ΙΙ≥…ΒΡΩ’ΦδΙΙ–ΆΈΣ ΓΘ‘ΎΥΡ¥σΨßΧεάύ–Ά÷–Θ§GaN τ”Ύ ΨßΧεΓΘ
Θ®2Θ©Ά≠ΓΔΧζ‘ΣΥΊΡή–Έ≥…Εύ÷÷≈δΚœΈοΓΘΈΔΝΘΦδ–Έ≥…≈δΈΜΦϋΒΡΧθΦΰ «ΘΚ“ΜΖΫ «ΡήΙΜΧαΙ©Ι¬ΒγΉ”Ε‘ΒΡ‘≠Ή”ΜράκΉ”Θ§Νμ“ΜΖΫ «ΨΏ”– ΒΡ‘≠Ή”ΜράκΉ”
Θ®3Θ©CuCl2»ή“Κ”κ““ΕΰΑΖ(H2N-CH2-CH2-NH2)Ω…–Έ≥…≈δάκΉ”ΘΚ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌ HΓΔNΓΔO»ΐ÷÷‘ΣΥΊΒΡΒγΗΚ–‘”…¥σΒΫ–ΓΒΡΥ≥–ρ « ΓΘ
ΔΎSO2Ζ÷Ή”ΒΡΩ’ΦδΙΙ–ΆΈΣ ΓΘ”κSnCl4ΜΞΈΣΒ»ΒγΉ”ΧεΒΡ“Μ÷÷άκΉ”ΒΡΜ·―ß ΫΈΣ ΓΘ
Δέ““ΕΰΑΖΖ÷Ή”÷–ΒΣ‘≠Ή”ΙλΒάΒΡ‘”Μ·άύ–ΆΈΣ ΓΘ““ΕΰΑΖΚΆ»ΐΦΉΑΖ[N(CH3)3]Ψυ τ”ΎΑΖΘ§ΒΪ““ΕΰΑΖ±»»ΐΦΉΑΖΒΡΖ–ΒψΗΏΒΡΕύΘ§‘≠“ρ « ΓΘ
ΔήΔ«÷–Υυ–Έ≥…ΒΡ≈δάκΉ”÷–Κ§”–ΒΡΜ·―ßΦϋάύ–Ά”– ΓΘ
aΘ°≈δΈΜΦϋ bΘ°ΦΪ–‘Φϋ cΘ°άκΉ”Φϋ dΘ°Ζ«ΦΪ–‘Φϋ
ΔίCuClΒΡΨßΑϊΫαΙΙ»γ”“ΆΦΥυ ΨΘ§Τδ÷–Cl‘≠Ή”ΒΡ≈δΈΜ ΐΈΣ ΓΘ
[Έο÷ ΫαΙΙ”κ–‘÷ ]
‘ΣΥΊX ΈΜ”ΎΒΎΥΡ÷ήΤΎΘ§ΤδΜυΧ§‘≠Ή”ΒΡΡΎ≤ψΙλΒά»Ϊ≤Ω≈≈¬ζΒγΉ”Θ§«“ΉνΆβ≤ψΒγΉ” ΐΈΣ2ΓΘ‘ΣΥΊYΜυΧ§‘≠Ή”ΒΡ3p ΙλΒά…œ”–4ΗωΒγΉ”ΓΘ‘ΣΥΊZ ΒΡ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ «ΤδΡΎ≤ψΒΡ3±ΕΓΘ
Θ®1Θ©X”κYΥυ–Έ≥…Μ·ΚœΈοΨßΧεΒΡΨßΑϊ»γ”“ΆΦΥυ ΨΓΘ
ΔΌ‘Ύ1ΗωΨßΑϊ÷–Θ§XάκΉ”ΒΡ ΐΡΩΈΣ ΓΘ
ΔΎΗΟΜ·ΚœΈοΒΡΜ·―ß ΫΈΣ ΓΘ
Θ®2Θ©‘ΎYΒΡ«βΜ·Έο(H2Y)Ζ÷Ή”÷–Θ§Y‘≠Ή”ΙλΒάΒΡ‘”Μ·άύ–Ά « ΓΘ
Θ®3Θ©ZΒΡ«βΜ·Έο(H2Z)‘Ύ““¥Φ÷–ΒΡ»ήΫβΕ»¥σ”ΎH2YΘ§Τδ‘≠“ρ « ΓΘ
Θ®4Θ©Y ”κZ Ω…–Έ≥…YZ42Θ≠
ΔΌYZ42Θ≠ΒΡΩ’ΦδΙΙ–ΆΈΣ (”ΟΈΡΉ÷Οη ω)ΓΘ
ΔΎ–¥≥ω“Μ÷÷”κYZ42Θ≠ΜΞΈΣΒ»ΒγΉ”ΧεΒΡΖ÷Ή”ΒΡΜ·―ß ΫΘΚ ΓΘ
Θ®5Θ©XΒΡ¬»Μ·Έο”κΑ±Υ°Ζ¥”ΠΩ…–Έ≥…≈δΚœΈο[X(NH3)4]Cl2Θ§1molΗΟ≈δΚœΈο÷–Κ§”–Π“ΦϋΒΡ ΐΡΩΈΣ ΓΘ
Θ®12Ζ÷Θ© ΓΑΈο÷ ΫαΙΙ”κ–‘÷ Γ±
Θ®1Θ©ΒΎΔσAΓΔΔθA‘ΣΥΊΉι≥…ΒΡΜ·ΚœΈοGaNΓΔGaPΓΔGaAsΒ» «»ΥΙΛΚœ≥…ΒΡ–¬–ΆΑκΒΦΧε≤ΡΝœΘ§ΤδΨßΧεΫαΙΙ”κΒΞΨßΙηœύΥΤΓΘGa‘≠Ή”ΒΡΒγΉ”≈≈≤Φ ΫΈΣ ΓΘ‘ΎGaNΨßΧε÷–Θ§”κΆ§“ΜΗωGa‘≠Ή”œύΝ§ΒΡN‘≠Ή”ΙΙ≥…ΒΡΩ’ΦδΙΙ–ΆΈΣ ΓΘ‘ΎΥΡ¥σΨßΧεάύ–Ά÷–Θ§GaN τ”Ύ ΨßΧεΓΘ
Θ®2Θ©Ά≠ΓΔΧζ‘ΣΥΊΡή–Έ≥…Εύ÷÷≈δΚœΈοΓΘΈΔΝΘΦδ–Έ≥…≈δΈΜΦϋΒΡΧθΦΰ «ΘΚ“ΜΖΫ «ΡήΙΜΧαΙ©Ι¬ΒγΉ”Ε‘ΒΡ‘≠Ή”ΜράκΉ”Θ§Νμ“ΜΖΫ «ΨΏ”– ΒΡ‘≠Ή”ΜράκΉ”

Θ®3Θ©CuCl2»ή“Κ”κ““ΕΰΑΖ(H2N-CH2-CH2-NH2)Ω…–Έ≥…≈δάκΉ”ΘΚ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌ HΓΔNΓΔO»ΐ÷÷‘ΣΥΊΒΡΒγΗΚ–‘”…¥σΒΫ–ΓΒΡΥ≥–ρ « ΓΘ
ΔΎSO2Ζ÷Ή”ΒΡΩ’ΦδΙΙ–ΆΈΣ ΓΘ”κSnCl4ΜΞΈΣΒ»ΒγΉ”ΧεΒΡ“Μ÷÷άκΉ”ΒΡΜ·―ß ΫΈΣ ΓΘ
Δέ““ΕΰΑΖΖ÷Ή”÷–ΒΣ‘≠Ή”ΙλΒάΒΡ‘”Μ·άύ–ΆΈΣ ΓΘ““ΕΰΑΖΚΆ»ΐΦΉΑΖ[N(CH3)3]Ψυ τ”ΎΑΖΘ§ΒΪ““ΕΰΑΖ±»»ΐΦΉΑΖΒΡΖ–ΒψΗΏΒΡΕύΘ§‘≠“ρ « ΓΘ
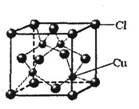
ΔήΔ«÷–Υυ–Έ≥…ΒΡ≈δάκΉ”÷–Κ§”–ΒΡΜ·―ßΦϋάύ–Ά”– ΓΘ
aΘ°≈δΈΜΦϋ bΘ°ΦΪ–‘Φϋ cΘ°άκΉ”Φϋ dΘ°Ζ«ΦΪ–‘Φϋ
ΔίCuClΒΡΨßΑϊΫαΙΙ»γ”“ΆΦΥυ ΨΘ§Τδ÷–Cl‘≠Ή”ΒΡ≈δΈΜ ΐΈΣ ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com