
题目列表(包括答案和解析)
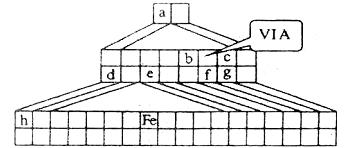
下图是金字塔式元素周期表的一部分(元素周期表的另一种画法),图上标有第VIA族和几种元素的位置。请回答下列问题:

(1)请在上图中描出金属与非金属的分界线,并将铁元素所在族的位置全部涂黑。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第VIIA族,理由是:氢的最外层电子“饱和缺一”。请用电子式表示LiH: 。
(3)f与c或g均能形成一些化合物,据有关材料f与c能形成化合物fc6,f能与g形成化合物f2g。请回答下面问题:
①甲同学通过分析认为fc6此物质不可在O2中燃烧,原因是 。
通过测定知此物质中的6个c原子在分子结构中化学环境相同,则fc 6分子空间构型为 。
②乙同学通过分析认为f2g2是分子晶体,试写出其结构简式: ;
该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液。试写出该过程的反应方程式: 。
(4)下列叙述正确的是( )
A.h的最高价氧化物对应的水化物是一种强碱。
B.硒化氢的稳定性强于f的氢化物的稳定性。
C.c与h形成化合物的水溶液显中性。
D.离子半径:f>g>h>d
E.f与d形成离子化合物为电解质,故该晶体能导电。
F.a、d、e常见氧化物熔沸点高低比较:e>d>a。
下图是金字塔式元素周期表的一部分(元素周期表的另一种画法),图上标有第VIA族和几种元素的位置。请回答下列问题:
(1)请在上图中描出金属与非金属的分界线,并将铁元素所在族的位置全部涂黑。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第VIIA族,理由是:氢的最外层电子“饱和缺一”。请用电子式表示LiH: 。
(3)f与c或g均能形成一些化合物,据有关材料f与c能形成化合物fc6,f能与g形成化合物f2g。请回答下面问题:
①甲同学通过分析认为fc6此物质不可在O2中燃烧,原因是 。
通过测定知此物质中的6个c原子在分子结构中化学环境相同,则fc 6分子空间构型为 。
②乙同学通过分析认为f2g2是分子晶体,试写出其结构简式: ;
该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液。试写出该过程的反应方程式: 。
(4)下列叙述正确的是( )
A.h的最高价氧化物对应的水化物是一种强碱。
B.硒化氢的稳定性强于f的氢化物的稳定性。
C.c与h形成化合物的水溶液显中性。
D.离子半径:f>g>h>d
E.f与d形成离子化合物为电解质,故该晶体能导电。
F.a、d、e常见氧化物熔沸点高低比较:e>d>a。
下图是金字塔式元素周期表的一部分(元素周期表的另一种画法),图上标有第VIA族和几种元素的位置。请回答下列问题:
(1)请在上图中描出金属与非金属的分界线,并将铁元素所在族的位置全部涂黑。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第VIIA族,理由是:氢的最外层电子“饱和缺一”。请用电子式表示LiH: 。
(3)f与c或g均能形成一些化合物,据有关材料f与c能形成化合物fc6,f能与g形成化合物f2g。请回答下面问题:
①甲同学通过分析认为fc6此物质不可在O2中燃烧,原因是 。
通过测定知此物质中的6个c原子在分子结构中化学环境相同,则fc 6分子空间构型为 。
②乙同学通过分析认为f2g2是分子晶体,试写出其结构简式: ;
该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液。试写出该过程的反应方程式: 。
(4)下列叙述正确的是( )
A.h的最高价氧化物对应的水化物是一种强碱。
B.硒化氢的稳定性强于f的氢化物的稳定性。
C.c与h形成化合物的水溶液显中性。
D.离子半径:f>g>h>d
E.f与d形成离子化合物为电解质,故该晶体能导电。
F.a、d、e常见氧化物熔沸点高低比较:e>d>a。
下图是金字塔式元素周期表的一部分(元素周期表的另一种画法),图上标有第VIA族和几种元素的位置。请回答下列问题:
(1)请在上图中描出金属与非金属的分界线,并将铁元素所在族的位置全部涂黑。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第VIIA族,理由是:氢的最外层电子“饱和缺一”。请用电子式表示LiH: 。
(3)f与c或g均能形成一些化合物,据有关材料f与c能形成化合物fc6,f能与g形成化合物f2g。请回答下面问题:
①甲同学通过分析认为fc6此物质不可在O2中燃烧,原因是 。
通过测定知此物质中的6个c原子在分子结构中化学环境 相同,则fc 6分子空间构型为 。
相同,则fc 6分子空间构型为 。
②乙同学通过分析认为f2g2是分子晶体,试写出其结构简式: ;
该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液。试写出该过程的反应方程式: 。
(4)下列叙述正确的是( )
| A.h的最高价氧化物对应的水化物是一种强碱。 |
| B.硒化氢的稳定性强于f的氢化物的稳定性。 |
| C.c与h形成化合物的水溶液显中性。 |
| D.离子半径:f>g>h>d |

 相同,则fc 6分子空间构型为 。
相同,则fc 6分子空间构型为 。| A.h的最高价氧化物对应的水化物是一种强碱。 |
| B.硒化氢的稳定性强于f的氢化物的稳定性。 |
| C.c与h形成化合物的水溶液显中性。 |
| D.离子半径:f>g>h>d |
题号
1
2
3
4
5
6
7
8
答案
A
D
D
B
B
D
B
B
题号
9
10
11
12
13
14
15
16
答案
D
D
B
D
C
D
C
D
17.(1)Fe及Fe后两纵行涂黑(1分)

 (2)∶Li?+?H → Li+[H∶] (2分)
(2)∶Li?+?H → Li+[H∶] (2分)
(3)①硫在SF 中显+6价不可再升,O
中显+6价不可再升,O 不可将负一价氟氧化。(2分)
不可将负一价氟氧化。(2分)
正八面体(1分)
|