
题目列表(包括答案和解析)
(12分)
科学家一直致力研究常温、常压下“人工围氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压力1.0×105Pa、反应时间3 h):
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
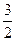 O2(g) ΔH=+765.2kJ·mol-1
O2(g) ΔH=+765.2kJ·mol-1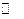 2NH3(g)。设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60 mol H2(g),.反应在一定条件下达到平衡时,NH3的物质的量分数(NH2的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60 mol H2(g),.反应在一定条件下达到平衡时,NH3的物质的量分数(NH2的物质的量与反应体系中总的物质的量之比)为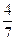 。计算
。计算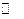 N2(g)+3H2(g)的平衡常数。
N2(g)+3H2(g)的平衡常数。人工固氮是指将氮元素由游离态转化为化合态的过程。据报道,常温、常压、光照条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成的主要产物为NH3,相应的热化学方程式为:N2(g)+3H2O(l) 2NH3(g)+
2NH3(g)+ O2(g) △H="+765.0kJ" /mol。
O2(g) △H="+765.0kJ" /mol。
Ⅰ.请在下图所示的坐标中画出上述反应在有催化剂和无催化剂两种情况下反应体系中的能量变化示意图,并进行标注(包括△H)。

Ⅱ.目前工业合成氨的原理是:N2(g)+
3H2(g) 2NH3(g) △H=-93.0kJ /mol。
2NH3(g) △H=-93.0kJ /mol。
回答下列问题:
(1)氢气的燃烧热△H=_______________kJ/mol。
(2)在恒温恒容密闭容器中进行的合成氨反应,下列能表示达到平衡状态的是_______(填序号)。
a.混合气体的压强不再发生变化
b.混合气体的密度不再发生变化
c.反应容器中N2、NH3的物质的量的比值不再发生变化
d.单位时间内断开a个H-H键的同时形成3 a个N-H键
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
(3)在恒温恒容的密闭容器中,合成氨反应的各物质浓度变化曲线如下图所示。请回答下列问题:
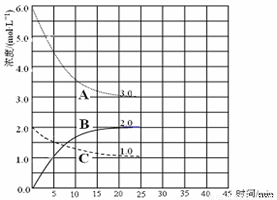
① 表示N2的浓度变化的曲线是 (选填曲线代号“A”、“B”或“C”)。
② 前25 min 内,用H2的浓度变化表示的化学反应平均速率是 。
③在25 min 末反应刚好达到平衡,则该温度下反应的平衡常数K = (计算结果可用分数表示)。若升高温度,该反应的平衡常数值将_______(填“增大”、 “减小”或“不变”)。
(4)在第25 min 末,保持其它条件不变,若升高反应温度并设法保持该温度不变,在第35 min末再次达到平衡。平衡移动过程中H2浓度变化了1.5 mol·L-1,请你在图中画出第25 min ~ 40 min NH3浓度变化曲线。
(5)在一定温度下,将1 mol N2和3 mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8 mol 。
①达平衡时,H2的转化率α1 = ____________。
②在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率为α2,当α1 + α2 =1时,则起始时n (NH3)= ________mol。
(11 分)科学家一直致力研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3,反应的化学方程式如下:N2(g)+ 3H2O(l) 2NH3(g)+ O2(g)。回答下列问题:
(1)进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压力1.0×105Pa、反应时间3 h),则该反应的正反应为 反应(填“吸热”或“放热”)
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
(2)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议: 。
(3)合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)。部分物质的燃烧热数
据如下:
H2(g) :△H=-285.8 kJ・mol-1;
CO(g) :△H =-283.0 kJ・mol-1;
CH4(g) :△H=-890.3 kJ・mol-1 。
已知1mol H2O(g)转变为1mol H2O(l)时放出44.0 kJ热量。写出CH4和H2O在高温下反应的热化学方程式__________________________________。
(4)有人设想寻求适合的催化剂和电极材料,以N2、H2为电极反应物,以HCl——NH4Cl为电解质溶液制成新型燃料电池,请写出该电极的正极反应式
(5)生成的NH3可用于制铵态氮肥,如(NH4)2SO4、NH4Cl,这些肥料显 性,原因是(用离子方程式表示)___________________________,使用时避免与________________物质合施。
(17分)人工固氮是指将氮元素由游离态转化为化合态的过程。据报道,常温、常压、光照条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成的主要产物为NH3,相应的热化学方程式为:N2(g)+3H2O(l) 2NH3(g)+
2NH3(g)+ O2(g) △H="+765.0kJ" /mol。
O2(g) △H="+765.0kJ" /mol。
Ⅰ.请在下图所示的坐标中画出上述反应在有催化剂和无催化剂两种情况下反应体系中的能量变化示意图,并进行标注(包括△H)。
Ⅱ.目前工业合成氨的原理是:N2(g)+3H2(g) 2NH3(g) △H=-93.0kJ /mol。
2NH3(g) △H=-93.0kJ /mol。
回答下列问题:
(1)氢气的燃烧热△H=_______________kJ/mol。
(2)在恒温恒容密闭容器中进行的合成氨反应,下列能表示达到平衡状态的是_______(填序号)。
a.混合气体的压强不再发生变化
b.混合气体的密度不再发生变化
c.反应容器中N2、NH3的物质的量的比值不再发生变化
d.单位时间内断开a个H-H键的同时形成3 a个N-H键
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
(3)在恒温恒容的密闭容器中,合成氨反应的各物质浓度变化曲线如下图所示。请回答下列问题:
① 表示N2的浓度变化的曲线是 (选填曲线代号“A”、“B”或“C”)。
② 前25 min 内,用H2的浓度变化表示的化学反应平均速率是 。
③在25 min 末反应刚好达到平衡,则该温度下反应的平衡常数K = (计算结果可用分数表示)。若升高温度,该反应的平衡常数值将_______(填“增大”、“减小”或“不变”)。
(4)在第25 min 末,保持其它条件不变,若升高反应温度并设法保持该温度不变,在第35 min末再次达到平衡。平衡移动过程中H2浓度变化了1.5 mol·L-1,请你在图中画出第25 min ~ 40 min NH3浓度变化曲线。
(5)在一定温度下,将1 mol N2和3 mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8 mol 。
①达平衡时,H2的转化率α1 = ____________。
②在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率为α2,当α1 + α2 =1时,则起始时n (NH3)= ________mol。
(1)已知热化学方程式如下:N2(g)+3H2O(1)==2NH3(g)+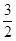 O2(g);△H="+765.2" kJ·mol-1,请在答题卡的坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注。
O2(g);△H="+765.2" kJ·mol-1,请在答题卡的坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注。
(2)明矾能净水的原因: (用离子方程式和必要的文字解释)
___________________________________________________________________________。
(3)已知FeCl3能水解 ,则配制FeCl3溶液的方法是 ____ 。
(4)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
铁锅的锈蚀是 腐蚀(填“析氢”或“吸氧”)
写出铁锅腐蚀负极的电极反应式:
正极的电极反应式:
一、单项选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意)
1.D 2.C 3.B 4.D 5.C 6.A 7.B 8.D
二、不定项选择题(本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分)
9.CD 10.AD 11.D 12.C 13.BC 14.D
三、(本题包括1小题,共14分)
15.
方案一:
(1)在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较
(2)排除因盐酸的加入,稀释氢氧化钠溶液而引起pH减小
方案二:
(1)赶走溶液中少量氧气,隔绝氧气
 (2)CO32―+H2O HCO3―+OH―
(2)CO32―+H2O HCO3―+OH―
(3)做对比实验,取上述NaOH溶液稀释,加入酚酞溶液出现红色且不褪去
方案三:
(1)7 (2)U形管中左边液面下降
(每空2分,共14分)
四、(本题包括2小题,共18分)
16.
⑴ 

⑵CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-
⑶Al4SiC4+2N2 4AlN+SiC+
4AlN+SiC+
⑷可行,该反应是一个焓减、熵略大于0的反应,能自发进行
(每空2分,共8分)
17.
⑴ CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4
生成的CaCO3溶解度小于CaSO4有利于反应向正向进行。
⑵)BCD ⑶CO2 ⑷ABD(每空2分,共10分)
 五、(本题包括1小题,共10分)
五、(本题包括1小题,共10分)
18.
⑴见图示(2分 ,其中过渡元素涂对得1分)
⑵  ⑶ r(Cl-)>r(K+)
⑶ r(Cl-)>r(K+)
⑷ ②④ (5) 
(除⑴外其余每空2分,共10分)
 六、(本题包括1小题,共10分)
六、(本题包括1小题,共10分)
19.
⑴①增大压强 t3~t4 ②
⑵①如图 ②适当增大压强,研究新催化剂
(每空2分,共10分)
七、(本题包括1小题,共8分)
20.
⑴ 2 第2周期第VIA族 (各1分,共2分)
⑵1s22s22p63s23p63d64s2
⑶H+ + AlO2-
+ H2O Al(OH)3
Al(OH)3 Al3+ + 3H2O
Al3+ + 3H2O
⑷4Fe(OH)2 + 2H2O+ O2=4Fe(OH)3
(除⑴外其余每空2分,共8分)
八、(本题包括1小题,共12分)
21.
⑴-80kJ?mol―1
⑵用过量的稀硫酸溶解过量的镁,不断搅拌,过滤,洗净、干燥
⑶加快反应速率,促进平衡向水解的方向移动
⑷取少量洗涤液,在其中加入AgNO3(或BaCl2),无沉淀生成则说明无相应离子。
Ag++Cl-=AgCl↓ Ba2++SO42-=BaSO4↓
(每空2分,共8分)
Ⅲ 1.5mol/L(4分,分步给分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com