
题目列表(包括答案和解析)
pH=6的HC1溶液与pH=4的HC1溶液等体积混合后,溶液中c(OH-)最接近于( )
A.0.5(10-8+10-10)mol/L B.2×10-10mol/L
C.(1×10-10-5×10-5)mol/L D.(10-8+10-10)mol/L
铜是一种与人类关系非常密切的有色金属。常温下,Cu2+在溶液中稳定, Cu+在酸性条件下易发生歧化反应:2Cu+=Cu2++Cu;大多数 +1价铜的化合物是难溶 物,如:Cu20、Cul、CuCl、CuH 等。
(1)在CuCl2溶液中逐滴加入过量KI溶液,可能发生的反应有:
2Cu2++4I-=2CuI↓(白色)+I2; 2Cu2++4I-+2Cl-=CuCl↓(白色)+I2
已知:常温下Ksp(CuCl)=1.20×10-6(mol/L)2; Ksp(CuI)=5.06×10-12(mol/L)2。 由此推断上述反应生成主要沉淀物的化学式是______。
(2)向CuH中加入过量稀HC1,有气体生成,该反应的离子方程式为______。
(3)将 冰 铜(由Cu2S和FeS熔合成含Cu 18%—20%的一种物质)加入熔剂,在髙温下 吹入空气,冰铜中的Cu2S被氧化为Cu2O,生 成 的Cu2O与Cu2S反应生成粗铜。上述两个反应的化学方程式分别是______、______。
(4)常温下,向0.20 mol • L-1硫酸铜溶液中加入氢氧化钠溶液,生成浅蓝色氢氧化铜 沉淀,当溶液的pH = 6时,c(Cu2+)=______mol.L‑1。[已知:Ksp(CuI)=2.2×10-20(mol/L)3]
(5)将0.80 gCuSO4 • 5H2O样品加热分解,其脱水过程中固体质量随温度的变化如下图所示。
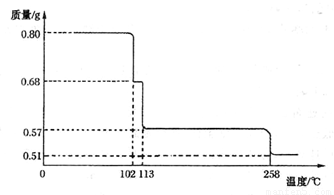
请 确定110°C时固体物质的化学式____________。(要求写出推断过程)
铜是一种与人类关系非常密切的有色金属。常温下,Cu2+在溶液中稳定,Cu+在酸性条件下易发生歧化反应:2Cu+=Cu2++Cu;大多数+1价铜的化合物是难溶物,如:Cu20、Cul、CuCl、CuH 等。
(1)在CuCl2溶液中逐滴加入过量KI溶液,可能发生的反应有:
2Cu2++4I-=2CuI↓(白色)+I2; 2Cu2++4I-+2Cl-=CuCl↓(白色)+I2
已知:常温下Ksp(CuCl)=1.20×10-6(mol/L)2; Ksp(CuI)=5.06×10-12(mol/L)2。由此推断上述反应生成主要沉淀物的化学式是______。
(2)向CuH中加入过量稀HC1,有气体生成,该反应的离子方程式为______。
(3)将冰铜(由Cu2S和FeS熔合成含Cu 18%—20%的一种物质)加入熔剂,在髙温下吹入空气,冰铜中的Cu2S被氧化为Cu2O,生成的Cu2O与Cu2S反应生成粗铜。上述两个反应的化学方程式分别是______、______。
(4)常温下,向0.20 mol ? L-1硫酸铜溶液中加入氢氧化钠溶液,生成浅蓝色氢氧化铜沉淀,当溶液的pH = 6时,c(Cu2+)=______mol.L?1。[已知:Ksp(CuI)=2.2×10-20(mol/L)3]
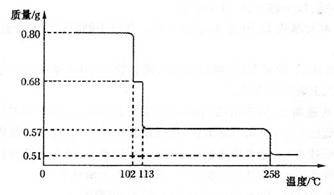
(5)将0.80 gCuSO4 ? 5H2O样品加热分解,其脱水过程中固体质量随温度的变化如下图所示。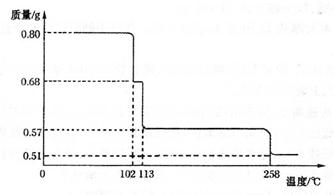
请确定110°C时固体物质的化学式____________。(要求写出推断过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com