
题目列表(包括答案和解析)
| 元素 | 原子结构或性质 |
| A | 原子最外层电子数是内层电子总数的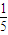 |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌.以下是过氧化氢法生产亚氯酸钠的部分工艺流程图:

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O.
②160 g/LNaOH溶液是指160 gNaOH固体溶于水所得溶液的体积为1 L.
(1)吸收塔内的反应的化学方程式为
2NaOH+2ClO2+H2O2![]() 2NaClO2+2________+________,
2NaClO2+2________+________,
若1 mol ClO2参加反应,则转移电子的物质的量是________mol;
(2)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是________(选填序号),
a.蒸馏
b.蒸发
c.灼烧
d.过滤
e.冷却结晶
要得到更纯的NaClO2·3H2O晶体必须进行的操作是________(填操作名称);
(3)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是________;
(4)160 g/L NaOH溶液的物质的量浓度为________,若要计算该溶液的质量分数,还需要的一个条件是________(用文字说明).
| 元素 | 性质或原子结构 |
| A | 原子核内只有一个质子 |
| B | 单质是空气中含量最多的气体 |
| X | 原子的最外层电子数是次外层电子数的3倍 |
| Y | 短周期元素中原子半径最大的元素 |
| Z | 最高正化合价与最低负化合价的代数和为6 |
| ||
| △ |
| ||
| △ |
| 实验操作 | 实验现象 | 结论及解释 |
| ①取少量NaBr 溶液于试管中,滴加 氯水 氯水 ,振荡;②再加入少量CCl4,振荡,静置. |
①溶液由无色变为橙黄色. ②溶液分层, 上层液体几乎为无色,下层液体为橙红色 上层液体几乎为无色,下层液体为橙红色 . |
氧化性:Z 单质>Br2 离子方程式 Cl2+2Br-═2Cl-+Br2 Cl2+2Br-═2Cl-+Br2 |
现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1。试回答:
(1)B是 、E是________ 。(写元素名称):
(2)A的原子结构示意图 ,B的离子结构示意图
D的单质分子的电子式 , C元素最高价氧化物的水化物的电子式 。
(3)写出B2A3分别与盐酸和氢氧化钠溶液反应的离子方程式:
, 。
(4)比较B、C、E三种元素形成的简单离子其离子半径的大小和氧化性的强弱:(B、C、E离子用实际离子符号表示)
离子半径: ;氧化性: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com